常兴研究组过去开发TAM (Targeted AID-induced mutagenesis),也就是融合核酸酶活性缺陷的Cas9蛋白和胞嘧啶脱氨酶AID,并且发现它具有两个特点。
首先,可以在sgRNA靶向的DNA上,将C/G碱基随机向其它碱基突变,可以用于分析肿瘤耐药性突变及诱导蛋白体外进化等;其次,在偶联UNG抑制剂UGI后,可以在将sgRNA靶向区域中一个小窗口内(5-6个碱基)的C高效向T突变 (Nature Methods, 2016)。
在这一新研究中,博士研究生袁娟娟和马云青首先注意到,98%以上的内含子有保守的GU(内含子开始)和AG(内含子末尾)序列,推测如果可以高效精确地将G突变成A,可以特异性阻断外显子识别,调控内源性mRNA的剪切。
通过这一策略,利用TAM诱导剪接位点DNA上G>A突变,就可以诱导可变外显子(alternative exon)及组成性外显子(constitutive exon)的跳读 (Exon skipping);改变可变剪接位点的选择(Alternative splice site);调节互斥外显子的选择(mutually exclusive exons);诱导小的内含子的包含 (intron retention)。
此外,如果通过TAM将3’剪接位点上游polypyrimidine track中包含的C向T突变,可以促进下游外显子的包含。因此,利用TAM可以成功地实现针对RNA剪接的“loss of function”和”gain of function”调控。
最后,研究人员探索了利用TAM修复杜氏肌营养不良症(DMD)的可行性。DMD是一种致命的遗传疾病(发病率男性中1/4000)。其发病原因在于,遗传突变造成Dystrophin蛋白的完全缺失,引发肌肉萎缩和瘫痪,最终造成心脏或肺功能的衰竭。
如果通过外显子跳读,能产生内部截短的Dystrophin蛋白,可以达到对DMD的治疗效果。因此研究人员构建了DMD病人来源的诱导型多能干细胞,此病人因为外显子删除造成Dystrophin蛋白的完全缺失。通过在剪接位点诱导G>A的突变,研究人员实现了目标外显子的完全跳读,在所有表达TAM的细胞中恢复了Dystrophin的蛋白表达,修复了心肌细胞的缺陷。
该研究得到科技部、国家自然科学基金委、中科院先导计划和上海市科委相关项目的资助。
论文链接
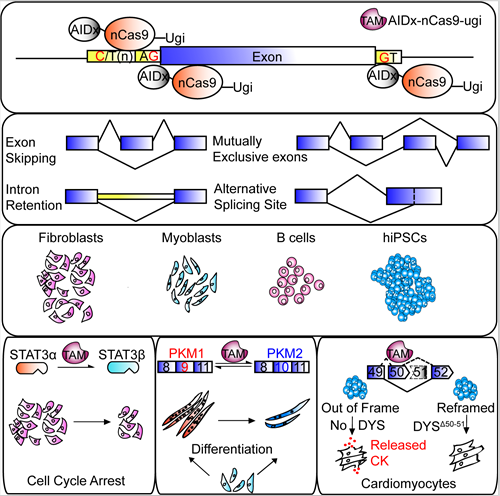
TAM 融合蛋白高效调控外显子跳读、互斥外显子选择、可变剪接位点选择和内含子包含
内容来源:中国科学院来源:中国科学院
原文链接:http://www.cas.cn/syky/201810/t20181008_4665370.shtml
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



