来源:生物探索
CRISPR-Cas9基因组编辑技术目前在动植物中已被广泛用于基因改造研究。其作为一种有前途的技术,也被期望作为矫正致病突变的工具用于临床应用,例如校正体细胞中与疾病相关的等位基因,以及纠正人类胚胎中的致病突变以减轻胎儿和新生儿遗传性疾病的负担。然而,基因编辑的应用最终取决于靶向双链断裂(DSB)触发的DNA修复。目前,我们对人类细胞中的修复机制仍然知之甚少,且其在不同的细胞类型中会有所不同。
近日,《Nature》杂志对发表在医学类预印本杂志《bioRxiv》上的三项评估早期人类胚胎中基因校正可行性的研究成果进行了综述和点评。其研究结果均表明,使用CRISPR–Cas9修饰人类胚胎的基因的突变修复效率低,镶嵌率高,且可能对靶位点或其附近的基因组造成不必要的大变化。
 doi: 10.1038/d41586-020-01906-4
doi: 10.1038/d41586-020-01906-4具体来说,6月5日,《bioRxiv》在线发表了来自英国伦敦弗朗西斯·克里克研究所的Kathy Niakan团队的研究成果。其使用CRISPR–Cas9对胚胎进行POU5F1(该基因在成人组织中的异常表达与肿瘤发生有关)基因突变后,观察到编辑后的细胞中杂合性丧失。在18个经过基因组编辑的胚胎中,约22%出现了意外的基因组编辑结果。该细胞跨越目标靶位点POU5F1以外的区域,以及POU5F1基因所在的6号染色体的片段均存在缺失和重排,影响了POU5F1周围大量的DNA片段。
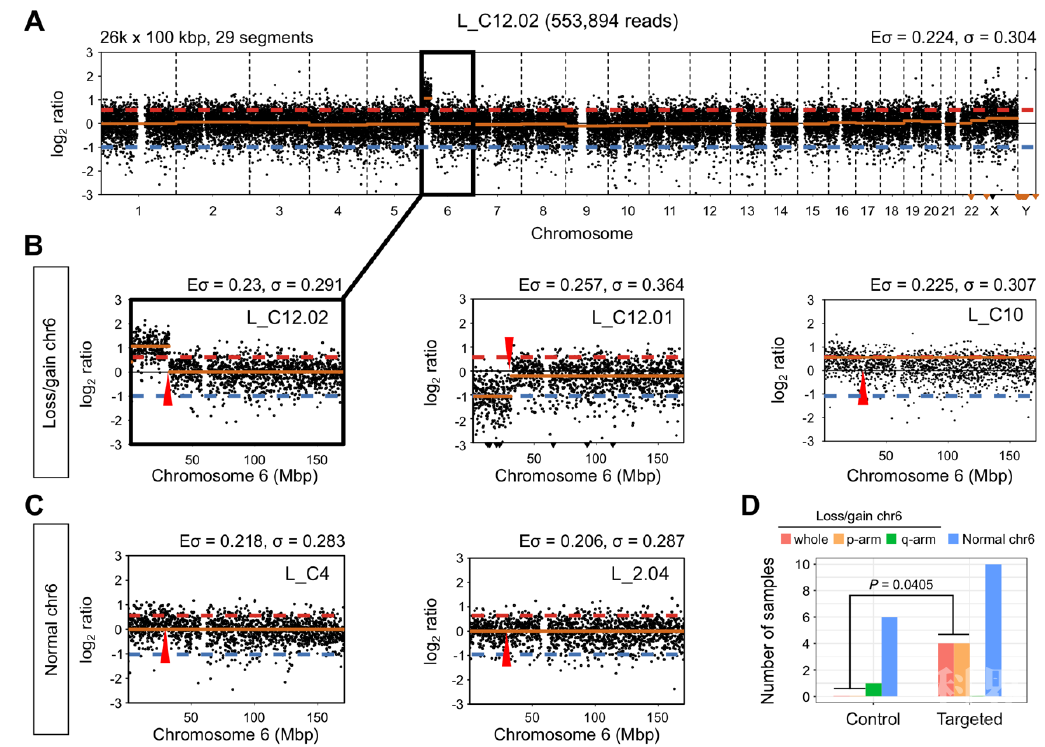 在POU5F1靶向胚胎样本中,6号染色体的片段缺失/增加是普遍的
在POU5F1靶向胚胎样本中,6号染色体的片段缺失/增加是普遍的6月20日,该杂志发表了来自美国哥伦比亚大学的干细胞生物学家Dieter Egli领导的团队对人类胚胎进行CRISPR–Cas9研究的成果。形成该胚胎的精子在EYS2的基因中携带导致失明的突变,而研究人员试图利用CRISPR–Cas9纠正该突变。结果发现,胚胎细胞中最常见的DNA修复结果是微同源性介导的末端连接,其导致胚胎的阅读框发生非镶嵌式恢复。然而,其中大约一半的断裂会未被修复,导致胚胎丢失了EYS所在染色体的很大部分,有时甚至是整个染色体。
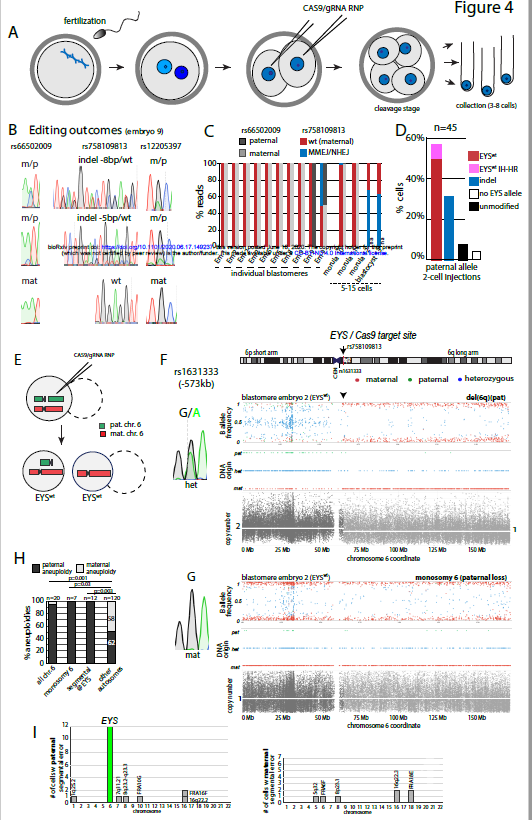 Cas9 RNP注入双细胞期胚胎后染色体丢失和嵌合体
Cas9 RNP注入双细胞期胚胎后染色体丢失和嵌合体同日,来自美国俄勒冈健康与科学大学的生殖生物学家Shoukhrat Mitalipov团队的研究发现,基因转化和NHEJ是植入前人类胚胎中的两种主要DNA DSB修复机制。在杂合性人类胚胎中的突变等位基因的DSB,通过使用完整野生型同源物作为模板在多达40%的目标胚胎中可通过基因转化来修复,而靶向纯合基因座可促进非同源末端连接(NHEJ)与基因转换的相互作用,并导致在两个基因座上均携带相同indel突变的胚胎。尽管基因转换可用于基因校正,但其也会导致广泛的杂合性(LOH),带来了严重的安全隐患。
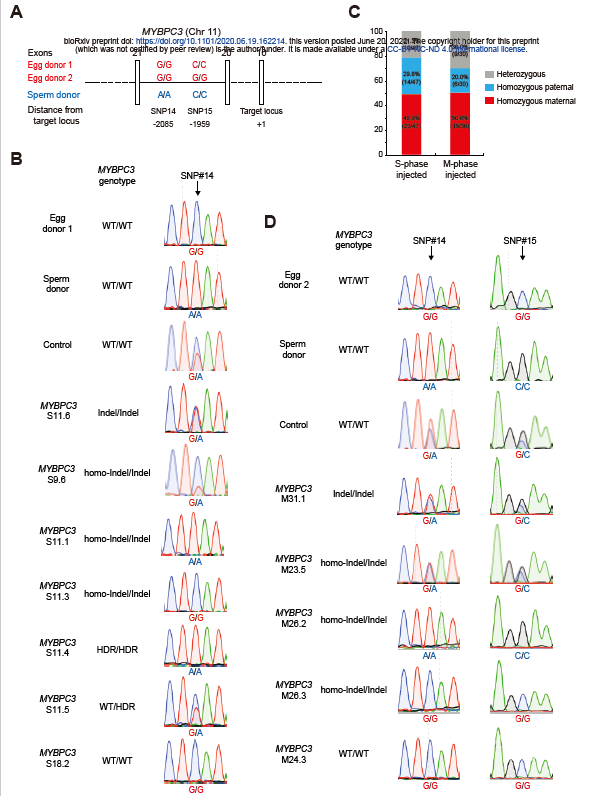 MYBP3胚胎基因转化导致的LOH
MYBP3胚胎基因转化导致的LOH这三项研究均显示出CRISPR基因编辑会导致胚胎染色体发生混乱,产生较大的DNA缺失和重排,这一结果也增加了科学家们对可遗传基因组编辑的安全性担忧。
End
参考资料:[1] CRISPR gene editing in humanembryos wreaks chromosomal mayhem
[2] Frequent loss-of-heterozygosityin CRISPR-Cas9-edited early human embryos
[3] Reading frame restoration at theEYS locus, and allele-specific chromosome removal after Cas9 cleavage in humanembryos
[4] FREQUENT GENE CONVERSION IN HUMANEMBRYOS INDUCED BY DOUBLE STRAND BREAKS
来源:biodiscover 生物探索
原文链接:https://mp.weixin.qq.com/s?__biz=MzU2MTQ2MDE0Ng==&mid=2247513505&idx=1&sn=3e0a84c6f127f1130ab84e62a1817856&chksm=fc7a937ccb0d1a6acd9252c3803aacac36704f068724e4619a82f3a11db573b9c6fbfd988893#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



