来源:BioArt
撰文 | 十一月1882年,德国生物学家Walther Flemming在卵细胞细胞核中发现了灯刷染色体的存在。灯刷染色体中DNA形成DNA环(DNA loop),DNA 环的存在使得相隔较远的区域可以相互接近并相互作用,在基因表达调控中具有非常重要的作用。在2019年,于洪涛研究组与Jan-Michael Peters研究组分别在Science 上发文,揭开了黏连蛋白Cohensin在DNA环挤压(DNA loop extrusion)过程中的关键作用(详见BioArt报道:Science | 于洪涛组用单分子成像证实粘连蛋白有DNA环挤压功能)【1,2】。黏连蛋白像钩环一样夹在DNA上,介导DNA的成环运动,黏连蛋白在其中发挥着马达蛋白类似的作用。凝缩蛋白作为染色体结构维持(Structure maintenance of chromosome , SMC)蛋白质复合体中的关键组分,也同样在DNA环挤压过程中发挥着类似于马达蛋白的作用。但其实关于凝缩蛋白复合体是如何将DNA压缩成为染色体的动态过程研究还并不清楚。
2020年3月4日,荷兰代尔夫特理工大学Cees Dekker研究组在Nature发文DNA-loop extruding condensin complexes can traverse one another,发现凝缩蛋白进行DNA环挤压,当两个DNA环结构靠近的时候,凝缩蛋白会穿过DNA环促进DNA形成Z-loop结构,因此凝缩蛋白可能是通过形成多种多样的环结构促进染色体凝缩的。

染色体空间结构的正常维持对于细胞维持正常运转非常重要。SMC蛋白质复合体包括凝缩蛋白、黏连蛋白以及Smc5/6复合体,在生物体中DNA组织发挥着关键的作用【3】。通过Hi-C等实验方式科学家们发现DNA环挤压的过程依赖于凝缩蛋白的DNA移位酶活的活性以及其挤压DNA的能力。但是单个凝缩蛋白复合体分子是如何进行DNA环挤压的以及如何促进有丝分裂期DNA的凝缩的还很不清楚。为了对凝缩蛋白介导的DNA环之间的相互作用关系进行研究,作者们对出芽酵母中凝缩蛋白对于λ-DNA底物产生的环挤压过程进行可视化研究。λ-DNA被挂在钝化表面之上,并且作者们使用Sytox orange染料【4】进行染色。在外加凝缩蛋白复合体以及ATP之后,在钝化表面会出现较亮的DNA聚集点,这些聚集点是DNA环挤压产生的地方。通过施加一个垂直于DNA平面的缓冲液流(Buffer flow),可以将其拉伸成为环状(图1)。2018年的一篇Science文章文中作者们使用的蛋白质浓度是1nM,在此条件下可以对形成的单个DNA环进行研究【4】。但是根据前人的研究发现,在酵母的细胞核中蛋白质的浓度更高大约为2-10nM,每10kbp的DNA中存在约一个凝缩蛋白复合体分子【5,6】。在较高蛋白质浓度下,作者们发现会出现两个DNA环的存在,并且这两个DNA环之间存在相互影响。
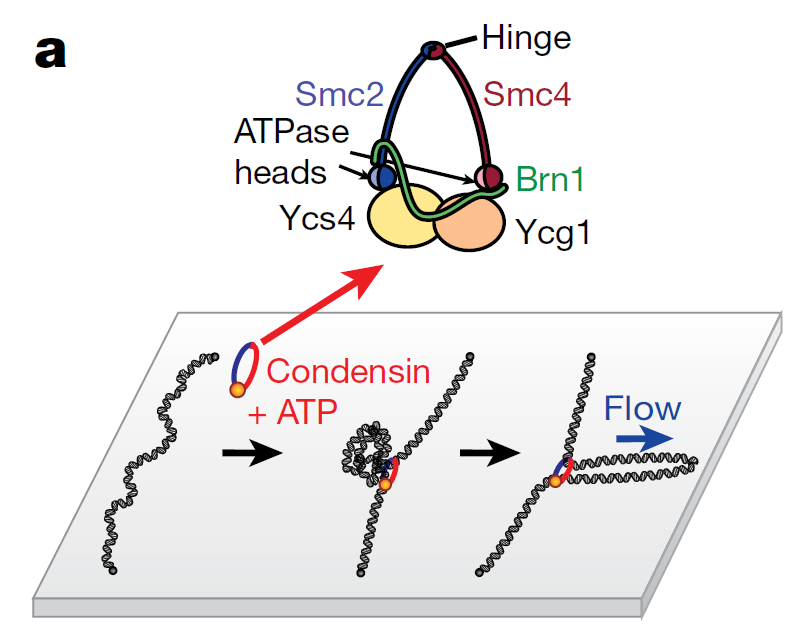 图1 体外建立凝缩蛋白促进DNA环挤压形成体系示意图
图1 体外建立凝缩蛋白促进DNA环挤压形成体系示意图通过单分子的成像,作者们发现,两个DNA环之间即使距离很远也存在拮抗相关的关系。由第二个凝缩蛋白挤压形成的新DNA环会以初始DNA环的收缩为代价。DNA张力越大,环的收缩越明显。但时,分离的两个单独DNA环并不是在高浓度凝缩蛋白存在情况下出现的最主要DNA结构。相反,主要存在的DNA结构是三个双链DNA存在的结构,这种结构作者们将其称为Z-loop(图2)。在凝缩蛋白浓度超过6nM之后,Z-loop是存在的主要λ-DNA结构。第一个环的形成时间长度依赖于凝缩蛋白的浓度,浓度越高形成时间越短,但是第二个“环中环”(loop-within-a-loop)的结构到Z-loop形成的时间则不依赖于蛋白的浓度。而且作者们发现,Z-loop形成的速度要比形成单个DNA环的速度要更快,而且Z-loop一旦形成会比单个DNA环的结构更加稳定。而且Z-loop中DNA是向两边方向对称扩展,说明DNA可以同时从两个方向同时被拉进Z-loop。
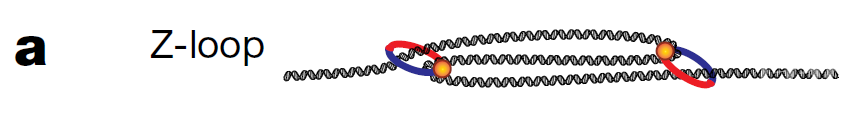
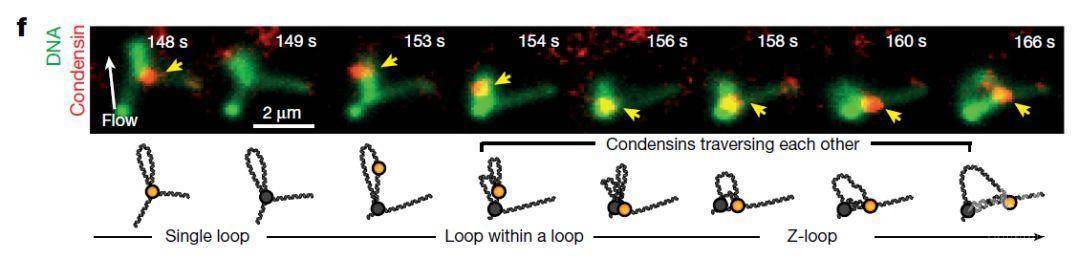 图2 Z-loop的形成过程
图2 Z-loop的形成过程总的来说,Cees Dekker研究组的工作从单分子成像的角度上给出了有丝分裂期间DNA双链压缩的可能机制。作者们建立了以出芽酵母体内凝缩蛋白浓度为蓝本的体外凝缩蛋白单分子成像系统,发现凝缩蛋白作为单向马达蛋白驱动DNA链环挤压过程中形成Z-loop的DNA结构,并发现Z-loop结构可以双向推动DNA被挤压到环结构中,促进染色体的凝缩,为染色体凝缩模型提供了新的DNA环结构形成的理论依据。
原文链接:https://doi.org/10.1038/s41586-020-2067-5
参考文献
1. Kim, Y., Shi, Z., Zhang, H., Finkelstein, I. J. & Yu, H. Human cohesin compacts DNA by loop extrusion. Science 366, 1345-1349, doi:10.1126/science.aaz4475 (2019).2. Davidson, I. F. et al. DNA loop extrusion by human cohesin. Science 366, 1338-1345, doi:10.1126/science.aaz3418 (2019).3. Uhlmann, F. SMC complexes: from DNA to chromosomes. Nat Rev Mol Cell Biol 17, 399-412, doi:10.1038/nrm.2016.30 (2016).4. Ganji, M. et al. Real-time imaging of DNA loop extrusion by condensin. Science 360, 102-105, doi:10.1126/science.aar7831 (2018).5. Wang, B. D., Eyre, D., Basrai, M., Lichten, M. & Strunnikov, A. Condensin binding at distinct and specific chromosomal sites in the Saccharomyces cerevisiae genome. Molecular and cellular biology 25, 7216-7225, doi:10.1128/mcb.25.16.7216-7225.2005 (2005).6. Ho, B., Baryshnikova, A. & Brown, G. W. Unification of Protein Abundance Datasets Yields a Quantitative Saccharomyces cerevisiae Proteome. Cell Syst 6, 192-205 e193, doi:10.1016/j.cels.2017.12.004 (2018).来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652481807&idx=4&sn=05f45a88d8c238f952ec8a8ee15cf617&chksm=84e23abbb395b3ad0ce0e3aa268415f85de660bb96e1b702a3c35828f92806c57ee4190f1e5b#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn