来源:中科院深圳先进院
近日,中国科学院深圳先进技术研究院计算机辅助药物设计中心主任袁曙光课题组与纳米中心李红昌课题组合作,通过生物计算的方法发现一大类药物分子可以有效阻止新冠病毒的侵染。
新冠病毒仍旧在全球肆虐。截止2020年11月5日,全球累计感染新冠病毒的人数超过4800万例,死亡病例超过122万人。目前还没有针对新冠病毒的特效药和疫苗上市。由于疫苗研发周期长,新冠病毒突变迅猛,疫苗最后的安全性和有效性还有待长时间验证。寻求有效的阻断机理和相关药物分子,成为治疗新冠迫在眉睫需要解决的问题。
目前针对新冠病毒生命周期的不同过程,科学家采用了不同的策略和药物,例如阻断RNA释放、阻断无须蛋白自组装、阻断RNA合成酶等,但现有的这些方法都不能完全、特效地清除和阻断病毒。本工作利用计算药学方法,针对人体ACE2受体蛋白筛选抑制剂。团队发现,抑制剂与ACE2结合后,其三维结构会发生很大变化。这些变化将导致病毒S蛋白的BRD结构域难以与人体ACE2蛋白相识别和结合,从而阻止病毒入侵正常的人体细胞(图2)。

图1. 新冠病毒生命周期以及抗病毒策略
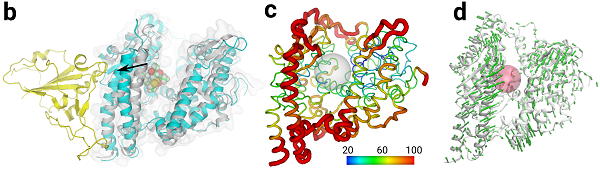
图2. 计算机分子动力学表明 ACE2受体本身柔性非常大(图c与图d)。ACE2与抑制剂结合前后构象会发生很大变化(图b白色与天蓝色卡通),从而阻止病毒S蛋白的BRD结构域(图b黄色卡通)与AC2原有的特异性结合。
由于初始所筛选活性最高的药物分子属于HDAC的抑制剂,团队系统性地对大部分临床以及上市的HDAC抑制剂做了系统性的细胞活性测试。结果表明,多个HDAC的抑制剂均可有效阻断新冠病毒侵染正常细胞。其中活性最高的药物分子,对病毒有效抑制EEC50高达90nM。
通过网络药理学系统性分析与新冠病毒侵入途径相关的蛋白调控网络发现,ACE2与多个HDAC蛋白对新冠病毒侵染以及病毒的生理周期过程发挥着重要作用(图3)。本研究发现有望为治疗新冠提供新机理和新思路。其中所发现的药物分子有效性最终还有待临床实验验证。
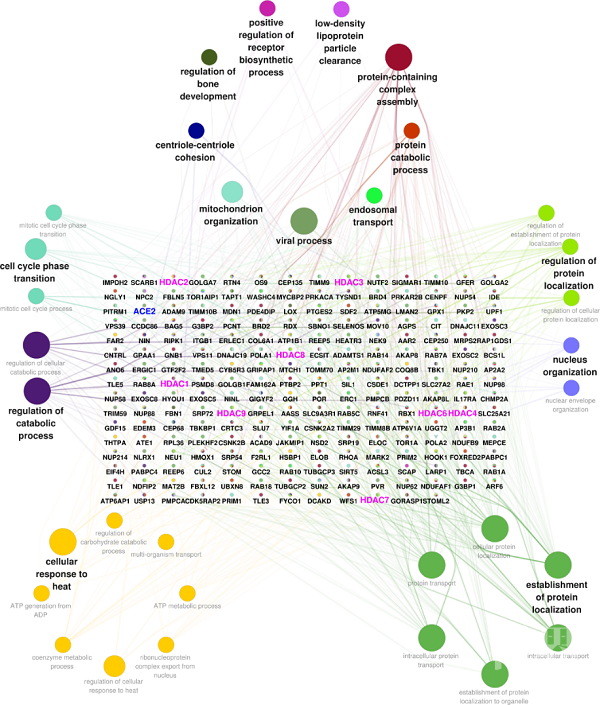
图3. 系统生物学分析发现ACE2与多个HDAC蛋白对病毒的侵染以及在病毒的生命周期中发挥着重要作用。
相关工作以封面故事形式发表在ACS Pharmacology & Translational Science期刊上(doi:10.1021/acsptsci.0c00163)。本工作第一单位和通讯单位均为深圳先进院,刘科副研究员、博士后邹荣峰和博士生崔文强为共同一作。陈显翀副研究员、李红昌研究员为共同通讯作者,袁曙光研究员为最后通讯作者。(点击左下角阅读原文)

来源:zky_szxjy 中科院深圳先进院
原文链接:http://mp.weixin.qq.com/s?__biz=MzA4NzI3NTYyNA==&mid=2652850049&idx=1&sn=8cf441ade57c93962a7e389eed6b977f
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



