来源:生物谷
个性化治疗可根据患者需求量身定制治疗方案。在罕见疾病中,开发针对一部分患者的靶向治疗方法可能是由于特定的医疗需求或现有治疗方法上存在的技术限制。较罕见的情况是,鉴定单例患者中的突变导致了患者特异性基因治疗方法的开发。
在一项新的研究中,Morelli等人在早发性运动神经病变的非典型病例中,通过广泛的靶向遗传筛选确定了甘氨酰-tRNA合成酶(glycyl-tRNA-synthetase, GARS)基因中的致病性缺失。这个基因的显性突变是造成腓骨肌萎缩症2D型(Charcot-Marie-Tooth disease type 2D, CMT2D)的原因。相关研究结果近期发表在Journal of Clinical Investigation期刊上,论文标题为“Allele-specific RNA interference prevents neuropathy in Charcot-Marie-Tooth disease type 2D mouse models”。
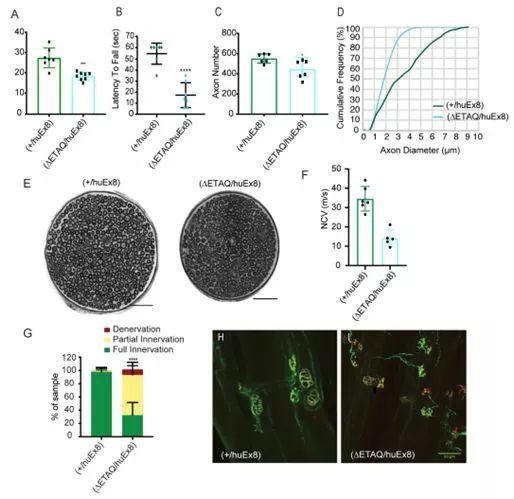
图片来自Journal of Clinical Investigation, 2019, doi:10.1172/JCI130600。
这些作者开发出靶向显性四个氨基酸缺失的等位基因特异性RNA干扰(RNAi)方法。在新生动物中,腺相关病毒(AAV)载体介导的脑室内递送阻止了在GARS基因中带有相同缺失的小鼠模型中的神经病变发生。但是,正如在其他发生轴突变性的神经病变中所观察到的那样,神经病变发生后的RNAi治疗会导致部分获益,甚至没有益处,这取决于干预的时机。一种靶向CMT2D小鼠模型中P278KY等位基因的类似方法显示出相似的结果。
这篇论文提供了用于概念验证的等位基因特异性策略,用于治疗CMT2D中的显性突变。尽管这种方法本质上是突变特异性的,但是这些作者指出,通过相同的载体将GARS转录本的非特异性敲除和RNAi抵抗性GARS基因拷贝的重新导入也是一种潜在的治疗策略。从翻译的角度来看,这种转基因表达盒的复杂性可能是一个挑战。但是,这篇论文清楚地总结了针对罕见疾病的个性化治疗方法开发的困难,并突出了具有不典型表现的超罕见突变患者的艰巨诊断历程。
参考文献:
1.Kathryn H. Morelli et al. Allele-specific RNA interference prevents neuropathy in Charcot-Marie-Tooth disease type 2D mouse models. Journal of Clinical Investigation, 2019, doi:10.1172/JCI130600.
2.Giuseppe Ronzitti et al. Interfering in Charcot-Marie-Tooth disease 2D. Science Translational Medicine, 2019, doi:10.1126/scitranslmed.aaz3712.
来源:BIOONNEWS 生物谷
原文链接:http://mp.weixin.qq.com/s?__biz=MzI2NjY1NjA5Mw==&mid=2247504570&idx=3&sn=bf9e898f47672325b07f8d1ea2d067fa&chksm=ea885288ddffdb9e3fdc32bfbeb238eb252b82f601294743f9743672ffc14291cc9e800d95a7&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn


