来源:BioArt
成体造血干细胞和祖细胞(HSPC)通过分化产生髓系(myeloid)和淋系(lymphoid)细胞来维持造血系统,成为研究细胞分化的经典模型之一。对这一分化模型的一般假设是,造血干细胞在分化中逐渐丧失多能性,并且成为只能产生特性细胞类型的祖细胞,例如失去分化成髓系细胞能力的骨髓淋巴祖细胞(CLP)。这种传统的树状分化路径随着单细胞技术的发展受到了诸多的挑战。例如通过单细胞谱系示踪(lineage tracing)技术Shalin Naik等发现LMPP这一曾经被认为具有多能性的祖细胞类型,在单细胞层面具有显著的异质性,只有少数的细胞具有真正的多能性,大部分细胞已经具有确定的分化路径并且缺乏分化成为其他类型细胞的能力【1】。多个单细胞转录组测序研究也在转录组层面揭示了类似的造血干细胞异质性【2】。然而,如何发现新的基因标记,并且对具有不同基因表达谱的细胞类群进行分离和功能鉴定依旧是当前研究的重点。

图 1 造血干细胞的分化模型从早期的树状到现在更加复杂的并行模型。每种细胞类群中都具有大量有不同分化偏好的细胞。(图片来自【2】)
2020年10月19日,Shalin Naik研究组在Nature Immunology杂志在线发表了 A new lymphoid-primed progenitor marked by Dach1 downregulation identified with single cell multi-omics 的研究论文。该研究首先利用自研的单细胞测序方法分析了小鼠造血干细胞(HSC)转录组的异质性,并且鉴定了Dach1表达下调作为标记早期淋系分化的标志事件。通过构建Dach1标记小鼠和进一步的功能试验证实了Dach1表达下调的LMPP细胞类群已经丧失了分化成髓系细胞的能力。这一类群被命名为LPP(lymphoid-primed progenitor)。 作者首先通过流式细胞筛选,对小鼠的骨髓造血干细胞(Lin-Sca-1+c-Kit+)进行了单细胞转录组测序,并且发现了这些未分化的干细胞具有大量的异质性,不同的细胞已经开始表达不同血细胞的标志基因,其中最显著的就是表达髓系细胞标志基因的细胞类群和表达淋系细胞标志基因的细胞类群。在大量的标志基因中,Dach1与髓系细胞的标志基因共表达,而在淋系细胞中很少表达。而Dach1基因在造血干细胞分化中的功能尚未被研究。
作者首先通过流式细胞筛选,对小鼠的骨髓造血干细胞(Lin-Sca-1+c-Kit+)进行了单细胞转录组测序,并且发现了这些未分化的干细胞具有大量的异质性,不同的细胞已经开始表达不同血细胞的标志基因,其中最显著的就是表达髓系细胞标志基因的细胞类群和表达淋系细胞标志基因的细胞类群。在大量的标志基因中,Dach1与髓系细胞的标志基因共表达,而在淋系细胞中很少表达。而Dach1基因在造血干细胞分化中的功能尚未被研究。
接下来,作者敲除了Dach1基因,然而并没有观察到HSPC细胞分化的改变。接着,作者构建了Dach1荧光标记小鼠并且检查了Dach1在不同HSPC细胞(LT-HSC, ST-HSC, MPP2, MPP3, MPP4/LMPP, CLP)中的分布,发现了Dach1表达在LMPP中有很大的异质性。通过进一步分离LMPP中Dach1+和Dach1-的细胞类群,作者发现Dach1- LMPP 和之前文献中报道的亚群均不重合(例如ELP),代表了一个新的未定义的细胞类群并将其命名为LPP。
为了进一步研究LPP的转录组表达,作者对包括LPP在内的各类造血干细胞进行了无偏单细胞测序,发现了LPP有特定的基因表达谱并且高表达多种淋系细胞的标志基因,包括Dntt,Satb1等。同时LPP又和CLP表达不同的标志基因,因此LPP和CLP是不同的细胞类群。细胞分化轨迹分析(trajectory analysis)暗示了在分化路径上LPP处于CLP的上游。体外和体内的功能试验同时验证了LPP几乎丧失了分化为髓系细胞的能力,仅保留了分化为淋系细胞的能力。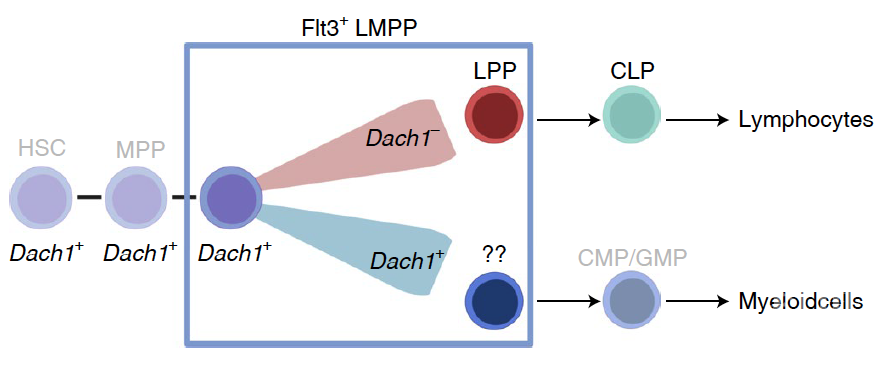 总的来说,该研究不仅通过单细胞测序刻画了造血干细胞转录组的异质性,还通过鉴定具体的标记基因Dach1,分离了具有不同分化潜力的细胞亚群并且验证了其分化能力。研究揭示了LMPP实际上是由至少两种不同类型的细胞所构成的,其中LPP已经不具有分化为髓系细胞的能力,进一步修正了造血干细胞的分化模型。值得注意的是,Dach1已经被报道和细胞周期密切相关,并且在肿瘤的增殖中扮演着重要作用【3】。其背后是否有着相似的基因调控网络还有待于进一步研究。对Dach1在造血干细胞细胞分化中功能的深入研究也将深化我们对于癌症的了解。
总的来说,该研究不仅通过单细胞测序刻画了造血干细胞转录组的异质性,还通过鉴定具体的标记基因Dach1,分离了具有不同分化潜力的细胞亚群并且验证了其分化能力。研究揭示了LMPP实际上是由至少两种不同类型的细胞所构成的,其中LPP已经不具有分化为髓系细胞的能力,进一步修正了造血干细胞的分化模型。值得注意的是,Dach1已经被报道和细胞周期密切相关,并且在肿瘤的增殖中扮演着重要作用【3】。其背后是否有着相似的基因调控网络还有待于进一步研究。对Dach1在造血干细胞细胞分化中功能的深入研究也将深化我们对于癌症的了解。
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652504112&idx=6&sn=1500a445b6253f33ba7fcd48a8181168&chksm=84e19384b3961a920ff9dca71018ef6e574a8cef073d541e5cfceeb0a7605718038bfb4c70cc#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



