来源:研之成理

▲第一作者:王强;通讯作者:游书力
从简单易得的 2-芳基吡啶类衍生物和商业可得的芳基溴代物出发,使用 Rh(C2H4)2Cl)]2 作为铑前体,TADDOL 骨架衍生的单膦配体作为手性配体,发展了吡啶导向的不对称 C-H 芳基化反应,高效地合成了一系列含有吡啶基团的轴手性联芳基化合物。
背景介绍
具有轴手性的联芳基骨架作为一种重要的结构单元广泛存在于具有生物活性的天然产物, 另外轴手性化合物在材料科学和药物化学中也应用广泛, 同时在不对称催化反应中还作为一种优势的手性配体骨架。与酶催化的动力学拆分、过渡金属催化的不对称偶联反应以及不对称有机催化等构建轴手性化合物的方法相比,利用过渡金属催化的不对称 C-H 官能团化策略来构建轴手性化合物是一类非常高效的方法,主要包括 Rh(III) 和 Pd(II) 催化体系,并且取得了非常不错的研究成果。我们课题组在这方面也取得了一些研究工作(Angew. Chem. Int. Ed. 2014, 53, 13244;J. Am. Chem. Soc. 2016, 138, 5242)。尽管如此,利用 Rh(III) 催化的策略合成轴手性联芳基化合物还存在着一些不足,例如对于简单的 2-芳基吡啶类化合物并不能得到很好的对映选择性控制。
研究出发点
基于轴手性化合物的重要性及研究现状,游书力教授课题组试想能否寻找一些高效的催化体系去解决这一问题。受 Glorius 教授的工作启发(Angew. Chem., Int. Ed. 2018, 57, 9950),我们使用 Rh(I)催化体系,对芳基吡啶的不对称碳氢键芳基化反应进行了研究,最终从简单的 2-芳基吡啶类化合物出发,芳基溴代物为芳基化试剂,高效合成了一系列轴手性联芳基化合物,相关实验结果发表在 J. Am. Chem. Soc. 上。
图文解析
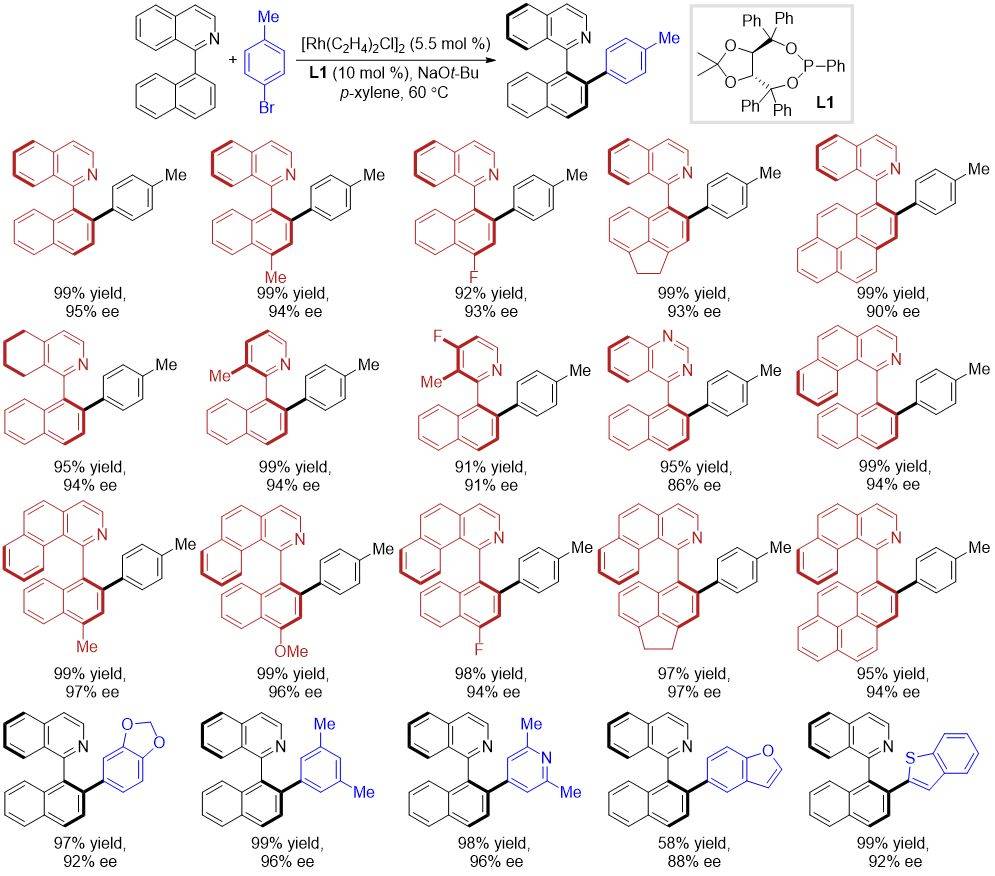
游书力课题组通过对反应的温度、溶剂、配体和碱等条件的考察,发现以 Rh(C2H4)2Cl)]2 和 TADDOL 骨架衍生的苯基亚磷酸酯 L1 作为催化剂,在 60 ºC 的条件下,以 99 % 收率和 95% ee 对映选择性得到轴手性联芳基分子。随后他们对反应的底物普适性进行了考察。结果表明,对于不同的 2-芳基取代的吡啶衍生物都能很好地兼容,反应均能得到优秀的区域选择性、收率和对映选择性。对于芳基溴代物,可以兼容不同位置的取代基,以及给电子基团和吸电子基团,同时杂芳环类底物也可以很好地参与反应。
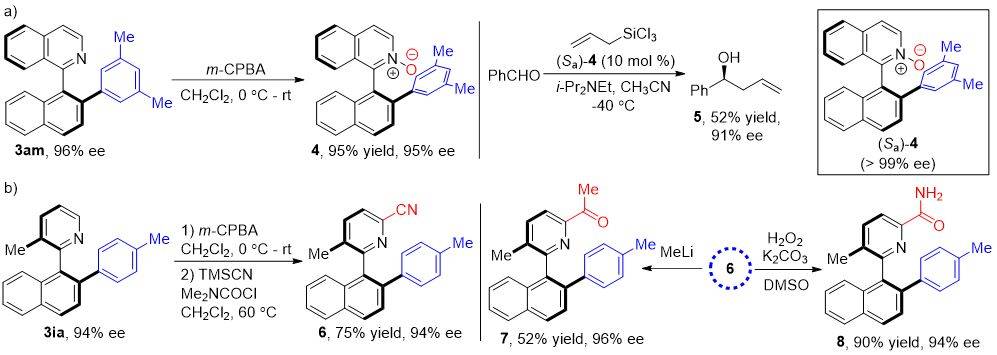
为了证明该方法学的应用价值,随后作者对轴手性联芳基产物进行了进一步的转化。例如,经氧化得到的手性吡啶氮氧化物 4 可以作为手性路易斯碱催化剂应用于醛的不对称烯丙基化反应中,反应得到了不错的对映选择性控制。另外轴手性吡啶化合物 3ia 可以在吡啶邻位进一步引入其他官能团(氰基、乙酰基等),为合成手性吡啶类催化剂提供了可能。
总结与展望
该工作为轴手性吡啶类化合物的合成提供一个高效的方法,为后续手性吡啶类化合物在催化剂和配体方面的应用提供了很好的合成工具。当然,这个工作也有一些遗憾,目前催化剂的用量还比较高,希望后续能够发展出更加高效、温和、实用的催化体系,快速获得结构多样的轴手性联芳基化合物。
文章链接:
https://pubs.acs.org/doi/10.1021/jacs.9b03862
来源:rationalscience 研之成理
原文链接:http://mp.weixin.qq.com/s?__biz=MzIwMzE5MzQ1NQ==&mid=2649327507&idx=3&sn=ba4134242a7d7c6eda1add7c966131bc&chksm=8ece0a93b9b98385333663b86b174f725418b11b1624eda29435927d6c49de3ba22495fccb02&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



