来源:BioArt
迄今为止已有超过10000种单基因突变被证实与人类疾病密切相关,其中大多数的单基因突变是可以遗传给后代的,被称为单基因遗传病,它符合孟德尔遗传规律,因而也通常会引起家族性疾病。单基因突变的遗传模式主要有五种,包括常染色体隐性遗传、常染色体显性遗传、X连锁显性遗传、X连锁隐性遗传和线粒体突变的母系遗传。近些年来,单基因遗传病的种类与日俱增,已经对人类健康构成了较大的威胁,因此寻找预防致病基因从亲代遗传到子代的新方法越来越受到科学家们的重视,基因治疗便应运而生,脱颖而出。基因治疗是通过一定的方式,将野生型基因或有治疗作用的DNA序列导入人体靶细胞来纠正或改善人类的遗传缺陷的方法,目前临床上批准的基因治疗只限于体细胞基因治疗,但是不容忽视的是,体细胞基因治疗存在以下缺陷:首先,由于大多数致病基因的突变一旦遗传给后代,就会导致组织或器官的不可逆损伤而引起疾病,在这些情况下,体细胞基因治疗不足以逆转疾病的病理状态,除非其实施是在疾病发生之前;其次,考虑到体细胞基因治疗的靶标是实体组织或器官的数以亿计的细胞,其效率依旧存在疑问;最后也是最重要的一点,体细胞基因治疗并不改变生殖细胞内缺陷基因的存在,其依旧可以遗传给后代。
基于体细胞基因治疗的这些缺陷,生殖细胞基因治疗越来越受到研究者们的关注,所谓生殖细胞基因治疗(germline gene therapy,GGT)即针对可再生细胞如干细胞和生殖细胞或者早期胚胎的基因治疗,尽管GGT在伦理上受到很多非议,但是不容否认,其可以及时纠正发育早期存在于少数胚胎细胞中的疾病相关突变并阻止致病突变遗传至后代。同时,考虑到大多数遗传疾病分子诊断技术的急剧发展以及在生殖细胞中纠正错误基因的技术发展【1】,切实探究GGT的临床治疗可能性仍旧是极其重要的。
2019年6月4日,来自美国俄勒冈健康与科学大学的Don P. Wolf教授、Paul A. Mitalipov教授以及Shoukhrat M. Mitalipov教授共同在Nature Medicine上发表题为Principles of and strategies for germline gene therapy的文章,详细探讨了最近利用内源性DNA修复机制进行生殖细胞基因治疗的策略和原则,为安全高效的GGT提供了新方向,也为阻止有害突变基因的遗传提供了新的指向。

目前临床上运用的较广泛的阻止生殖细胞突变基因遗传的方法主要有两个,其一是在孕早期通过羊水穿刺或绒毛取样进行产前诊断,再由父母做出终止妊娠或是生下有缺陷婴儿的艰难选择;其二是胚胎移植前基因诊断(PGD),进而选择不携带突变的胚胎进行移植,但是体外受精导致的胚胎发育不良、异倍体的存在以及胚胎移植率低等原因将导致该方法的成功率降低,特别是当父母有一方是纯合子常染色体显性突变或双方均是纯合子常染色体隐性突变时该方法将不适用(图1)。而与这两类基于选择的方法不同,配体或移植前胚胎的基因修复将挽救大多数突变胚胎,增加可移植胚胎的数量,从而避免了对一个小生命的弃置,这也是GGT为何被一些家庭所接受的主要原因。
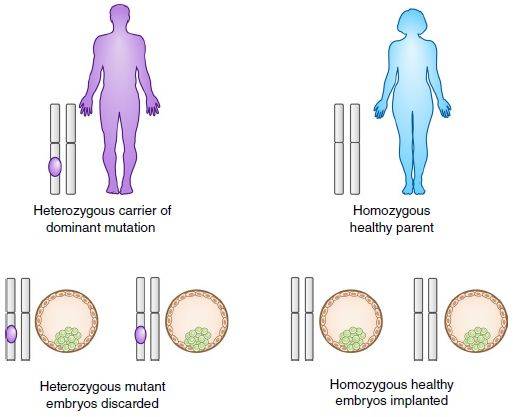
图1 PGD胚胎选择模式(父母一方携带杂合子常染色体显性突变)
传统体细胞基因治疗的方法主要有两个,其一是运用病毒载体将一个正常基因的合成拷贝插入到基因组的非特定位置,而不只是基因的突变内源性拷贝 (或多个拷贝) ,出于安全性和有效性考虑,这种方法并不适用于GGT,同时因为这种方法会导致人类基因组的基因修饰,在伦理上也是不适合GGT的;另一种则是是利用基因编辑如CRISPR-Cas9技术改变突变的有害基因,但是其主要的局限性在于在数千种产生额外的新生突变的致病生殖细胞突变中,只有一小部分可以被治愈,这也依旧不能满足GGT对于高效的需求。鉴于此,本文作者从三个方面阐释了目前GGT的有效治疗策略。
1. 线粒体DNA(mtDNA)突变治疗策略。
由于线粒体基因组缺乏天然的DNA修复和重组机制,基因编辑产生的直接DNA改变对其是没有作用的,而GGT中的一种方法即线粒体替代治疗(mitochondrial replacement therapy , MRT)通过用捐赠者的未突变mtDNA替代突变携带者卵母细胞中的突变mtDNA,从而实现安全地抑制有害的线粒体基因突变从母体转移给婴儿。值得注意的是,MRT过程中仍会有一小部分(1-4%)的母系突变mtDNA残留在卵母细胞或是胚胎中,虽然这些微量突变不足以致病,但是,在胚胎移植后期和胎儿发育过程中其选择性扩增和快速逆转为同质母体mtDNA仍是潜在的安全隐患。
2. 杂合子突变治疗策略
传统的基因编辑技术可以高效诱导特定位点的DNA双链断裂(DSB),继而通过非同源末端接合(NHEJ)和同源重组修复(HDR)机制被修复。研究表明,NHEJ易于出错,从而频繁在DSB位点引入插入缺失突变【2】,与之相反,HDR能确保相对精确的DSB修复而不增加或减少DNA序列,但是其修复效率仅占1-5%,这并不能满足GGT对于严格的安全和高效的需求。由此基因转换应运而生。基因转换是将供体序列单向转换至高度同源的受体序列中而不需要外源模板的过程,基因转换发生在减数分裂非交叉重组时期,被DSB修复机制激活,进而导致完整的同源序列复制到DSB区域,已有研究表明CRISPR-Cas9诱导的突变基因MYBPC3的基因转换修复效率达到64%,从而导致纯合的野生型MYBPC3胚胎的高产出率(图2)。
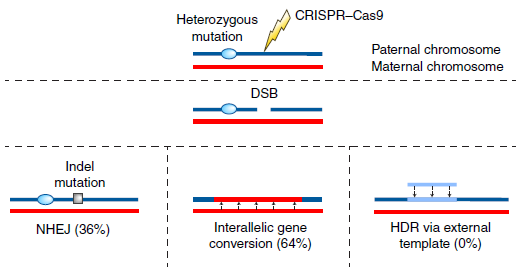
图3 生殖细胞中MYBPC3杂合子突变修复
3. 核苷酸替换和纯合子突变治疗策略
单碱基编辑可以实现单个核苷酸的替换,既可以用于杂合子核苷酸替换,也可以用于纯合子突变修复,相比于传统的基因编辑其最大的优势在于单碱基编辑并不诱导DSB产生,因而避免了NHEJ过程,减少了插入缺失突变的产生,同时也不需要基于模板的HDR修复,从而提高了修复效率。但是现存的单碱基编辑技术存在明显的脱靶现象,同时它限制于单核苷酸替换突变以及相对较新的运用也意味着目前阶段单碱基编辑技术应用的局限性。此外,作者也提出针对纯合子突变的治疗,需要寻找新的治疗方法,例如增加HDR的发生率。
基于以上生殖细胞基因治疗策略,在实现高治疗效率的同时,本文作者提出,GGT还必须坚持两点原则。
首先是安全性问题。基因编辑的脱靶效应以及不合需要的在靶突变都是重要的安全考量问题,必须结合移植前或产前活体检查和诊断以确定精准的在靶修复。与此同时,GGT过程中一个普遍存在的问题就是生物嵌合现象——在胚胎或后代中同时存在着修复和未被修复的细胞,这也使得PGD的筛选变得更加复杂,可喜的是,已有研究证实,减少生物嵌合现象的方法包括缩短Cas9蛋白的半衰期、在受精卵早期引入CRISPR-Cas9或者在卵母细胞M期注射CRISPR-Cas,当然也可以通过增加基因转换的效率并减少NHEJ修复来减少生物镶嵌现象。
第二个重要原则就是伦理监督。长久以来,世界范围内多个组织围绕着人类GGT临床应用的伦理审查问题争论不休,但是一致的意见是,在适当的监管和同意下,人类胚胎移植前的GGT研究是必须进行的,只有正确评估其安全性、可行性和有效性,才有可能为未来的临床应用建立高标准。
未来的路还很长,在严格遵守生殖细胞基因治疗原则的基础上,还需要更多的工作确保更精准有效的治疗策略,GGT应用于临床任重而道远!
原文链接:
https://www.nature.com/articles/s41591-019-0473-8
参考文献
1. Cornu, T. I., Mussolino, C. & Cathomen, T. Refining strategies to translate genome editing to the clinic. Nat. Med. 23, 415–423 (2017).
2. Spies, M. & Fishel, R. Mismatch repair during homologous and homeologous recombination. Cold Spring Harb. Perspect. Biol. 7, a022657 (2015).
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652470775&idx=4&sn=440508333ba02190e24ebb551d2e68da&chksm=84e2ee43b3956755ee7771f8b1be341185271d7475396232cf84a421b6735c429dd03c2b0be5&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn