来源:BioWorld
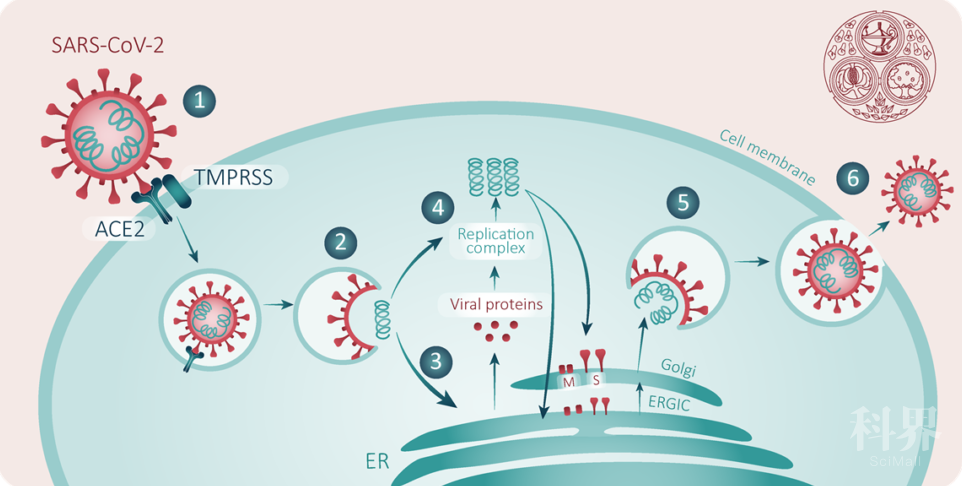
SARS-CoV-2使用其Spike蛋白受体结合域(S-RBD)与宿主细胞受体血管紧张素转化酶2(ACE2)结合,这是其感染人类细胞的最关键步骤。
7月29日,国际顶尖学术期刊 Nature 提前上线了一篇新冠肺炎疫苗的研究论文。
四川大学华西医院魏霞蔚、逯光文及澳门科技大学张康作为共同通讯作者,开发了一款重组蛋白候选新冠疫苗。该疫苗已在鼠、兔以及非人灵长类动物中证实能够强烈诱导针对新冠病毒的保护性免疫应答和中和性抗体的产生。

该研究团队庞大,由四川大学华西医院、中国医学科学院北京协和医学院、国家食品药品监督管理局、同济大学、中国人民解放军总医院第五医院、香港理工大学、成都电子科技大学、澳门科技大学、清华大学等单位合作完成,研究团队中还包括魏于全院士、王福生院士等。
为尽量减少潜在副作用,研究团队找到了新冠病毒Spike蛋白受体结合域(S-RBD)中319-545的氨基酸序列,实验结果表明,包含S-RBD氨基酸残基319-545的重组疫苗可在免疫小鼠、兔和非人灵长类动物(猕猴)中,仅接受一次疫苗注射,在7天或14天即可诱导有效的功能性抗体反应。
注射疫苗免疫后动物的血清可以阻断了新冠病毒RBD与细胞表面表达的ACE2受体的结合,并在体外中和SARS-CoV-2假病毒和SARS-CoV-2活病毒的感染。
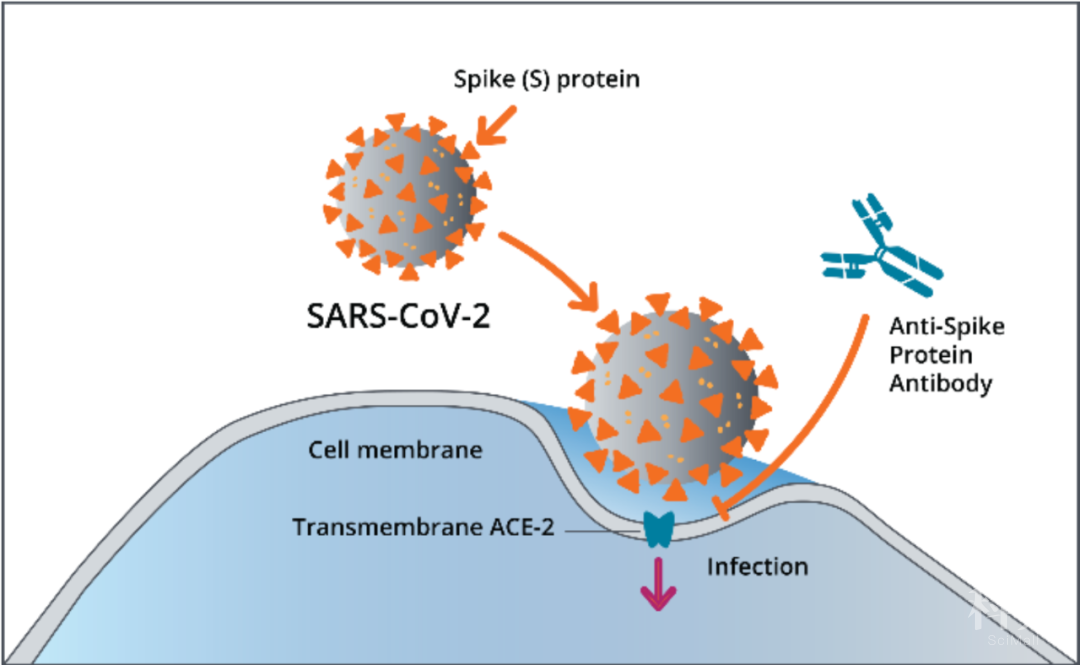
更重要的是,该重组疫苗还为非人类灵长类动物提供了体内SARS-CoV-2攻击的保护。
之前的研究在COVID-19患者的血清中也发现了升高的RBD特异性抗体。几种免疫途径和CD4 T淋巴细胞与疫苗抗体反应的诱导有关。
这些发现突出了RBD结构域在SARS-CoV-2疫苗设计中的重要性,并通过诱导针对RBD结构域的抗体为保护性疫苗的开发提供了依据。
来源:ibioworld BioWorld
原文链接:https://mp.weixin.qq.com/s?__biz=MzU1MzMxMzcyMg==&mid=2247505209&idx=4&sn=e5a8aad19b4805c64a4ec57705a4566f&chksm=fbf621eccc81a8fa56c9c4d5f8b2d86979dea0afd2879341df384ed30b9684de292bc050408f#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn

