来源:BioArt
大脑突触重塑在整个生命中不断发生,包括海马体在内的区域会根据经验发生突触重塑,对学习和记忆巩固非常关键。深入了解神经环路中突触重塑的影响因素,对于理解经验如何在大脑中稳定编码至关重要。而在多种影响因素中,固有免疫系统在调控突触形成中的作用不断显现。小胶质细胞是大脑中分布最为丰富的免疫细胞。研究报道发现小胶质参与到突触重塑过程中。小胶质细胞与树突棘接触,会在丘脑发育早期和海马区吞噬突触成分【1】。小胶质细胞也可以依赖经验获得促进突触小棘形成。2020年2月7日,浙江大学医学院谷岩研究员课题组和王朗副研究员课题组合作首次发现用于免疫的小胶质细胞通过清除突触而引起记忆遗忘,并且进一步发现补体信号通路参与了小胶质细胞介导的遗忘,并且依赖于记忆印迹细胞的活动(Science | 谷岩/王朗团队揭示大脑中的免疫细胞竟是记忆遗忘的“主谋”)【2】。然而神经元和小胶质细胞之间的相互作用介导的突触重塑稳定性变化的机制尚不清楚。小胶质细胞调控突触变化的分子机制研究还处于起步阶段。
近日,来自UCSF的Anna V. Molofsky团队在Cell上发表了题为Microglial Remodeling of the Extracellular Matrix Promotes Synapse Plasticity的文章。该研究发现成年海马神经元以经验依赖的方式表达IL-33,作用于小胶质细胞上IL-33受体,促进受损的细胞外基质(Extracellular Matrix ECM)的吞噬。

该研究团队在2018年在Science上发表的一项研究表明IL-33调控小胶质细胞的活性和功能。研究发现出生后早期,丘脑和脊髓中星形胶质细胞表达的IL-33会促进小胶质细胞吞噬突触,限制突触数量【3】。团队首先探索了成年小鼠大脑中IL-33的表达部位。利用Il33mCherry/+报告基因小鼠,作者发现与发育中的大脑不同,成年小鼠大脑中表达IL-33的大多为海马中的神经元。
IL-33有两个亚型IL-33a和IL-33b,受不同启动子调控。作者发现神经元主要表达IL-33b而星形胶质细胞产生IL-33a。利用条件性敲除工具鼠neuron-specific Syn1Cre可以敲除神经元中IL-33的表达,并且通过IL-33免疫染色作者验证了IL-33表达神经元更细致的分布情况,以齿状回区域最为丰富。
作者接下来利用三个月年龄的报告基因小鼠,分别饲养在enriched environment (EE) 和 social isolation (SI)环境中四周后发现SI环境降低海马神经元中IL-33表达,EE可以增加IL-33表达。
作者观察到齿状回神经元表达IL-33的水平存在异质性,于是作者利用单核RNA测序(single-nucleus RNA sequencing)分析了海马神经元异质性与功能的相关性。作者发现齿状回神经元被分为两个亚类。利用流式分选出Il33mCherry/+神经元,分析发现与其中一个亚型重叠,这个亚型中与细胞粘附、突触组装和可塑性基因富集。作者发现与组装和重塑细胞外基质的18种相关基因也在此类神经元中富集。总结来讲IL-33表达的神经元中突触形成和ECM重塑相关基因富集。进一步分析发现IL-33的水平与树突棘的密度呈正相关。
为了确定IL-33的靶向细胞,于是作者量化IL1RL1(也叫ST2,IL-33受体),发现海马中小胶质细胞是主要的表达细胞,流式分选qPCR和定量原位杂交也证实了这些结果。神经元缺失了IL-33和小胶质细胞缺失IL1RL1会导致树突棘密度降低。利用全细胞膜片钳分析发现IL-33 cKO的小鼠中兴奋性突触后电流频率降低,这与树突棘密度降低一致。利用慢病毒将IL-33递送至齿状回也足以促进树突棘的形成。
齿状回新生神经元的整合需要神经回路重塑,并且在EE环境中增加。作者探讨了IL-33在这一过程中的作用发现,IL-33 cKO小鼠新生时,神经元数量无明显变化,但是在EE中饲养五周,与对照组相比,新生神经元明显减少,树突棘密度降低,突触整合受损。这表明新生神经元的经验依赖性增加需要神经元来源的IL-33。自然而然作者接下来检测了IL-33是否参与到海马依赖的记忆环路调控。作者发现IL-33 cKO的小鼠具有完整的记忆唤起和情景分辨力。但在14到28天之间,与对照组相比,cKO小鼠的情景分辨能力逐渐下降。这表明神经元来源的IL-33通过远时间点可以提高海马内存精度。之后作者发现在老年小鼠的海马中IL-33表达下降,记忆精度和突触棘可塑性下降。神经元中IL-33释放增加可以改善大脑中衰老相关结构和功能改善。
为了寻找相关机制,作者对IL-33处理四小时后的海马小胶质细胞转录谱特征进行了分析。IL-33处理后,小胶质细胞的IL-1β、TNF和多种趋化因子得到激活。在上调的基因中,A类清道夫受体Marco以及衔接蛋白Gas7(巨噬细胞吞噬所必需)上升明显。这些与IL-33在促进小胶质细胞吞噬作用一致。分析发现IL-33处理后,差异表达的76种基因与ECM相关,多种ECM蛋白酶上调明显,其中Adamts4和Mmp14编码的膜定位金属蛋白酶,主要用于裂解硫酸软骨素蛋白聚糖(chondroitin sulfate proteoglycans CSPGs),这是大脑中ECM蛋白的主要成分。
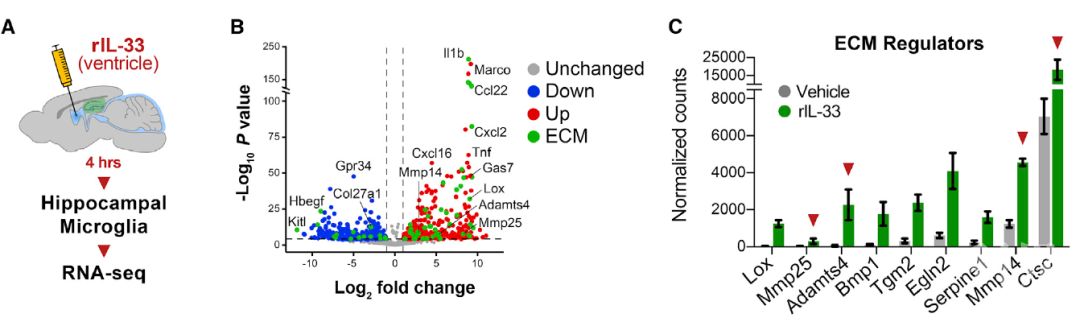
IL-33处理四小时后的海马小胶质细胞转录谱特征
Aggrecan是神经元周围富集的CSPG, 在齿状回分布明显。免疫染色发现Aggrecan定位于小胶质细胞CD68+溶酶体中。在IL-33cKO小鼠小胶质细胞的CD68+溶酶体数量减少,Aggrecan吞噬量减少了54%。体内观察到IL-33缺乏会导致突触周围ECM积累,树突棘密度降低。表明IL-33作用的小胶质细胞是ECM清除和突触重塑的重要调节细胞。
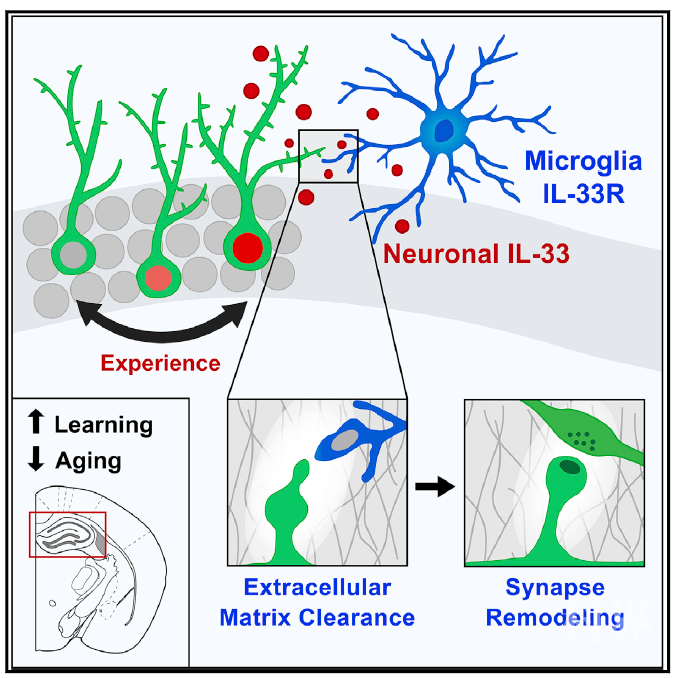
该研究定义了IL-33介导的小胶质细胞促进稳定突触重塑的细胞机制,证明了神经元来源的IL-33驱动小胶质细胞吞噬ECM,导致突触可塑性增加。阿尔茨海默病模型中发现ECM的清除和外源性IL-33的补充有助于疾病治疗,这也表明揭示调节大脑小胶质细胞调控突触功能的分子机制有助于开发认知修复的新策略。还有多个问题亟待回答:尚需更加精细地,单个神经元水平上研究IL-33的表达特性,以及IL-33神经元释放的分子机制;以及小胶质细胞对于髓鞘和其他重要成分之间的关系。
来源:BioGossip BioArt
原文链接:https://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652493099&idx=6&sn=55f82115d3fddea72a19454c487d86bb&chksm=84e2469fb395cf892bbd992f69a6cb49da27c4791e6731adaccbcac673ecf948b453821461bf#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



