来源:X一MOL资讯
酶因其高效专一的催化特性在医药、食品、轻工等领域具有广阔的应用前景。酶制剂的制备,是酶实现产业化应用的必由之路。然而,传统方法在其制备过程中为实现稳定化或功能化常引入各类添加剂,导致制备复杂化、操作性降低,以及相关纯度和活性问题。另一方面,酶在催化过程中常需要激活剂参与激活。直接在反应体系中添加激活剂,由于其与酶的接触效率较低,加入量较大而利用效率低,造成成本上升。如何解决上述问题,在高效利用激活剂的同时实现酶稳定化,高效制备高性能酶制剂,是该领域的关键挑战。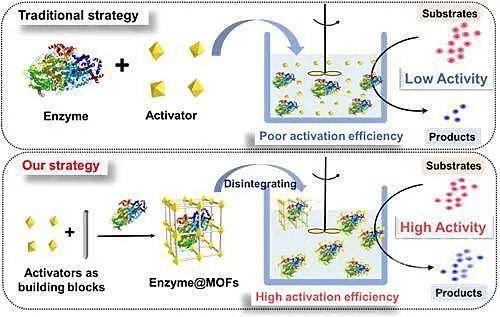
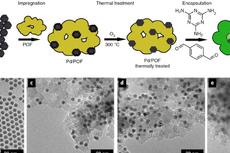
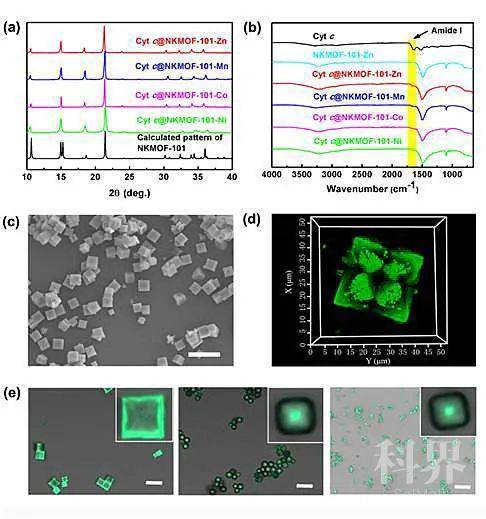
近日,南开大学药物化学生物学国家重点实验室陈瑶研究员团队取得了重要研究进展,将金属激活剂与酶通过原位共组装创制了新一代晶态酶制剂平台。作者利用金属激活剂(Mn2+、Co2+、Zn2+、Ni2+)、方酸配体与酶,在室温水相中自组装形成固体晶态的酶@MOFs复合物。通过粉末衍射、红外及激光共聚焦显微镜等技术手段证实该组装过程将酶成功负载到MOF中。酶在NKMOF-101-Zn中呈现有趣的花式分布(图2)。其中MOFs在酶周围形成了含有金属激活剂的规则保护层,分布在酶周围。MOFs的良好溶解性使其在酶催化过程中充当“崩解剂”,其中的金属激活剂在与酶的共释放过程中得以充分接触而高效激活酶分子。结果表明,该新型酶制剂对酶活的促进作用高达151%。同样条件下,直接向酶催化体系中加入相同量金属激活剂、配体或MOFs,未发现明显激活效果。此外,MOFs保护层的保护力使酶的耐热性、有机溶剂稳定性等均有显著提高(图3)。
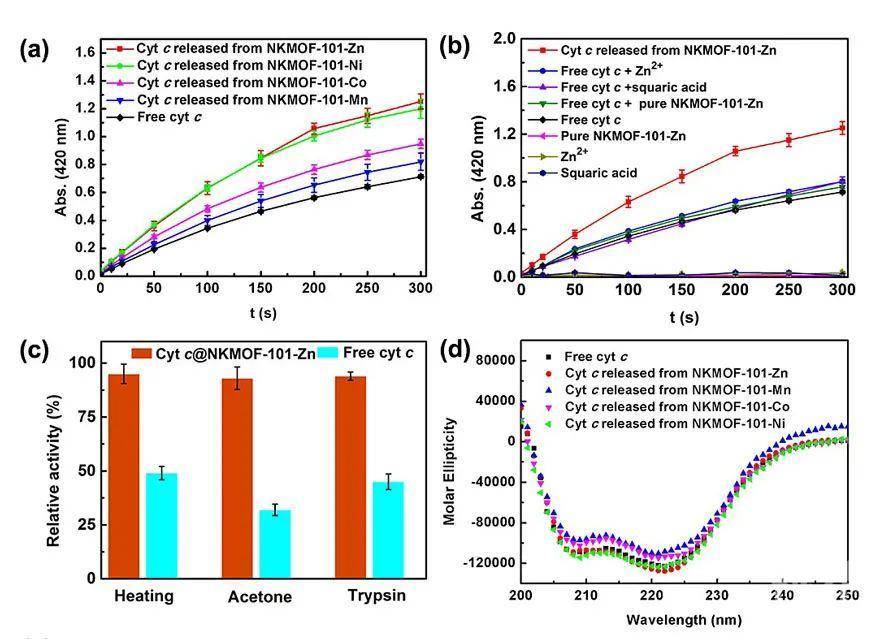
进一步的机理研究表明,由于酶包覆在MOFs中的邻近效应,MOFs在共释放激活剂和酶分子的过程中,充当了“离子泵”的作用,为酶提供金属激活剂,并使其充分接触而高效地激活酶分子。此外,不同金属激活剂构建的多种酶@MOFs所表现出的酶活促进和稳定化效果也各不相同,这将有望针对不同酶分子实现定制化高性能酶制剂的创制,用于酶的便捷储运和使用。
该酶制剂策略在实现激活剂对酶的精准高效激活的同时,实现了对酶的稳定化,大大提高了酶制剂的催化效率和可操作性,且无需额外添加助剂。这种新型晶态酶制剂平台具有普适性和可定制化等特点,已申请专利保护。这一成果近期发表在Angewandte Chemie International Edition 上。论文唯一通讯作者是南开大学陈瑶研究员,第一作者是南开大学博士研究生安红德。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657642189&idx=7&sn=8d985b408be8f74b46a8b24a15eb107d&chksm=80f84f1db78fc60be0ccf6a2184a976c58b8d91e3ffdc16b242bbe7398c9782b6b3444f67036&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn