来源:X一MOL资讯
英文原题:Rationally Designed Polymer Conjugate for Tumor-Specific Amplification of Oxidative Stress and Boosting Antitumor Immunity
通讯作者:宋万通,中国科学院长春应用化学研究所
作者:Sheng Ma(马胜),Wantong Song (宋万通)*,Yudi Xu(徐玉迪),Xinghui Si(司星辉),Shixian Lv(吕世贤),Zhaohui Tang(汤朝晖),Xuesi Chen(陈学思)*
生物可降解高分子材料因其优异的生物相容性、良好的生物可降解性和制备的可控性在肿瘤治疗中展现出广阔的应用前景。将高分子材料用于抗肿瘤药物的传输与缓控释在过去的二十几年间经历了巨大的发展。通常这些高分子材料不具备治疗活性,而仅仅作为载体来传输活性药物以获得治疗效果。但是,作为高分子材料本身,通过合理的设计在其中引入一些功能性构筑基元,可以制备一些功能性高分子载体,突破原有载体材料功能惰性而仅作为载体或辅料存在的设计理念。这样的功能性高分子载体材料本身就可以具备抗肿瘤效果;而当用于药物担载时,亦可能与药物起到协同增效而大大提升药物的治疗效果。
基于这样的理念,中国科学院长春应用化学研究所陈学思院士团队通过功能性分子基元的模块化组合,设计合成了一种含有肿瘤特异性协同增强氧化应激功能模块的长循环高分子共轭物(TSEOP)。TSEOP的自组装纳米胶束在系统注射后,富集到肿瘤组织,在肿瘤细胞的内源性刺激下,产生肉桂醛(CA)和醌甲基化合物(QM),分别作为活性氧(ROS)产生器和谷胱甘肽(GSH)的消除器,协同增强肿瘤细胞内的氧化应激,在直接杀伤肿瘤细胞的同时诱导肿瘤细胞的免疫原性,激活肿瘤细胞特异性抗肿瘤免疫响应。由于利用了肿瘤细胞与正常细胞的生理特征差异,该TSEOP共轭物具有肿瘤细胞特异性,并不会对正常细胞造成明显的伤害(图1)。

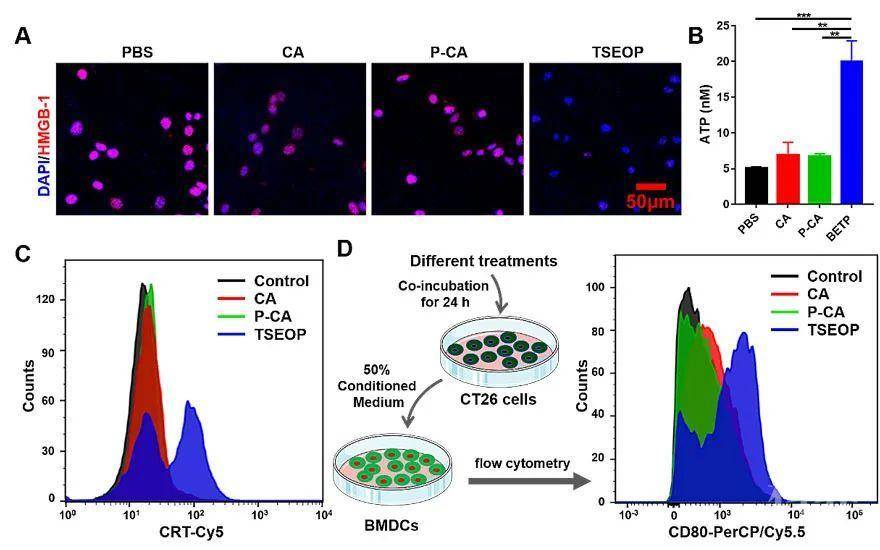
在体外实验中, TSEOP诱导CT26肿瘤细胞产生大量的ROS,导致肿瘤细胞发生凋亡。不仅如此,TSEOP治疗增强了肿瘤的免疫原性:CT26肿瘤细胞表面钙网蛋白(CRT)阳性细胞比例增加,细胞内高迁移率族蛋白B1(HMGB1)和ATP大量释放。当用TSEOP处理的肿瘤细胞上清孵育小鼠骨髓来源树突状细胞(BMDCs)时,BMDCs中CD80阳性的比例明显升高,表明TSEOP在杀伤肿瘤细胞的同时可以刺激抗原提呈细胞的活化(图2)。
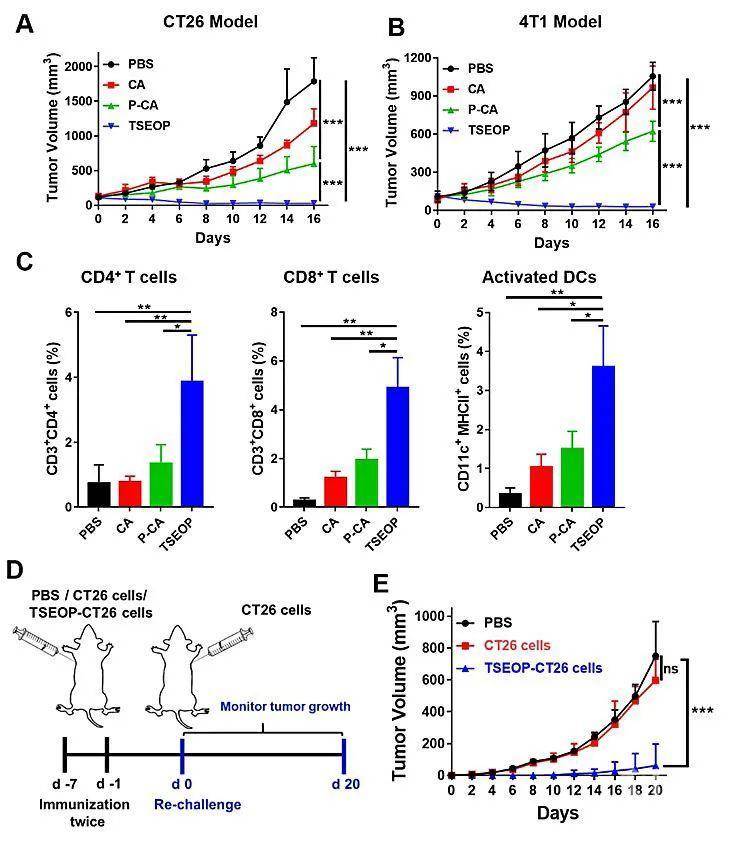
在对CT26和4T1皮下肿瘤模型的治疗实验中,单独使用TSEOP治疗都取得了100%的肿瘤抑制率,实现了肿瘤的治愈,并且TSEOP的治疗组小鼠肿瘤组织存在显著增加的CD4+和CD8+ T细胞,表明TSEOP治疗可以有效地激活获得性免疫。进一步,利用TSEOP处理的CT26肿瘤细胞进行小鼠的疫苗接种和再挑战实验,BALB/c小鼠在接受两次经TSEOP预处理的CT26细胞(TSEOP-CT26细胞)的皮下免疫后,再次种植CT26细胞,6只小鼠中有4只并没有形成肿瘤。相比之下,接受PBS或者未经处理的CT26细胞对小鼠进行皮下免疫则没有影响肿瘤的生长(图3)。以上结果表明,TSEOP的治疗能激活肿瘤特异性的抗肿瘤免疫响应,抑制肿瘤的生长和复发。
以上研究结果近期发表在Nano Letters 上,中科院长春应化所博士生马胜为论文的第一作者,宋万通副研究员和陈学思院士为论文的共同通讯作者。


来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657632874&idx=2&sn=921e6acea211e88576e3a62b420ab483&chksm=80f86bbab78fe2ac1227797544e2c7521ae973a8b5a034862a080e67342fba198f8c8b091a14&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



