来源:中国高科技
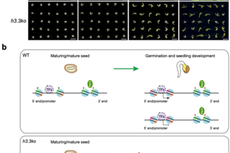
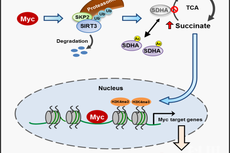
癌基因cMyc是一个重要的转录因子,调控约15%的人类基因表达,在肿瘤细胞的增殖、凋亡以及代谢重编程等方面发挥重要作用。然而,目前尚不清楚,cMyc是否通过转录以外的机制,来广泛地调控基因的表达以及肿瘤的发生发展。中国科学院科学家团队——中科大教授张华凤课题组、高平课题组联合军事医学科学院段小涛课题组研究发现,cMyc能够促使琥珀酸脱氢复合酶(SDH complex)中的重要亚基SDHA乙酰化以及SDH复合酶失活,导致底物琥珀酸(succinate)的积累,进而上调组蛋白H3K4的三甲基化(H3K4Me3)水平以及基因的表达。
机制方面,发现cMyc通过泛素连接酶SKP2促进线粒体中SIRT3的蛋白降解,从而导致SDHA的乙酰化上升。通过质谱进一步鉴定出SDHA受调控的乙酰化位点K335,小鼠实验显示SDHA的K335位点乙酰化在cMyc诱导肿瘤过程中起重要作用。
进一步分析临床病人弥散性大B细胞瘤(DLBCL)样本发现,高表达cMyc的DLBCLs中,SIRT3发挥着抑癌因子的功能,而K335位乙酰化的SDHA发挥着促进肿瘤的作用。这一发现揭示了cMyc驱动的肿瘤发生过程中SDHA乙酰化修饰发挥的重要病理学作用。
SDHA被认为是抑癌蛋白,它的失活突变体与多种肿瘤,例如副神经结瘤、乳腺癌、肾癌等,有一定程度的联系。这项研究表明,至少在弥散性大B细胞淋巴瘤中,SDHA通过乙酰化失活而极大地促进了cMyc异常表达的肿瘤的进展。因此,靶向SDHA的乙酰化将可能为此类肿瘤的临床治疗提供潜在的策略和手段。
该论文以Myc-mediated SDHA acetylation triggers epigenetic regulation of gene expression and tumorigenesis 为题,3月16日在线发表于Nature Metabolism 期刊。中国科大生命学院博士李世庭和黄的为该论文的共同第一作者,张华凤、高平和段小涛为论文的共同通讯作者。这项工作得到安徽医科大学蔡永萍课题组、军事医学科学院李爱玲课题组、中国科大周荣斌课题组和瞿昆课题组的大力帮助。
(来源:中国科学院)
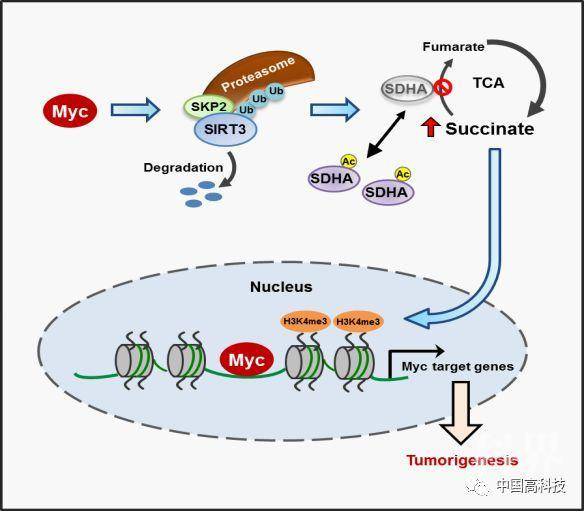
(来源:中国科学院)
来源:cas-hitech 中国高科技
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MDczMTAzMA==&mid=2650048774&idx=1&sn=210f8150cbe26d7fc7b0202e845931e2&chksm=87387d7fb04ff46926f16ee37714eb857b69005527f8fbd4b0cfef5475b0b2db9070f1f4f571&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn