哺乳动物生物钟调节着睡眠-觉醒循环、内分泌、物质能量代谢等多种生理功能,对于生物适应环境具有重要意义。2017年,北京生命科学研究所/清华大学生物医学交叉研究院张二荃实验室发现哺乳动物生物钟与低氧信号通路存在相互调控作用,并揭示其在基因组水平互作的机制。然而,对于生物钟与低氧信号互作的具体生化机制以及该互作在生物演化上的意义仍有待进一步研究。
5月17日,中国科学院西北高原生物研究所小哺乳动物适应性进化与管理学科组张堰铭实验室与北京生命科学研究所/清华大学生物医学交叉研究院张二荃实验室、蔡涛实验室合作,在Cell Reports上发表了题为A Highland-adaptation Mutation of the Epas1 Protein Increases Its Stability and Disrupts the Circadian Clock in the Plateau Pika的研究论文。该研究揭示了低氧诱导因子Epas1的稳定性影响高原鼠兔昼夜节律生物钟的分子机制。
高原鼠兔(Ochotona curzoniae, 图1)生活在青藏高原及其相邻地区海拔3000–5000米的高山草甸和高山草原上,是青藏高原数量最多的哺乳动物,对维持青藏高原生态平衡意义重大。高原鼠兔常年生活在低温、低氧的极端环境中,是研究低氧适应的理想动物模型。该研究中,研究人员首先通过监测高原鼠兔的体温与活动,发现饲养于高原环境的高原鼠兔的体温与行为的昼夜节律较弱甚至没有节律;其细胞和分子层面的生物钟同样具有振幅低、节律紊乱的特点(图2A–C)。
哺乳动物昼夜节律生物钟的核心振荡器是由转录激活因子Clock/Bmal1和转录抑制因子Per/Cry构成的转录翻译反馈回路(Transcription-translation feedback loop,TTFL)。研究人员通过荧光素酶报告基因实验发现高原鼠兔的Clock、Bmal1、Cry1/Cry2具有正常的转录激活/抑制功能,且向小鼠Per2-/-成纤维细胞回补高原鼠兔的Per2可以重建稳定的生物节律(图2D–E),说明高原鼠兔核心生物钟基因的自身功能并无异常。
考虑到高原鼠兔长期生活在低氧的条件下,而低氧信号通路又与生物钟息息相关,研究人员分析了高原鼠兔与平原地区哺乳动物(如家兔、大鼠、小鼠、人等)缺氧诱导因子(HIF)家族蛋白编码基因的序列,发现高原鼠兔Epas1基因(编码Epas1蛋白,又称HIF-2α )第14个内含子5’端存在一个特异的G>A的点突变。RT-PCR结果表明,该突变会改变Epas1 mRNA的剪接方式,产生增加了72个碱基的转录本以及增加了24个氨基酸的蛋白(下称L-Epas1,未突变的蛋白称为S-Epas1)。这一突变在弱节律的高原鼠兔中以杂合形式存在,在无节律的个体中则以纯合形式存在。全局蛋白质稳定性(Global protein stability, GPS)分析表明,与S-Epas1相比,L-Epas1蛋白在缺氧条件下更稳定。此外,向家兔、大鼠、小鼠的Epas1蛋白中插入相同的24个氨基酸片段也会提高蛋白质的稳定性(图3)。
为研究Epas1蛋白对生物钟的影响,研究人员在高原鼠兔细胞中敲低Epas1的表达,发现在无节律的高原鼠兔细胞中敲低Epas1基因可有效恢复细胞的节律性,说明Epas1在破坏高原鼠兔节律中起到关键作用。荧光素酶报告基因实验和凝胶阻滞或电泳迁移率变动实验(Electrophoretic mobility shift assay,EMSA)表明,Epas1可以和核心生物钟蛋白Bmal1形成异源二聚体并结合在生物钟基因的E-box元件上促进基因的转录,但Epas1-Bmal1的转录激活活性远低于Clock-Bmal1。在平原哺乳动物中,Epas1的稳定性较低,在常氧条件下降解速率快;在高原鼠兔中,由于24个氨基酸的插入,Epas1的稳定性提升,因此可以与核心生物钟蛋白Bmal1相互作用并干扰生物节律。
为探究上述结论是否适用于在体情况,研究人员使用CRISPR/Cas9构建了敲入高原鼠兔L-Epas1基因的C57小鼠。将敲入高原鼠兔L-Epas1基因的小鼠的视交叉上核(Suprachiasmatic nucleus,SCN,哺乳动物生物钟中枢)进行体外培养,发现敲入高原鼠兔L-Epas1基因使SCN的生物节律对缺氧胁迫更加敏感。通过注射AAV病毒使小鼠在SCN特异性表达高原鼠兔L-Epas1可以使小鼠在低氧环境下体温节律的稳定性下降(图4A),进一步证明了Epas1稳定性增加会导致生物节律紊乱。将敲入高原鼠兔L-Epas1的C57小鼠在低氧环境中饲养一个月后,研究发现与敲入了大鼠Epas1或未做敲入的C57小鼠相比,敲入高原鼠兔L-Epas1的C57小鼠面对低氧胁迫时体重下降减少、血液中血红素含量水平较低、无明显的心室肥大(图4B–C)。上述结果说明,突变的Epas1蛋白虽然会导致生物节律紊乱,但减少了低氧环境下心脏的损伤程度,或可解释L-Epas1在演化过程中被保留的原因。

图1.高原鼠兔
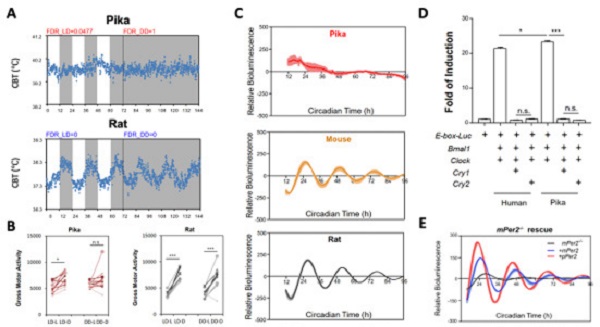
图2.高原鼠兔的体温、活动和离体细胞均无明显节律,但是其核心生物钟基因功能正常
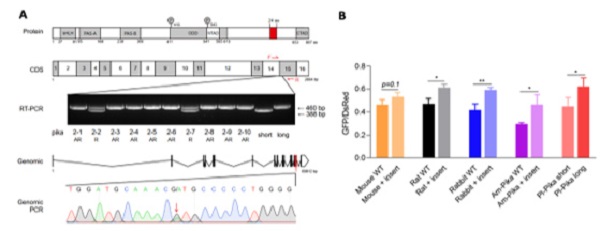
图3.A.高原鼠兔Epas1基因多态性;B.24aa的插入导致Epas1蛋白稳定性增加
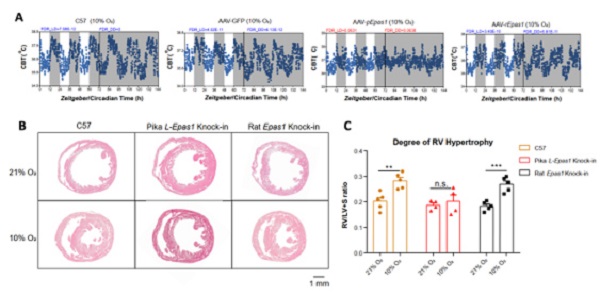
图4.A.SCN过表达高原鼠兔Epas1的小鼠体温节律性变差;B-C.高原鼠兔的Epas1可以降低低氧环境对心脏的损伤

