来源:中科院之声
中国科学院上海药物研究所研究员徐华强团队与山东大学教授孙金鹏团队、浙江大学教授张岩团队等首次解析了糖皮质激素与其膜受体GPR97和Go蛋白复合物的冷冻电镜结构,这也是国际上首次解析的黏附类GPCR与配体和G蛋白复合物的高分辨率结构。相关研究成果以Structures of glucocorticoid-bound adhesion receptor GPR97-Go complex为题,于2021年1月6日在线发表在Nature上。
黏附类G蛋白偶联受体(Adhesion G protein-coupled receptors, aGPCRs)是GPCR超家族成员之一,在生物体一些重要的生理过程中发挥关键分子开关的作用,如脑的发育、水盐调节、炎症以及细胞命运决定等。与GPCR超家族其他成员相比,aGPCRs除了具有经典的7次跨膜核心(7TM)外,还具有较长的胞外区域,组成了拥有不同功能的结构域。目前普遍认为aGPCRs可被结合胞外的基质蛋白或可溶性小分子激活,然而,学界尚不清楚小分子配体是否可以直接结合7TM并激活受体。
糖皮质激素对机体的发育、生长、代谢及免疫等功能发挥重要的调节作用,是机体应激反应最重要的调节激素和临床上使用最广泛的抗炎及免疫抑制剂之一。经典理论认为,糖皮质激素通过与糖皮质激素核受体结合,并穿过核孔,在细胞核内发挥调控相关基因表达的作用。该作用方式通常需要较长的反应时间,被称为基因组机制。徐华强课题组分别在2002年和2014年解析了糖皮质激素核受体与地塞米松(Cell, 110: 93-105)和内源性糖皮质激素——氢化可的松(Cell Research, 24: 713–726)的晶体结构,揭示了糖皮质激素识别与功能调控其核受体的机制,推动了糖皮质激素受体靶向药物的开发。此外,糖皮质激素被发现能够快速引起细胞和机体的变化,这提示生物体内可能存在糖皮质激素的膜受体,其能够介导糖皮质激素的快速反应。研究发现,糖皮质激素的快速反应与G蛋白有密切关系,Gi的抑制剂PTX能够抑制糖皮质激素的快速作用,并据此推测GPCR是糖皮质激素的潜在膜受体。孙金鹏和山东大学教授易凡团队等对GPR97进行了受体生理学和内源性配体发现等工作,发现包括糖皮质激素类的氢化可的松、可的松以及11-脱氧皮质醇等在内的内源性类固醇激素均能够激活GPR97,其中,地塞米松具有更强的GPR97激活能力,并最终确认Go是GPR97激活后偶联的G蛋白通路。
在前期工作基础上,合作团队采用单颗粒冷冻电镜技术,分别对外源配体倍氯米松(BCM)以及内源性配体氢化可的松(cortisol)激活GPR97后形成的复合物进行了结构解析,最终分别获得了两个配体激活态的GPR97受体与Go蛋白的复合物结构,分辨率分别为3.1埃和2.9埃(图1a和1b)。
与其他GPCR亚家族成员相比,GPR97的7TM呈现独特的空间分布,其螺旋展现出与其他受体不同的长度。根据传统理论,aGPCR特有的胞外GAIN结构域和7TM在激活GPCR的过程中作为整体发挥其核心功能,然而,研究人员在结构中首次发现糖皮质激素结合在GPR97 7TM核心中的一个椭圆形正构结合口袋(图1c);此外,GPR97还展现出不同于其他A类GPCR成员的独特激活机制。GPR97序列中不含有保守的PIF、DRY和NPxxY等motif,其首先通过toggle switch W6.53识别配体并被激活。激活的受体借助首次发现的upper Quaternary core(UQC)将受体TM3-TM5-TM6捆绑在一起,继而通过HLY motif介导与Go蛋白的结合。受体7TM组成较大的胞内侧G蛋白结合口袋,3个胞内环均参与受体与G蛋白的相互作用,胞内环与受体的组成性激活密切相关;该研究中,研究人员还首次阐述了G蛋白的棕榈酰化修饰在其偶联GPCR中的关键作用。研究首次发现Gαo的α5螺旋C351位点被棕榈酰化修饰(图2),并进一步验证了该修饰在Go与GPR97的偶联中的独特作用。
综上,合作团队首次发现了糖皮质激素的高亲和力膜受体,并通过单颗粒冷冻电镜技术,解析了黏附类GPCR家族中GPR97在糖皮质激素的激活作用下与Go蛋白复合物的结构,从而在近原子分辨率上揭示了糖皮质激素识别并激活膜GPR97,以及受体偶联Go蛋白的分子机制。该成果将对糖皮质激素膜受体功能研究和黏附类GPCR的激活机制理解发挥重要的示范及推动作用。
上海药物所为该研究的第一完成单位。上海药物所与山东大学基础医学院联合培养博士生平玉奇,浙江大学基础医学院博士后毛春友,山东大学基础医学院副教授肖鹏、硕士研究生赵儒嘉,上海药物研究所研究员蒋轶为论文的共同第一作者;孙金鹏、张岩、徐华强为论文的共同通讯作者,易凡和山东大学教授于晓为论文的共同作者。研究工作得到国家基金委、科技部、上海市科委等单位的支持。
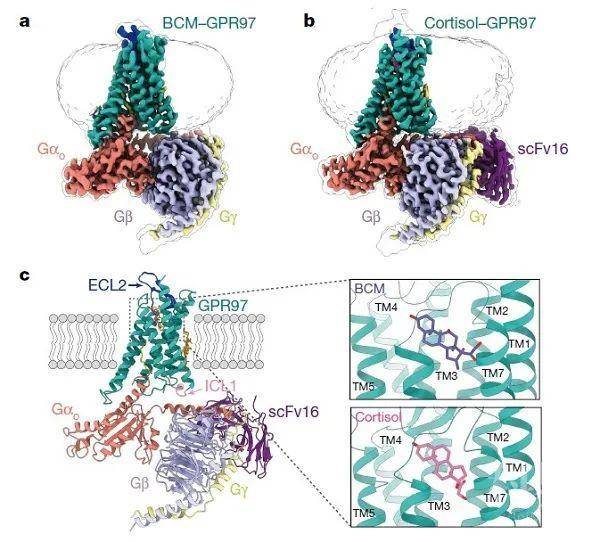
图1.GPR97的冷冻电镜结构
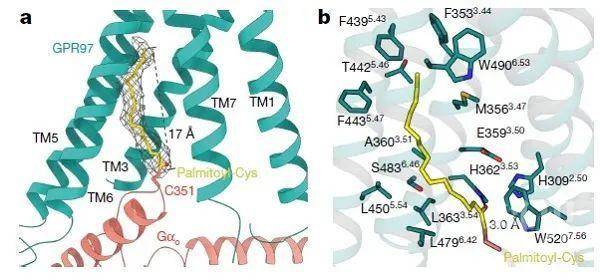
图2.Go棕榈酰化修饰
来源:zkyzswx 中科院之声
原文链接:http://mp.weixin.qq.com/s?__biz=MjM5NzIyNDI1Mw==&mid=2651786157&idx=2&sn=734ddbb18ab79c51ae38237fd5968428
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn