来源:BioArt
哺乳动物细胞通过称为缺氧诱导因子(hypoxia-inducible factors, HIFs)的转录调节因子对氧气不足做出反应。尽管具有短暂的保护作用,但长期的HIF激活会在不同组织中驱动不同的病理反应,例如促进肥胖症患者的炎症和胰岛素抵抗以及阻止早产儿白质形成等【1,2】。这种细胞功能障碍很大程度上归因于所有细胞类型共享的经典低氧应答的激活时间延长。然而,难以解释的是保守的缺氧特征基因如何导致多样的细胞表型。
近日,来自美国凯斯西储大学医学院的Paul J. Tesar课题组在Cell Stem Cell 杂志上发表了一篇题为“Non-canonical Targets of HIF1a Impair Oligodendrocyte Progenitor Cell Function” 的文章,作者使用衍生于多能干细胞的少突胶质细胞祖细胞(oligodendrocyte progenitors, OPCs)中慢性HIF1a累积模型,证明HIF1a可以通过激活非经典靶标以损害OPCs来源的少突胶质细胞的产生。在这项工作中,作者以少突胶质细胞为例,确立细胞类型特异性的HIF1a靶标干扰特定类型细胞应答低氧功能的观点,对于其他组织细胞类型缺氧应答的研究具有借鉴意义。

首先,为了探索HIF介导的少突胶质细胞发育阻断的潜在机制,作者在小鼠多能干细胞衍生的OPCs中生成了慢性HIF1a积累的细胞模型。由CRISPR-Cas9介导的Vhl敲除的OPC(sgVhl OPC)与低氧条件下培养的OPC在蛋白质和RNA水平上反应相似。那么,HIF1a累积是OPC分化的泛抑制剂还是特异性抑制剂呢?作者刺激sgVhl OPCs形成星形胶质细胞或少突胶质细胞,对两种细胞类型标志物染色,证明HIF1a的作用是少突胶质细胞特异性的,随后通过对其分化不同阶段标记物进行染色显示,所有阶段标志物的获取均发生延迟。因此,这些数据表明HIF1a的累积会特异性的破坏OPC的早期分化,从而延迟少突胶质细胞和髓磷脂的形成。
为了确认负责特异性阻断少突胶质细胞发育的HIF1a的基因靶标,作者主要通过ChIP-seq绘制全基因组染色质结合图谱,以及与小鼠其他细胞类型数据集的比对,发现OPCs特定HIF1a峰下谱系特定转录因子Olig2的基序高度富集,而不富集于其他任何组织特异性HIF1a峰,进一步的免疫共沉淀也证实HIF1a与Olig2的物理相互作用。此外,作者还发现一种从OPCs分化为少突胶质细胞所需的转录因子Sox10及其下游靶基因Plp1和Pdgfra在sgVhl OPC中发生降低,而其他谱系转录因子保持不变。值得注意的是,HIF1a并不与之结合,表明HIF1a是通过激活“其他基因”靶标来间接抑制Sox10从而阻断少突胶质细胞的发育。
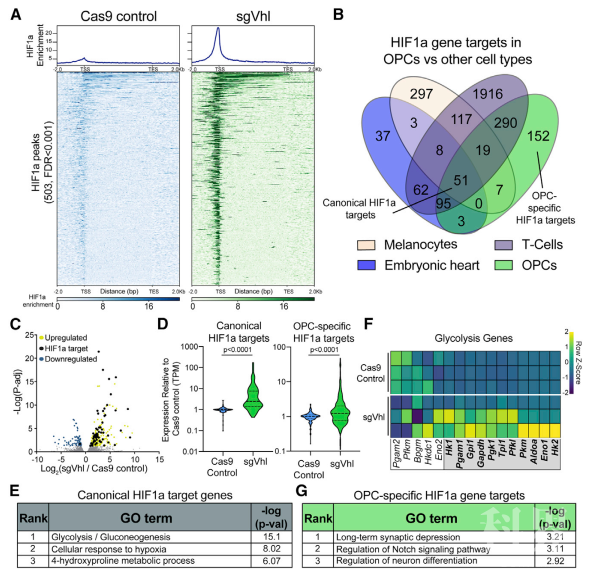
图1,OPC特异性的HIF1a靶标鉴定方法及结果
接下来,作者想知道HIF1a直接作用的“其他基因”,将重点放在属于OPCs特异性且HIF1a非经典靶标的排名靠前的Ascl2和Dlx3两个基因上。使用CRISPR激活(CRISPR activation, CRISPRA)技术在OPCs中异位表达Ascl2和Dlx3足以损伤分化过程中早期(O4+),中间(O1+)和晚期(MBP+)少突胶质细胞标记物的获取,且导致Sox10表达水平显着降低。已知ASCL2会损害体细胞干细胞的分化,并可以在关键分化基因上起阻遏作用,那么 ASCL2是否同样可以直接结合到Sox10的上游调控区域发挥分化阻断作用呢?作者通过CHIP-seq发现, ASCL2能够直接结合Sox10的上游增强子并减少Sox10的表达。值得注意的是,RNAi介导的sgVhl OPC中Ascl2或Dlx3的分别敲低并不能挽救少突胶质细胞的形成,提示这些非经典HIF1a靶标可能需要共同作用以抑制Sox10表达并损伤OPCs向少突胶质细胞的形成。
为了确定可能克服HIF1a施加的分化障碍的潜在通路,作者试图筛选出能够增加sgVhl OPC中MBP+少突胶质细胞形成能力的生物活性化合物。其中,MEK/ERK抑制剂在筛选中富集并能增导致少突胶质细胞形成增加。那么,MEK抑制作用是通过直接改善HIF1a积累情况还是调节其下游靶点来影响sgVhl OPC的分化呢?作者使用经测试的最有效MEK抑制剂300nM AZD8330处理细胞持续14小时,并不会改变HIF1a的核累积。此外,HIF1a的下游直接靶标Ascl2和Dlx3也并未增加MEK/ERK信号的激活。因此,这些数据提示MEK抑制剂处理是通过绕过HIF1a及其直接下游靶标的方式来影响少突胶质细胞的分化。
基因集富集分析(Gene set enrichment analysis, GSEA)显示AZD8330对sgVhl OPC的处理导致“少突胶质细胞分化”和“少突胶质细胞发育”通路的富集,且对少突胶质细胞分化至关重要的两个基因Sox10和Myrf表达降低。考虑到MEK抑制剂并不干涉HIF1a及其下游靶基因的表达,那么它所介导的Sox10表达增加的情况似乎不太可能对sgVhl OPC具有特异性。与此假设一致,在用300 nM AZD8330处理14小时的Cas9对照OPC中,Sox10表达也同样增加。但需要注意的是,MEK抑制剂会导致sgVhl OPC中少突胶质细胞的形成显着增加,而对对照OPC却几乎没有影响,这突显了HIF1a所施加的背景特异性阻断作用。以上数据表明,HIF1a累积引起的Sox10表达降低对于少突胶质细胞分化中HIF介导的阻滞至关重要,在不改变sgVhl OPC中经典HIF功能的情况下恢复Sox10表达可恢复少突胶质细胞的形成。
最后,为了评估MEK抑制在低氧人脑OPC中的作用,作者利用先前建立的从多能干细胞中产生能够进行髓鞘形成的大脑类器官的方法【3】。首先通过低氧探针(hypoxyprobe)定义类器官低氧区域的免疫组化证明,SOX10的表达显着受损。随后使用DMSO或300 nM AZD8330处理类器官,再次使用低氧探针处理并收集样品进行分析。结果显示,与类器官内的正常氧区相比,低氧区域的MYRF+少突胶质细胞数量显着减少了2.8倍,而AZD8330的处理导致低氧区域内少突胶质细胞的数量显着增加1.8倍。这些结果共同表明,氧张力会影响少突胶质细胞的发育,而MEK抑制克服了在人脑发育的3D模型中低氧介导的少突胶质细胞形成的抑制作用。
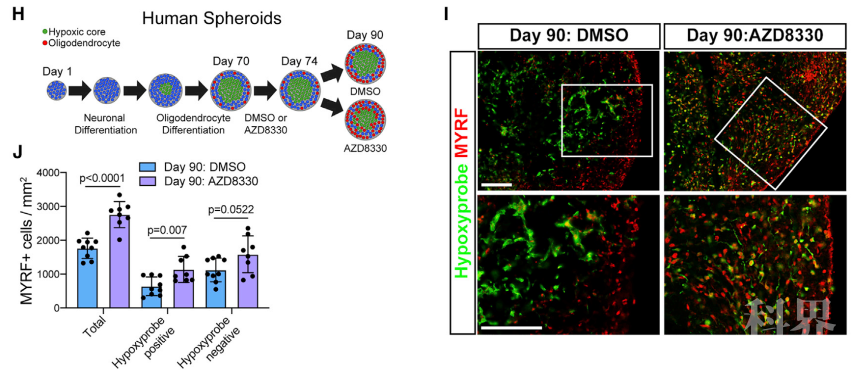
图2,MEK抑制剂可以恢复类器官中低氧区域少突胶质细胞形成能力
总的来说,在这项研究中作者对OPC中HIF1a的全基因组功能靶标进行了分析,发现HIF1a不仅与多种细胞类型共享的典型缺氧反应基因结合,而且还以细胞类型特异性方式激活了一组独特的非典型基因。然而,MEK/ERK信号调节Sox10表达的机制仍然未知,验证非经典HIF1a靶标的作用对于未来的研究和临床治疗都将十分重要,例如早熟弥漫性白质损伤和成人白质中风。此外,了解除OPC之外的其他细胞类型特异性的HIF1a靶点是否是低氧介导的功能障碍的关键驱动因素,也将是十分有趣的研究内容。
原文链接:
https://doi.org/10.1016/j.stem.2020.09.019
参考文献
1, Lee, Y.S., Kim, J.W., Osborne, O., Oh, D.Y., Sasik, R., Schenk, S., Chen, A., Chung, H., Murphy, A., Watkins, S.M., et al. (2014). Increased adipocyte O2 consumption triggers HIF-1a, causing inflammation and insulin resistance in obesity. Cell 157, 1339–1352.
2, Scafidi, J., Hammond, T.R., Scafidi, S., Ritter, J., Jablonska, B., Roncal, M., Szigeti-Buck, K., Coman, D., Huang, Y., McCarter, R.J., Jr., et al. (2014). Intranasal epidermal growth factor treatment rescues neonatal brain injury. Nature 506, 230–234.
3, Madhavan, M., Nevin, Z.S., Shick, H.E., Garrison, E., Clarkson-Paredes, C., Karl, M., Clayton, B.L.L., Factor, D.C., Allan, K.C., Barbar, L., et al. (2018). Induction of myelinating oligodendrocytes in human cortical spheroids. Nat. Methods 15, 700–706.
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652514260&idx=6&sn=46d9e9dbdf5aac5ff969e0993a593bc0
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn




