来源:BioArt
癌症的免疫治疗主要依靠细胞毒性T细胞来杀伤肿瘤细胞,已成为当前肿瘤治疗研究领域的一大热点。以CAR-T和免疫检查点PD-1/L1为目标的免疫治疗已经成功应用于部分癌症的治疗。虽然这种疗法对一部分癌症病人有效,但大部分癌症病人并没有收到很好的效果。不同的肿瘤对免疫疗法的响应不同,这主要是受肿瘤组织主要组织相容性复合物(MHC)途径的影响。与T细胞不同的是,MHC-非限制性的细胞毒性淋巴细胞(包括自然杀伤(NK)细胞)可以不受MHC的限制而杀死对T细胞有抗性的肿瘤细胞。探索MHC-非限制性的细胞毒性淋巴细胞的机理对于发展免疫治疗的新策略具有重要的意义。
2020年11月27日,美国科罗拉多大学博尔德分校沈晶石教授课题组在Science Advances杂志上发表了题为“PBRM1 and the glycosylphosphatidylinositol pathway promote tumor killing mediated by MHC-unrestricted cytotoxic lymphocytes”的研究论文,对调控MHC-非限制性细胞毒性淋巴细胞杀伤肿瘤的关键因子进行了全基因组水平上的筛选,发现并鉴定了糖磷脂酰肌醇(GPI)锚生物合成通路和PBRM1在肿瘤杀伤过程中的调控功能。

在该项研究中,科研人员首先对MHC-非限制性的TALL-104细胞毒性细胞杀伤HAP1肿瘤细胞的过程进行了多次高通量基因筛选(图)。他们筛选出了PIGP, PIGS, PIGL 和 GPAA1等合成GPI锚定蛋白的基因。重要的是,这些基因并不参与肿瘤对T细胞介导的细胞毒性反应。筛选中鉴定出的另一个基因是PBRM1,它编码SWI/SNF染色质重塑复合物的一个亚基。肿瘤细胞中的PBRM1突变在T细胞介导的杀伤中具有敏化作用。与之相反,这些PBRM1突变引起对MHC-非限制性杀伤肿瘤的抵抗。进一步的机制研究表明PBRM1和GPI合成途径通过调节肿瘤细胞中NK细胞受体的配体来促进MHC-非限制性细胞毒性淋巴细胞的溶胞颗粒分泌。
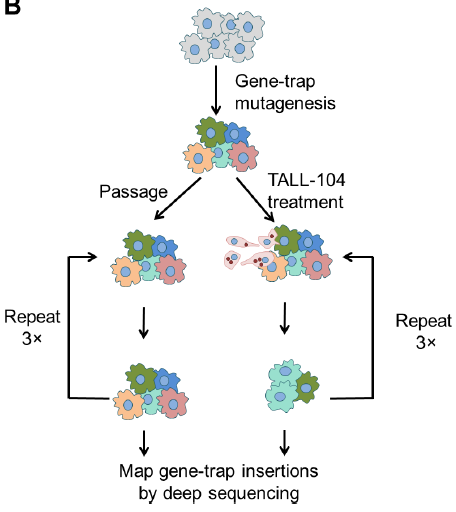
图. 对TALL-104杀伤HAP1细胞的调控因子进行高通量基因筛选
综上,该研究通过高通量基因筛选发现了参与调控MHC-非限制性杀伤肿瘤细胞的因子并探讨了它们调控肿瘤杀伤的作用机理。这些调节因子有可能作为癌症免疫治疗的新靶点。
原文链接:
http://advances.sciencemag.org/cgi/content/full/6/48/eabc3243
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652511830&idx=7&sn=d21db985e79a5d9c1d79dc7d75485a77
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn


