研究论文指出,三分之一的女性和半数男性会在有生之年被诊断出癌症。幸运的是,当肿瘤局限于很小的部位,可以借助手术、化疗等治疗手段将其清除。然而危险的是,癌细胞有时候会从原发肿瘤的位置扩散到身体其他部位,造成更广泛的侵袭,也使治疗更加困难。事实上,90%的癌症死亡是由癌细胞转移而引起的。

图片来源:123RF
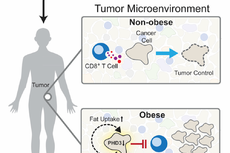
临床上观察到,在一些癌症中,肥胖的人发病率更高,也有更高的转移风险。以三阴性乳腺癌为例,这种类型侵袭性很强,而且风险和预后与患者的肥胖程度有关。
肥胖是如何影响癌症转移的呢?在近期发表于《科学》子刊Scientific Advances的一项新研究中,科学家们揭示了肥胖、脂肪组织和癌细胞转移之间的一种联系,从而为遏制癌细胞转移指出了新的方向。

科学家们重点关注了细胞外基质(ECM)的作用。细胞外基质是由胶原蛋白、弹性蛋白、层粘连蛋白、酶和其他糖蛋白等组成的混合物,为细胞生长提供了支撑。在肿瘤组织中,ECM也为肿瘤细胞的生长和侵袭提供了重要的微环境。
在这项研究中,研究人员设计了一种实验方法,来比较正常的苗条雌鼠和被喂肥的雌鼠的ECM。他们取出小鼠的乳腺组织,设法去除其中的细胞后,得到了完整的天然ECM。
蛋白质组学分析的结果显示,肥胖让小鼠乳腺ECM中近十种核心蛋白的含量发生了明显的改变,而其中增多的一些蛋白,比如胶原蛋白VI,由脂肪细胞产生。
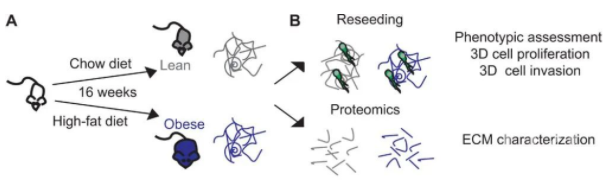
▲分析和比较瘦小鼠和胖小鼠的乳腺ECM(图片来源:参考资料[1])
这些变化与肿瘤有什么关系呢?研究人员从移植了三阴性乳腺癌细胞的肿瘤负荷小鼠身上,同样分离出乳腺ECM,发现其蛋白组成竟然和肥胖小鼠的十分相似。
更关键的是,当研究人员把一些乳腺癌细胞分别添加到瘦小鼠和胖小鼠的乳腺ECM上,发现从胖小鼠身上分离的ECM可以像肿瘤负荷小鼠的一样,让肿瘤细胞在上面快速迁移;相反,肿瘤细胞在瘦小鼠的ECM中生长时,很少会迁移。换句话说,在肥胖个体中,ECM似乎早早地为肿瘤细胞做好了转移的准备。
进一步分析表明,肥胖小鼠ECM中增多的那些胶原蛋白VI,正是促进三阴性乳腺癌细胞迁移的重要驱动力。当研究人员给小鼠使用药物抑制脂肪细胞产生胶原蛋白VI后,肿瘤的生长和侵袭得到了控制。
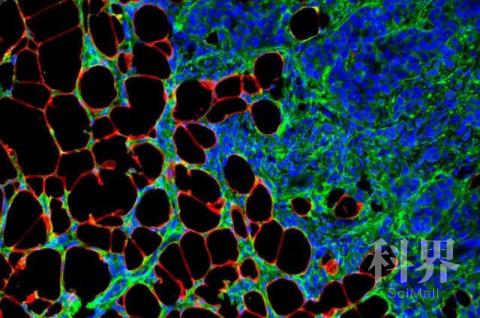
▲脂肪组织(红色)为附近的乳腺癌细胞(蓝色)提供了大量胶原蛋白VI(绿色)(图片来源:参考资料[2])
从小鼠实验中获得的结果在人类患者的样本中得到了一些初步验证。研究人员检查了肥胖程度不同的三阴性乳腺癌患者的活检组织,发现BMI越高的患者,其肿瘤周围区域内的胶原蛋白VI含量越高。负责该研究的Madeleine Oudin教授表示,针对ECM的这些发现或有助于指出癌症治疗的新药靶标。
研究人员强调,如今肥胖正成为流行的问题,根据美国CDC的数据,美国成年人中已有70%超重或肥胖,了解肥胖如何影响癌症转移,也将对更好地应对癌症提供重要的洞见。
参考资料:
[1] Andrew L. Wishart et al., (2020) Decellularized extracellular matrix scaffolds identify full-length collagen VI as a driver of breast cancer cell invasion in obesity and metastasis. Science Advances. Doi: 10.1126/sciadv.abc3175
[2] The obesity and cancer metastasis connection. Retrieved Nov. 11, 2020 from https://medicalxpress.com/news/2020-10-obesity-cancer-metastasis.html
内容来源:环球科学
来源:环球科学
原文链接:http://www.huanqiukexue.com/a/qianyan/shengwu__yixue/2020/1117/30693.html
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn