肝脏星状细胞占肝脏固有细胞总数的15%,占非实质细胞的30%左右。HSC存在于Disse腔中,呈梭形或多边形,胞浆内有多个富含维生素A的脂滴,其细长的突起向外延伸环绕在血窦内皮细胞外面,是体内储存视黄醛衍生物的首要部位。在正常肝脏中,星状细胞处于静止状态,不表达α平滑肌肌动蛋白(α-SMA),增殖活性低,合成胶原能力低,其主要功能是贮存视黄醛类。
简介肝星状细胞是ECM的主要来源, HSC激活并转化为肌成纤维细胞样细胞(MFC),各种致纤维化因素均把HSC作为最终靶细胞。肝星状细胞激活并转化为肌成纤维细胞样细胞(MFC),各种致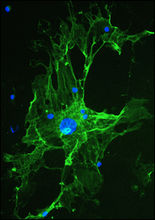 纤维化因素均把HSC作为最终靶细胞,正常情况下肝星状细胞处于静止状态。当肝脏受到炎症或机械刺激等损伤时,肝星状细胞被激活,其表型由静止型转变为激活型。激活的肝星状细胞一方面通过增生和分泌细胞外基质参与肝纤维化的形成和肝内结构的重建,另一方面通过细胞收缩使肝窦内压升高。
纤维化因素均把HSC作为最终靶细胞,正常情况下肝星状细胞处于静止状态。当肝脏受到炎症或机械刺激等损伤时,肝星状细胞被激活,其表型由静止型转变为激活型。激活的肝星状细胞一方面通过增生和分泌细胞外基质参与肝纤维化的形成和肝内结构的重建,另一方面通过细胞收缩使肝窦内压升高。
背景早在1876年,德国CarlvonKupffer在使用氯化金染色法研究肝脏的神经系统时无意中发现肝血窦周围有呈星状形态的细胞,将其命名为星状细胞(sternzellen)。1898年,Kupffer用印度墨水对兔肝进行染色时,观察到能吞噬墨水颗粒的肝巨噬细胞,也就是后来人们为纪念Kupffer而命名的Ku pffer细胞。因为同样为星状形态,Kupffer误把肝巨噬细胞和星状细胞混为一谈,认为星状细胞就是肝巨噬细胞。这种观点在当时得到了广泛的认同。直到1951年,日本学者ToshioIto通过光学显微镜发现人的肝窦周围有一种富含脂质小滴、并且有网状纤维包绕的细胞,并将之命名为伊东细胞(ItoCel1s)或贮脂细胞(fat-storingcells)。1958年,Suzuki用银染色法在Disse腔内观察到这种星芒状的细胞,发现其突起与肝脏内的自主神经末梢相连系,他认为这种细胞能将来自肝内自主神经的冲动传递给肝实质细胞,并将其称为“间质细胞”;1966年,Bronfenmajor证实了伊东细胞的发现,又给该细胞起新名叫脂细胞(1ipocytes);1971年,KenjiroWake采用电镜,结合氯化金染色法和苏丹红染色法发现Ito所描述的伊东细胞和Kupffer所发现的星状细胞原来是同一类型的细胞,并指出上述细胞既不同于肝窦内皮细胞,也不是肝内的巨噬细胞。这种细胞富含VitaminA和脂质小滴,其中脂质小滴发出的自体荧光,以及这种细胞能被氯化金染色的特性都与VitaminA的存在有关。至此,人们才揭开了这种星芒状细胞的真实面目,并开始了对其功能的研究,逐渐发现了它与肝纤维化的关系。1995年,国际上正式将其命名为HSC。
pffer细胞。因为同样为星状形态,Kupffer误把肝巨噬细胞和星状细胞混为一谈,认为星状细胞就是肝巨噬细胞。这种观点在当时得到了广泛的认同。直到1951年,日本学者ToshioIto通过光学显微镜发现人的肝窦周围有一种富含脂质小滴、并且有网状纤维包绕的细胞,并将之命名为伊东细胞(ItoCel1s)或贮脂细胞(fat-storingcells)。1958年,Suzuki用银染色法在Disse腔内观察到这种星芒状的细胞,发现其突起与肝脏内的自主神经末梢相连系,他认为这种细胞能将来自肝内自主神经的冲动传递给肝实质细胞,并将其称为“间质细胞”;1966年,Bronfenmajor证实了伊东细胞的发现,又给该细胞起新名叫脂细胞(1ipocytes);1971年,KenjiroWake采用电镜,结合氯化金染色法和苏丹红染色法发现Ito所描述的伊东细胞和Kupffer所发现的星状细胞原来是同一类型的细胞,并指出上述细胞既不同于肝窦内皮细胞,也不是肝内的巨噬细胞。这种细胞富含VitaminA和脂质小滴,其中脂质小滴发出的自体荧光,以及这种细胞能被氯化金染色的特性都与VitaminA的存在有关。至此,人们才揭开了这种星芒状细胞的真实面目,并开始了对其功能的研究,逐渐发现了它与肝纤维化的关系。1995年,国际上正式将其命名为HSC。
性质及功能HSC位于Disse间隙内,紧贴着肝窦内皮细胞(sinusoidalendothelialcells,SEC)和肝细胞。其形态不规则,胞体呈圆形或不规则形,常伸出数个星状胞突包绕着肝血窦。此外,HSC还伸出胞突与肝细胞、邻近的星状细胞相接触。HSC胞质内有1~14个直径约1.0~2.0μm的富含维生素A和甘油三酯的脂滴,胞浆中有丰富的游离核糖体、粗面内质网及发达的高尔基复合体。胞核形态不规则,由于脂滴的挤压,常致细胞核有一个或多个凹陷,核内可见1~2个核仁。正常肝脏中HSC的数目很少,只占肝细胞总体数目的5%~8%及总体体积的1.4%,但HSC的立体分布和伸展足以覆盖整个肝窦微循环。
正常情况下HSC表现为富含VitA脂滴的静止型,其功能主要有:
(1)代谢和贮存VitA:肝脏储存有体内80%左右的维生素A,对体内维生素A的代谢起着重要作用。视黄醛在小肠内酯化后被运输到肝脏并与特异的视黄醛结合蛋白结合,然后转运到邻近的HSC储存。
(2)储存脂肪:正常HSC胞质内的脂滴含有大量的甘油三酯,为肝细胞提供能源。
(3)合成和分泌胶原及糖蛋白、蛋白多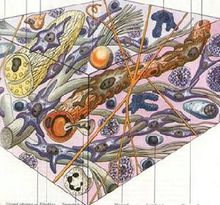 糖等基质成分:研究认为,HSC是正常及纤维化肝脏中细胞外基质(extracellularmatrix,ECM)的主要合成细胞。正常肝脏中HSC合成的胶原以Ⅰ型、Ⅲ和Ⅳ型为主,其合成量是肝细胞的10倍、内皮细胞的20倍以上。HSC还能合成纤维连接蛋白、层连蛋白和粗纤维调理素等糖蛋白成分,以及硫酸皮素、硫酸软骨素和透明质酸等蛋白多糖。
糖等基质成分:研究认为,HSC是正常及纤维化肝脏中细胞外基质(extracellularmatrix,ECM)的主要合成细胞。正常肝脏中HSC合成的胶原以Ⅰ型、Ⅲ和Ⅳ型为主,其合成量是肝细胞的10倍、内皮细胞的20倍以上。HSC还能合成纤维连接蛋白、层连蛋白和粗纤维调理素等糖蛋白成分,以及硫酸皮素、硫酸软骨素和透明质酸等蛋白多糖。
(4)合成基质金属蛋白酶(matrixmetalloproteinase,MMP)及其组织抑制剂(tissueinhibitorofmetalloproteinases,TIMP):正常情况下,HSC能分泌多种胶原酶和基质降解蛋白酶如基质金属蛋白酶(matrixmetalloproteinase,MMP)-1、MMP-2等以降解各种细胞外基质,同时分泌组织金属蛋白酶抑制剂(tissueinhibitorofmetalloproteinase,TIMP-1)防止胶原过度降解,使肝脏ECM的合成和分解处在一个动态平衡中。
(5)表达细胞因子及受体:正常情况下,HSC可以分泌肝细胞生长因子(HGF),参与肝细胞再生的调控。此外,HSC还能表达少量的转化生长因子(transforminggrowthfactor-β,TGF-β)、血小板衍生的生长因子(Plateletderivedgrowthfactor,PDGF)和胰岛素样生长因子(IGF)等,同时HSC能表达TGF-β1的II、III型受体和PDGF受体的α亚单位等。
(6)参与肝窦血流调节:HSC伸出胞突包绕着肝窦,通过其纤长突起的收缩功能调节肝窦内微循环,从而影响着肝脏的血流分布和门静脉压力。
生物学特征正常情况下肝星状细胞处于静止状态。当肝脏受到炎症或机械刺激等损伤时,肝星状细胞被激活,其表型由静止型转变 为激活型。肝星状细胞位于肝窦周Disse 腔内,约占肝脏所有细胞的13%。在规HE染色的肝组织切片中,不能显示星状细胞,但可用免疫组织化学将其定位,并可将其分离进行体外细胞培养。正常情况下肝星状细胞呈静止状态,它在肝脏中的生理功能主要有参与维生素A 的代谢,储存脂肪的功能,肝星状细胞的胞浆中含有类视黄醇物质的脂滴,是维生素A 的主要储存处,肝星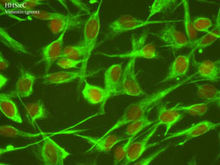 状细胞还有调节血管和肝窦血流的作用。在病理条件下如肝脏受到物理、化学及病毒感染生物因素的刺激时,肝星状细胞增殖并激活,转变为“肌成纤维细胞”,表达α-平滑肌动蛋白、合成ECM等。当肝脏有炎症时,肝星状细胞发生激活, Gressner 等研究提出了肝星状细胞激活的“三步级联反应”。模式激活型的肝星状细胞具有以下特征:
状细胞还有调节血管和肝窦血流的作用。在病理条件下如肝脏受到物理、化学及病毒感染生物因素的刺激时,肝星状细胞增殖并激活,转变为“肌成纤维细胞”,表达α-平滑肌动蛋白、合成ECM等。当肝脏有炎症时,肝星状细胞发生激活, Gressner 等研究提出了肝星状细胞激活的“三步级联反应”。模式激活型的肝星状细胞具有以下特征:
1、胞体增大,胞突伸展。胞质中脂滴消失,VitA含量减少。胞质内粗面内织网、高尔基体发达,具有旺盛的蛋白质合成能力;
2、细胞增生频率增加, 并且向肝损伤部位迁徙;
3、表达α-平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)、波形蛋白(vimentin)及结蛋白(desmin),成为肌纤维样母细胞;
4、收缩性增强;
5、ECM分泌增加;
6、细胞因子、趋化因子及受体分泌增加;
7、TIMP合成及分泌增加,使ECM成分降解减少。其中α-SMA的表达为HSC激活的标志。
活化肝星状细胞的持续激活是肝纤维化发生发展过程中的关键环节。激活的肝星状细胞一方面通过增生和分泌细胞外基质参与肝纤维化的形成和肝内结构的重建,另一方面通过细胞收缩使肝窦内压升高,这两类变化最终奠定了肝纤维化、门静脉高压症发病的病理学基础。肝星状细胞的激活过 程十分复杂,包括两个主要阶段:启动阶段及持续阶段。持续阶段则是这些刺激因素维持肝星状细胞的活化表型,结果引起肝纤维化的形成。启动阶段主要是依赖于旁分泌刺激因素。而持续阶段则与旁分泌、自分泌刺激因素均有关。
程十分复杂,包括两个主要阶段:启动阶段及持续阶段。持续阶段则是这些刺激因素维持肝星状细胞的活化表型,结果引起肝纤维化的形成。启动阶段主要是依赖于旁分泌刺激因素。而持续阶段则与旁分泌、自分泌刺激因素均有关。
启动阶段启动阶段是指早期基因表达的改变及在细胞因子等刺激因素作用下产生的细胞表型改变。当肝实质细胞受到损伤时,邻近的肝细胞、库普弗细胞、窦内皮细胞和血小板等通过旁分泌作用可分泌多种细胞因子,如肿瘤坏死因子α(TNF-α)、转化生长因子β(TGF-β)、胰岛素生长因子(IGF-1)、肝细胞生长因子(HGF)、血小板源性生长因子(PDGF)、内皮素(ET)-1等,作用于HSC并使之出现肌成纤维母细胞(myofibroblast,MFB)样表型转化,激活并导致细胞增殖、ECM合成增加等。激活后的肝星状细胞可自分泌TGF、PDGF、ET等细胞因子使活化得以持续,此时即使除去原发因素纤维化仍会持续。
持续阶段持续阶段指由于上述各种因子的作用而维持星状细胞的激活状态并有纤维形成。肝星状细胞活化的持续阶段有以下特征性的变化,这些改变的直接或间接效应是增加ECM的沉积。此阶段肝星状细胞的活化受自分泌和旁分泌的双重调节。
(1)细胞增殖:PDGF是肝星状细胞的最强丝裂原,肝星状细胞活化早期PDGF受体增强了肝星状细胞对这种丝裂原的反应;
(2)细胞趋化聚集:肝星状细胞能向化学趋化剂的部位移动,在一定程度上解释了为什么肝星状细胞在肝内多分布在炎性间隔内;
(3)纤维形成:增加基质形成是肝星状细胞活化导致肝纤维化的最直接途径。一方面,ECM合成的量增加;另一方面,合成的ECM种类异常,在正常情况下,肝星状细胞以合成型胶原为主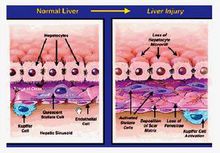 。而活化后则以产生型胶原为主;
。而活化后则以产生型胶原为主;
(4)细胞的收缩作用:肝星状细胞的收缩作用可能是引起肝纤维化后门静脉阻力增加的重要因素。晚期肝硬化典型的纤维带中充满着大量肝星状细胞,活化的肝星状细胞通过收缩窦周和收缩硬化的肝脏阻碍门静脉血流。引起肝星状细胞收缩的主要刺激因子是内皮素-1(endothelin-1,ET-1),其受体在静止或活化的HSC均有表达;
(5)基质降解:在肝纤维化过程中,伴随着ECM重构,基质蛋白酶质和量的改变起重要作用。肝星状细胞几乎能表达基质降解所需要的所有关键成分,因此,活化的肝星状细胞不仅在ECM生成过程中起作用,而且在ECM降解过程中也起重要作用。基质蛋白酶家族是一类钙依赖蛋白酶,能够特异性地降解胶原蛋白和一些非胶原蛋白成分。根据基质蛋白酶对底物的特异性将其5类:①间质性胶原酶;②明胶酶;③溶基质素;④膜型基质金属蛋白酶;⑤金属弹力蛋白酶;
(6)视黄醇类消失:随着肝星状细胞活化,细胞失去了其特征性的核周视黄醇(维生素A)脂滴;
(7)白细胞趋化及释放细胞因子:除了肝脏内多种细胞因子通过旁分泌发挥作用外,肝星状细胞自分泌的细胞因子对其活化的持久延续也很重要。活化的肝星状细胞自分泌TGF-B以及ET-1。分别导致肝星状细胞产生大量ECM和具有收缩性。肝星状细胞还能通过诱导单核巨噬细胞浸润来扩大炎症效应。
凋亡激活的肝星状细胞有两个去向:
(1)由激活态转变回静止态。研究认为IL-10是一种能够调控这一反应的刺激因子,可以下调炎症反应并增加组织间隙胶原酶的活性;
(2)发生细胞凋亡而死亡。体外培养试验表明,静止的肝星状细胞不发生凋亡,肝星状细胞在活化的同时出现自发性凋亡。近年来,有关肝星状细胞凋亡分子机制的研究进展较快,现已证明有多种基因产物参与肝星状细胞凋亡过程。其中包括死亡受体家族如Fas与FasL系统、天冬氨酸特 异性半胱氨酸蛋白酶即Caspase家族、bcl-2调节蛋白家族等。人们通过对这些蛋白家族成员生化特性、生物功能以及上游下游分子作用机理的深入研究,提出了肝星状细胞凋亡主要的两条信号转导通路:细胞凋亡的线粒体依赖性途径和死亡受体途径。两条通路的结果都是引发了Caspase家族的级联反应,最终表现为凋亡的产生。
异性半胱氨酸蛋白酶即Caspase家族、bcl-2调节蛋白家族等。人们通过对这些蛋白家族成员生化特性、生物功能以及上游下游分子作用机理的深入研究,提出了肝星状细胞凋亡主要的两条信号转导通路:细胞凋亡的线粒体依赖性途径和死亡受体途径。两条通路的结果都是引发了Caspase家族的级联反应,最终表现为凋亡的产生。
调控1、Fas/FasL系统Fas也称Apo-1或CD95,属于肿瘤坏死因子(tumornecrosisfactor,TNF)受体和神经生长因子(nervegrowthfactor,NGF)受体超家族。Fas是一个48kDa的I型跨膜蛋白分子,由319个氨基酸组成,定位于人10号染色体长臂。Fas主要分布于组织细胞中,少量以可溶性形式(sF as)存在于细胞质和血清中。Fas配体(FasLigand,FasL)是一个分子量约为40kDa,属于TNF家族的Ⅱ型跨膜蛋白分子,其C端位于胞外,N端深入胞内,定位于人1号染色体。主要表达于活化的T淋巴细胞表面。FasL或Fas抗体与细胞表面的Fas结合可诱导细胞凋亡。
as)存在于细胞质和血清中。Fas配体(FasLigand,FasL)是一个分子量约为40kDa,属于TNF家族的Ⅱ型跨膜蛋白分子,其C端位于胞外,N端深入胞内,定位于人1号染色体。主要表达于活化的T淋巴细胞表面。FasL或Fas抗体与细胞表面的Fas结合可诱导细胞凋亡。
2、Caspases家族近年来,在机体内发现多种半胱天冬蛋白酶(cysteineaspartate-specificproteinase,caspase)家庭成员,它们是结构特征相似的同源蛋白酶,这些蛋白酶都是特异性的在底物的天冬氨酸序列后切断肽键。在哺乳动物细胞内至少发现了十三种,编号Caspase-1~13,其中包括两个在人类还未找到相应对等物的小鼠Caspase-11、12。根据其序列同源性可将它们分为三个亚家族:ICE样、ICH-1样和CPP32样蛋白酶。Caspase家族的过度表达均可引起一系列不可逆转的蛋白质裂解,最终导致细胞死亡,可以说,Caspases蛋白的表达是各种细胞凋亡机制共同的最后通路。
本词条内容贡献者为:
董慧珠 - 副主任医师 - 山西省心血管病医院 神内