来源:X一MOL资讯
肿瘤微环境(TME)涉及新生血管、失调的生物合成中间体、乏氧与微酸环境等异常的理化条件,与肿瘤的产生、发展、侵袭性转移等行为密切相关。因此,开发具有肿瘤微环境响应性的智能诊疗试剂对实现针对肿瘤的精准治疗及降低副作用方面具有明显优势。然而,目前仍旧缺少简便的方法制备满足诊疗需求的TME响应型诊疗材料。
碳点(carbon dots, CDs)作为一类新型荧光纳米材料,凭借其优异的光学性能、良好的生物相容性、易于修饰性及潜在的光热(PTT)/光动力(PDT)治疗性能而在肿瘤诊疗领域展现出巨大的应用潜力。如何赋予CDs针对TME特异识别、响应的性能,有效提升其在肿瘤组织的富集,同时实现增强的治疗效果,是提升CDs在肿瘤诊疗领域应用价值所亟待解决的问题。
近日,中科院宁波材料所/江南大学林恒伟研究员(教授)等人通过简便组装的方式,以光敏剂二氢卟吩e6(Ce6)修饰的荧光碳点(CDs-Ce6)及铜离子(Cu2+)作为功能性结构单元构建了TME智能响应型纳米诊疗平台(Cu/CC NPs),可用于荧光成像介导下的肿瘤协同治疗。
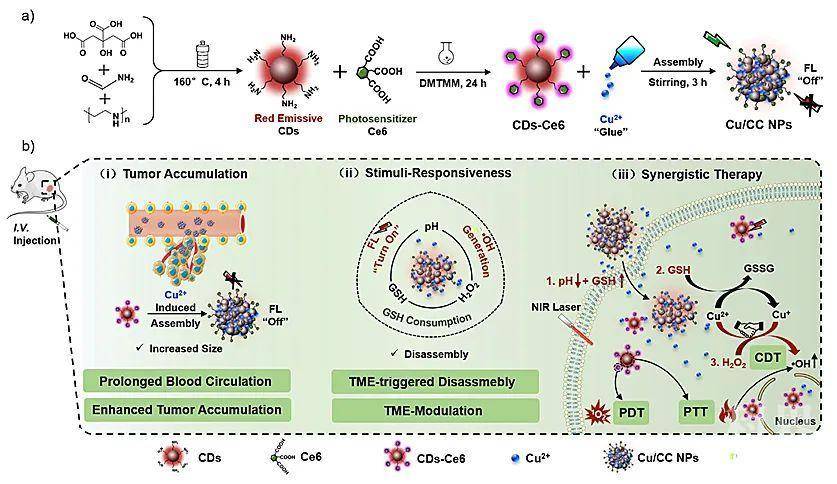
图1. 研究思路示意图
该组装体具有利于血液长循环的颗粒尺寸,其荧光与光敏性能在正常生理环境中处于“off”的状态。当进入肿瘤组织后,Cu2+离子一方面在高浓度双氧水(H2O2)存在条件下发生类芬顿反应,发挥化学动力学治疗功能(CDT);另一方面消耗过表达的谷胱甘肽(GSH)以增强细胞内活性氧(ROS)的产生,放大氧化应激水平,提高治疗效率。值得注意的是,被还原的Cu+与CDs-Ce6之间的络合能力减弱,在肿瘤微酸环境的作用下诱导组装体发生解组装,促使荧光及光敏性能有效恢复,可控的转变为“on”的状态。除了基于TME智能响应的特性,Cu/CC NPs还展现出良好的光热转换性能及“GSH+弱酸环境”激活的光动力性能。
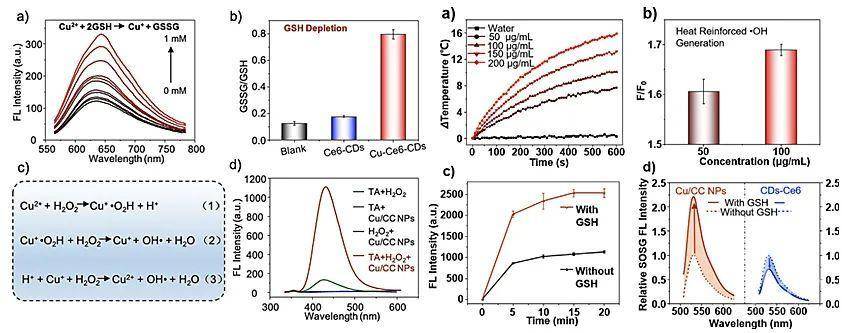
图2. Cu/CC NPs的内源(TME)及外源(激光)刺激响应性
Cu/CC NPs结合了PTT、PDT和光热增强的CDT协同治疗模式,在提高肿瘤治疗效率的同时有效降低了副作用。该研究一方面针对CDs在肿瘤生物医学中的应用,提出了解决CDs缺乏TME特异性识别/响应能力、肿瘤累积不充分及单一治疗模式限制的问题的策略,另一方面也丰富了金属离子在肿瘤治疗中的潜在价值。
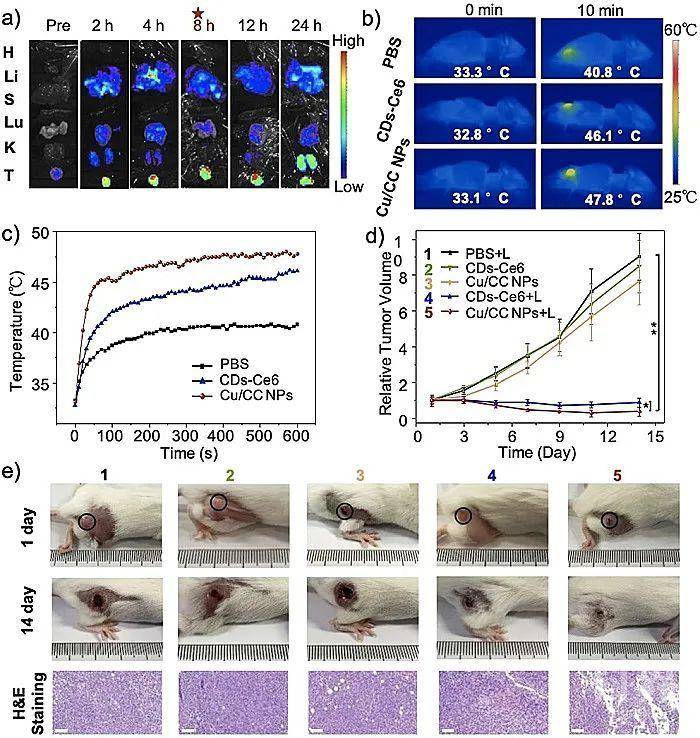
图3. Cu/CC NPs在小鼠内的累积(荧光成像)、光热成像及治疗效果
相关论文近期发表于Angew. Chem. Int. Ed.。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657661214&idx=4&sn=13645ddc925c526d9886e8b000f7f84a&chksm=80f898ceb78f11d87d98871629e7519c49bbb65777632db3c1e3e9ca0139d9be728e2a93908d&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



