细胞凋亡(apoptosis)是细胞接受某种信号或受到某些因素刺激后,为维持内环境稳定,由基因控制的细胞自主有序的死亡,在个体生长发育以及相关疾病(如癌症、糖尿病和神经退行性疾病等)的发生、发展中起着重要的作用。细胞凋亡受泛素(ubiquitin)-蛋白酶体(proteasome)通路和细胞自噬(autophagy)通路等多种信号通路调控。泛素-蛋白酶体通路负责细胞内大多数蛋白质的降解,对各种细胞活动至关重要。而在特定的生理或病理条件下,细胞自噬可通过溶酶体降解错误折叠蛋白、蛋白质聚集物和细胞器等细胞内物质,在防止细胞凋亡发生中起着一定的作用。
自噬起始最为关键的环节之一是自噬小体(autophagosome)形成。自噬标志性蛋白LC3-II不仅参与自噬小体的形成,也是自噬途径的底物受体,在自噬过程中起着至关重要的作用。自噬小体形成时,胞浆型LC3-I去掉一小段多肽,转变为自噬小体膜型LC3-II。这样,LC3-II/I比值的大小可估计自噬水平的高低。LC3-II可通过自噬降解,但其前体LC3-I是如何降解的一直是一个谜1。邱小波教授及其合作者研究发现LC3-I通过以PA28g为激活因子的蛋白酶体降解,显示蛋白酶体可直接调控细胞自噬。
虽然很多因素可激活自噬,但在正常状态下自噬是如何被抑制的仍不清楚。BRUCE/Apollon是一个巨型膜蛋白,分子量约为530 kDa,具有泛素化相关的E2和E3双重活性2-5。邱小波教授早期的工作揭示BRUCE是一个必需的凋亡抑制蛋白(IAP),会在凋亡启动时通过泛素连接酶Nrdp1(Neuregulin receptor degradation protein-1)/RNF41(Ring finger protein 41)介导的泛素-蛋白酶体通路降解5。他与合作者们最近发现BRUCE不仅抑制凋亡,而且通过其LIR (LC3-interacting region)结构域结合LC3-I,促进LC3-I降解,进而抑制自噬;BRUCE在自噬相关的应激条件下则可通过自噬-溶酶体途径降解。该结果提示BRUCE的这种作为凋亡和自噬的双闸效应可能恰恰是细胞维持正常状态的关键。
SIP (Siah1-interacting protein, 亦称CacyBP,Calcyclin-binding protein)与E3泛素连接酶Siah-1相互作用,并促进器官发育和肿瘤发生相关蛋白b-catenin的泛素化和降解6。SIP蛋白在多种哺乳动物的细胞和组织中表达,但在脑组织和多种肿瘤细胞中高表达。邱小波教授团队发现SIP通常抑制Nrdp1介导的BRUCE通过蛋白酶体通路的降解,并介导BRUCE从反面高尔基体网(trans-Golgi network)、循环内体(recycling endosome)转运至自噬小体,促进自噬的发生及线粒体自噬;但在DNA损伤类抗癌药物诱导下,SIP会在Nrdp1的作用下发生单泛素化,从而失去抑制Nrdp1介导的BRUCE通过蛋白酶体通路降解的能力,最终导致细胞凋亡。SIP基因敲除抑制细胞自噬,从而抑制BRUCE、损伤的线粒体和polyQ类蛋白聚集物通过自噬途径降解。总之,LC3-I通过蛋白酶体通路降解,而SIP通过抑制BRUCE介导的LC3-I通过蛋白酶体降解而促进自噬;并且,DNA损伤类抗癌药物会使SIP发生单泛素化,最终使细胞的命运从自噬向凋亡转变(图)。由于泛素化是一个可逆过程,SIP有可能在凋亡和自噬之间起到一个双向开关的作用。这种开关作用不仅对细胞应对微环境的微妙变化非常重要,而且可能在癌细胞应对DNA损伤类抗癌药物的反应中也起着关键的作用。
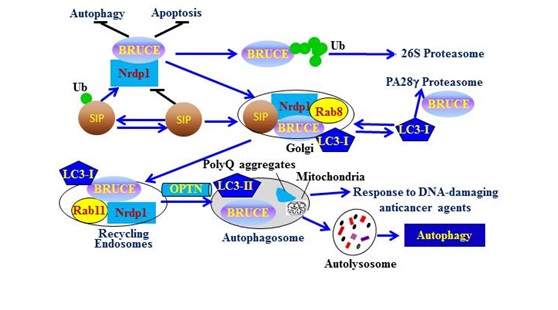
图:SIP通过抑制BRUCE介导的LC3-I经蛋白酶体降解促进自噬。
SIP调控LC3-I通过PA28g-蛋白酶体降解、细胞凋亡/自噬的转换及DNA损伤类抗癌药物的敏感性。
Nrdp1是由邱小波教授早期发现的一个泛素连接酶,可以介导凋亡抑制蛋白BRUCE、帕金森症关键蛋白Parkin以及表皮生长因子受体蛋白ErbB3通过泛素-蛋白酶体通路降解5,7,8。 Nrdp1还可以通过泛素化接头蛋白MyD88以及激酶TBK1而调控Toll样受体蛋白介导的免疫应答9。抗肿瘤药lenalidomide在骨髓发育异常综合症中具有十分重要的作用10,Nrdp1是lenalidomide的潜在靶标,其可与JAK2相关的细胞因子受体复合物互作,从而调控其在细胞表面的暴露以及功能11,12。Clec16a是I型糖尿病的关键蛋白,在线粒体自噬中具有重要作用,可促进自噬小体的成熟。Nrdp1可以通过泛素化Parkin并与Clec16a相互作用,从而调控线粒体自噬并影响糖代谢7,13。邱小波教授团队的这些成果,不仅有利于揭示细胞凋亡和自噬的调控机理,而且将为揭示多种人类重大疾病,包括癌症、糖尿病和神经退行性疾病等,发生和治疗的机理提供依据。
相关论文“SIP/CacyBP Promotes Autophagy by Regulating Levels of BRUCE/Apollon, which Stimulates LC3-I Degradation”已于2019年6月18日在线发表在《美国科学院院报》(Jiang et al., 2019,Proc. Natl. Acad. Sci. USA, published online June 18, 2019, https://doi.org/10.1073/pnas.1901039116)。邱小波教授和哈佛大学医学院的Alfred Goldberg院士为该文的共同通讯作者,我校姜天霞博士等5人及中科院微生物所刘翠华研究员为共同第一作者。参与这一工作的还有清华大学的李蓬院士和俞立教授、日本京都大学的Shu-ichi Matsuzawa教授、美国加州Sanford Burnham Prebys医学研究所的Ze’evRonai教授以及我校脑认知科学研究院舒有生教授和资源学院张文生教授等。该研究受到国家自然科学基金委员会和科技部国家重点研发计划相关项目资助。
参考文献
1 Rubinsztein, D. C. et al.Autophagy5, 585-589 (2009).
2 Bartke, T., Pohl, C., Pyrowolakis, G. & Jentsch, S. Mol Cell14, 801-811, (2004).
3 Hao, Y. et al.Nat Cell Biol6, 849-860, (2004).
4 Qiu, X. B. & Goldberg, A. L. J Biol Chem280, 174-182, (2005).
5 Qiu, X. B., Markant, S. L., Yuan, J. & Goldberg, A. L. EMBO J23, 800-810, (2004).
6 Matsuzawa, S.-i. & Reed, J. C. Molecular cell7, 915-926 (2001).
7 Zhong, L., Tan, Y., Zhou, A., Yu, Q. & Zhou, J. J Biol Chem280, 9425-9430, (2005).
8 Qiu, X. B. & Goldberg, A. L. Proc. Natl. Acad. Sci. U. S. A.99, 14843-14848, (2002).
9 Wang, C. et al.Nat. Immunol.10, 744-752, (2009).
10 Raza, A. et al.Blood111, 86-93, (2008).
11 Basiorka, A. A. et al.Cancer Res76, 3531-3540, (2016).
12 Wauman, J., De Ceuninck, L., Vanderroost, N., Lievens, S. & Tavernier, J. J. Cell Sci.124, 921-932, (2011).
13 Soleimanpour, S. A. et al.Cell157, 1577-1590, (2014).


