来源:iNature
DNA病毒通常在进入后将基因组DNA排出到宿主细胞的细胞核中。然而,尚不清楚核病原体衍生的DNA如何触发先天免疫反应。
2019年7月18日,曹雪涛团队在Science 在线发表题为“Nuclear hnRNPA2B1 initiates and amplifies the innate immune response to DNA viruses”的研究论文,该研究报道异质核核糖核蛋白A2B1(hnRNPA2B1)识别致病性DNA并扩增IFN-α/β的产生。在DNA病毒感染后,核定位的hnRNPA2B1感知病毒DNA,同源二聚化,然后通过精氨酸脱甲基酶JMJD6在Arg226处去甲基化。这导致hnRNPA2B1易位至细胞质,其中它激活TBK1-IRF3途径,导致IFN-α/β产生。另外,hnRNPA2B1促进NAS-甲基腺苷(m6A)修饰和CGAS,IFI16和STING mRNA的核质运输。这反过来又放大了由这些因子介导的细胞质TBK1-IRF3的活化。因此,hnRNPA2B1在启动IFN-α/β产生和增强STING依赖性细胞质抗病毒信号传导中起重要作用。
另外,2019年6月25日,曹雪涛团队在PNAS 在线发表题为“An endosomal LAPF is required for macrophage endocytosis and elimination of bacteria”的研究论文,该研究发现LAPF(含有PH和FYVE结构域的溶酶体相关和凋亡诱导蛋白)是细胞膜内陷介导的内吞作用所必需的。Lapf缺陷型巨噬细胞具有内吞和消除细菌的能力受损。巨噬细胞特异性Lapf缺陷小鼠对大肠杆菌(E.coli)感染更敏感,细菌负荷更高。此外,Lapf缺乏损害TLR4内吞作用,导致TLR-触发的促炎细胞因子的产生减弱。LAPF定位于早期内涵体并与caveolin-1相互作用。酪氨酸激酶Src对LAPF的磷酸化是LAPF-Src- Caveolin复合物形成和内吞作用以及细菌消除所必需的。总的来说,该研究表明LAPF对细菌的内吞作用和诱导炎症反应至关重要,这表明LAPF和Src可能是控制传染病的潜在靶标
2019年6月18日,曹雪涛团队在Cell Research 在线发表题为“Interferon-inducible cytoplasmic lncLrrc55-AS promotes antiviral innate responses by strengthening IRF3 phosphorylation”的研究论文,该研究鉴定了一种新的细胞质长非编码RNA(lncRNA),lncLrrc55-AS,它驱动正反馈环以促进干扰素调节因子3(IRF3)信号传导和IFN-I产生
2019年5月10日,中国医学科学院基础医学研究所北京协和医学院基础学院曹雪涛,姜明红等人在Cellular & Molecular Immunology 在线发表题为“E3 ubiquitin ligase RNF170 inhibits innate immune responses by targeting and degrading TLR3 in murine cells”的研究论文,该研究通过免疫沉淀巨噬细胞中的TLR3结合蛋白,将环指蛋白170(RNF170)鉴定为结合TLR3的E3连接酶。RNF170介导K766在TLR3的TIR结构域中的K48连接的多泛素化,并通过蛋白酶体途径促进TLR3的降解。RNF170的遗传缺失在体外和体内选择性地增强TLR3触发的先天免疫应答。 研究结果揭示了RNF170通过促进TLR3降解选择性抑制TLR3触发的先天免疫反应的新作用。
另外,曹雪涛团队在2019年还发表了7篇文章,在免疫领域取得新突破。

通过模式识别受体(PRR)识别病毒核酸可以触发对病毒的宿主先天免疫应答。这导致由干扰素调节因子(IRF)信号传导介导的由NF-κB信号传导和I型干扰素调节的促炎细胞因子的产生。通常,一旦DNA病毒进入宿主细胞,它们就会在宿主细胞核内弹出并复制它们的基因组DNA。然而,在细胞核内识别病原体的DNA的过程仍然是个谜。
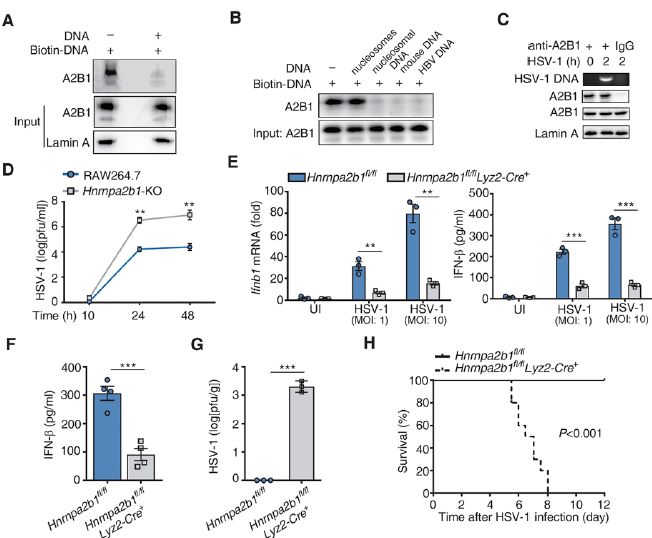
hnRNPA2B1激活抗病毒防御以抑制DNA病毒复制
迄今为止,只有一种蛋白质γ-干扰素诱导蛋白16(IFI16)被提出用于识别细胞核内的病毒DNA并激活IFN-I的产生和炎症反应。鉴于宿主细胞经常遇到核病原体衍生的DNA,因此该研究试图鉴定细胞核内其他未表征的IFN-1引发剂。

hnRNPA2B1的二聚化是其核质转运和活化所必需的
已经鉴定出许多能够识别病毒DNA并诱导IFN-α/β产生的蛋白质,如RNA聚合酶III,IFI16,干扰素调节因子(DAI)的DNA依赖性激活剂,LRRFIP1,LSm14A和环状GMP-AMP(cGAMP)合酶(cGAS) )等。然而,只有细胞质cGAS和DNA-PK在功能上被证实为体内DNA传感器。还报道了几种蛋白质参与DNA病毒诱导的炎症反应,包括黑素瘤2(AIM2),IFI16,Rad50和Sox2等。因此,需要更全面地了解针对DNA病毒的先天免疫应答,尤其是关于将病原体衍生的DNA的核识别与细胞质信号传导的激活联系起来的途径。

hnRNPA2B1是cGAS,IFI16和STING有效的I型干扰素诱导所必需的
在该研究,检查了与单纯疱疹病毒-1(HSV-1)的基因组DNA结合的核蛋白,以及在病毒感染后易位至细胞质。该分析揭示了异质核核糖核蛋白A2B1(hnRNPA2B1)作为限制DNA病毒感染的I型干扰素产生的核启动子。在直接识别核病原体衍生的DNA后,hnRNPA2B1易位至细胞质以启动先天免疫应答。然后,hnRNPA2B1同时促进mRNA的核质转运和细胞质表达,例如CGAS,IFI16和STING mRNA,其扩增抗病毒先天免疫信号。总之,这项研究强烈表明,核DNA传感器如hnRNPA2B1是先天免疫防御的重要贡献者。
参考信息:
https://science.sciencemag.org/content/early/2019/07/17/science.aav0758
来源:Plant_ihuman iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247502941&idx=4&sn=d307aa9d84a059ecff47ba7ef6719f68&chksm=fce6bf82cb913694836ba270acd738d7ea404a236a14430dd7719e34661b78a0e96f9e8682ae&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn


