来源:易科学
2018年诺贝尔生理学或医学奖花落癌症免疫疗法的先驱者美国James P Allison教授和本庶佑教授。其获奖原因是发现了免疫检查点抑制疗法(ICB)。
近几年,使用PD-L1的免疫检查点抑制疗法在临床应用上大放异彩。免疫检查点抗体药物能够激活部分肿瘤患者的免疫效应,显著延长肿瘤患者生存期。
不幸的是,ICB治疗对大多数肿瘤患者的响应率比较低,只有小部分接受治疗的患者对目前的ICB治疗有反应(其占比低于30%)。其中一个重要原因便是肿瘤组织内细胞毒性T淋巴细胞(CTLs)浸润程度低导致免疫耐受。
同时,免疫检查点抗体药物易造成非肿瘤靶向分布(on-target but off-tumor),从而引发严重的免疫相关毒副作用。因此,开发一种切实可行的策略来对抗这种免疫耐受和扩大ICB治疗已成为当务之急。
为了迎接这一挑战,中国科学院上海药物研究所(SIMM)的科学家们开发了一种用于癌症免疫治疗的肿瘤微环境活化抗体纳米颗粒。这项研究发表在《Science Immunology》网络版上。
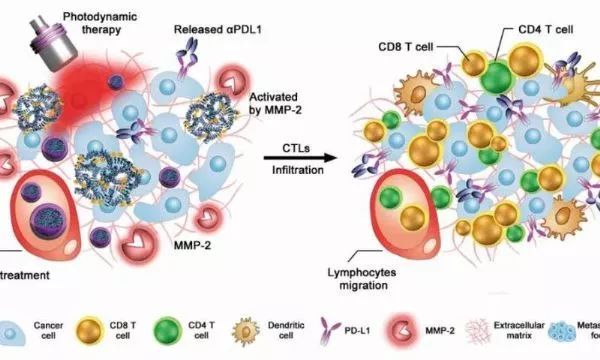
图片来源:Science Immunology
在这项研究中,于海军教授、李亚平教授和他们的同事通过整合anti-PD-L1抗体(αPDL1)和吲哚菁绿(ICG)到一个纳米平台上获得了工程化的抗体纳米颗粒。
ICG是一种经临床批准用于活体手术荧光成像的荧光团,以及用于光动力治疗的光敏剂(PDT)。抗体纳米颗粒可以在血液循环并保持惰性,从而保护αPDL1不与正常组织相互作用。一旦通过增强渗透性和保留(EPR)效应累积在肿瘤部位,抗体纳米粒子被肿瘤特异性的微环境激活,释放αPDL1 来抑制PD-L1。
此外,科学家们还发现,抗体纳米粒通过ICG为基础的PDT效应,触发肿瘤抗原的释放,促进肿瘤内细胞毒性T淋巴细胞(CTLs)的浸润。"这对癌症免疫治疗至关重要,因为CTL已被充分确认为肿瘤细胞的杀手,"该研究的共同通讯作者于教授解释说。
最后,他们发现抗体纳米粒不仅能有效提高BALB/c小鼠的抗肿瘤免疫功能,还能诱导BALB/c小鼠的长期免疫记忆效应,从而导致肿瘤显着消退。
抗体纳米颗粒介导的ICB和PDT联合治疗有效地抑制了荷载4T1乳腺癌的BALB/C小鼠身上肿瘤的生长以及向肺和淋巴结的转移,导致>70%的老鼠生存超过65天,而接受αPDL1治疗的老鼠在42天时全部死亡。
参考资料:
[1] Elegant antibody nanoparticles override immunological tolerance of tumors
[2] Engineering nanoparticles to locally activate T cells in the tumor microenvironment
[3] 上海药物所构建免疫检查点抗体药物递送系统
来源:easysciencenews 易科学
原文链接:http://mp.weixin.qq.com/s?__biz=MjM5ODYzMTMxMw==&mid=2650867002&idx=1&sn=c9912e7a5bf70e423866a78e12e99f33&chksm=bd3267c48a45eed23b86fff786fed860096954547c6fd842ca975afe311bea4fcffbcf687a07&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn