来源:中国科学杂志社
浙江大学申有青教授课题组近期在《中国科学:化学》上发表综述文章,分析体内肿瘤靶向过程。
抗肿瘤纳米药物因能缓解传统小分子化疗药的全身毒性而进入临床应用。但目前研究的多数抗肿瘤纳米药物未能显著提高肿瘤治疗效果, 因而止步于临床前或早期临床研究, 如何显著提高疗效已成为下一代抗肿瘤纳米药物亟需解决的关键问题。
浙江大学申有青教授课题组在《中国科学:化学》上发表综述文章,分析体内肿瘤靶向过程。静脉注射的纳米药物需经过体内血液循环(C)、肿瘤蓄积(A)、肿瘤内渗透(P)、被细胞内吞(I)和在胞内释放(R)五步级联过程(即CAPIR cascade)才能在肿瘤细胞内发挥药效。使纳米药物的纳米特性包括稳定性(stability)、表面性质(surface properties)、尺寸(size)随输送过程各步的要求自主适应(self-adaptive)是纳米药物高效完成输送过程、获得高疗效的关键, 但在肿瘤组织中渗透能力的天然缺失仍是纳米药物的“短板”。
在临床转化方面, 体内安全性评价的复杂性和可控生产的复杂性是功能集成型纳米药物临床转化的瓶颈。同时, 该文还介绍了最近提出的基于剥夺肿瘤信号分子的铜元素、使信号蛋白失活而达到抑瘤效果的新型类分子靶向药物。
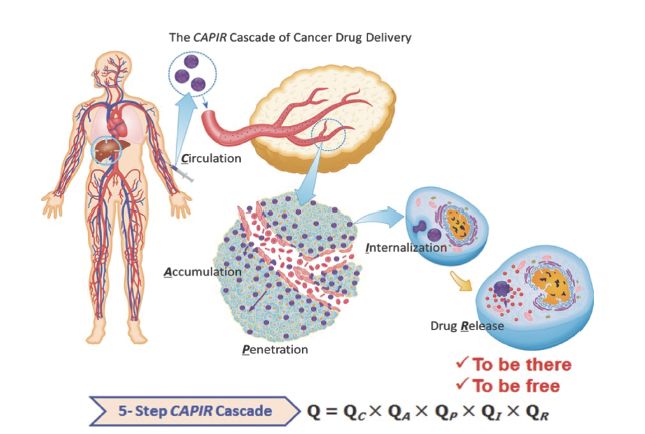
图 肿瘤纳米药物将药物输送至肿瘤细胞内的CAPIR级联输送过程
纳米药物研究的意义和动力来自于临床应用, 与其他药物一样, 安全、有效、可生产是纳米药物临床转化的必要条件。对应于纳米药物, 这就是纳米药物临床转化需具备的CES三要素: C (capability)是指纳米药物在体内输送的3S纳米特性转换能力, 它直接决定纳米药物的疗效(有效性); E (excipientability)是纳米载体的可用于药用辅料的能力, 包括在体内无毒性和免疫原性, 且可被机体完全清除能力; S (scale-up ability)是指纳米药物可建立GMP生产过程、实现稳定规模化生产的能力。
目前已被批准进入临床的纳米药物如多柔比星脂质体(Doxil)、紫杉醇聚合物载药胶束(Genexol-PM)等虽然结构简单、生物相容、生产便利、兼具ES优势, 但载体的功能单一、无法兼顾CAPIR输送的每步过程, 使体内输送效率低(C低下), 导致治疗效果不佳, 限制了这类纳米药物的继续发展。
具备3S纳米特性转换的纳米药物可实现体内高效输送、提高疗效, 然而这类纳米载体往往需要将不同功能的聚合物或材料共同组装成纳米载体, 或者将不同功能的单元键合到一个聚合物主体上, 制备集多功能于一体的纳米载体, 即all functions-into-one (AIO)方法。
然而AIO法制备的纳米药物不可避免地具有复杂的成分及结构, ES能力大大下降: 所含的成分, 甚至其各种代谢产物的体内行为和代谢过程需完全阐明; 而复杂的结构使制备过程的质控指标数大大增加, 建立规模化可控生产过程和GMP过程也变得非常困难, 因此这种纳米药物的成药性降低而所需人力、物力、财力的投入剧增, 使得制药企业对AIO类纳米药物的临床转化尝试望而却步, 因而绝大部分AIO类纳米药物仅局限于临床前研究阶段。
另一方面, 目前报道的大部分多功能纳米药物仍无法克服肿瘤渗透这一“瓶颈”, 疗效仍无法与当下一些新型高效治疗方法(如分子靶向治疗、免疫治疗)相媲美, 甚至仅仅减少毒副作用, 也使临床转化缺乏动力。因此, AIO类纳米药物需解决多功能赋予的有效性与导致的组分和生产过程复杂性之间的矛盾, 同时还要克服肿瘤组织渗透效率低的短板, 进一步提高治疗效果, 是其临床转化的出路。
刘婧, 胡豆豆, 周泉, 申有青. 抗肿瘤纳米药物的设计与挑战. 中国科学: 化学, 2019, DOI: 10.1360/SSC-2019-0026
来源:scichina1950 中国科学杂志社
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQ5MzQyNA==&mid=2656800204&idx=2&sn=253744152dbbc5192b5bfee4a67df7b2&chksm=84a11313b3d69a0587df96ef19f86ab0487d2aace3c795cd9087f59f9a3570bf449828226584&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



