来源:BioArt
肿瘤是一高度异质性疾病,由大多数已分化肿瘤细胞和极少数具自我更新潜能的肿瘤干细胞(Cancer Stem Cells, CSCs)组成。CSCs是对传统治疗具有抵抗的一群处于“静息状态”的细胞,也是肿瘤转移和复发的根源。尽管CSCs在肿瘤进展、转移与耐药中的核心作用已得到认可,但对其精细调控分子机制仍有待进一步深入。
2019年6月28日,Nature Communications在线发表了上海市第一人民医院王红霞团队的研究成果“TSPAN8 promotes cancer cell stemness via activation of sonic Hedgehog signaling”。

Tetraspanins又称作四次跨膜蛋白超家族(TM4SF),由33个家族成员组成,包括TSPAN8、与分化(CD)相关的CD63、CD37、CD53、CD81和CD9等。Tetraspanins家族共同特征是具有四个高度保守的膜跨域,在多种细胞功能中发挥重要生物学调控。越来越多证据表明,TSPAN8调控多种人类肿瘤细胞的迁移、侵袭和转移能力,包括卵巢癌和消化道肿瘤、肝癌、胰腺癌和胶质瘤等,然而其具体分子机制仍不清楚。
王红霞团队近年来一直聚焦四次跨膜蛋白生物学功能调控的多样性及与肿瘤进展的关系开展系列性研究工作。这篇文章报告了前期研究成果:TSPAN8通过与PTCH1相互作用,增强PTCH1与SHH结合、解除PTCH1对SMO的抑制。此外,TSPAN8招募ATXN3去泛素酶来进一步稳定SHH/PTCH1联合复合体、抑制蛋白酶体介导的降解。稳定的SHH/PTCH1促进了GRK2蛋白激酶与SMO的结合,随后SMO磷酸化、SMO发生纤毛易位以及调控下游基因表达的GLI1激活。
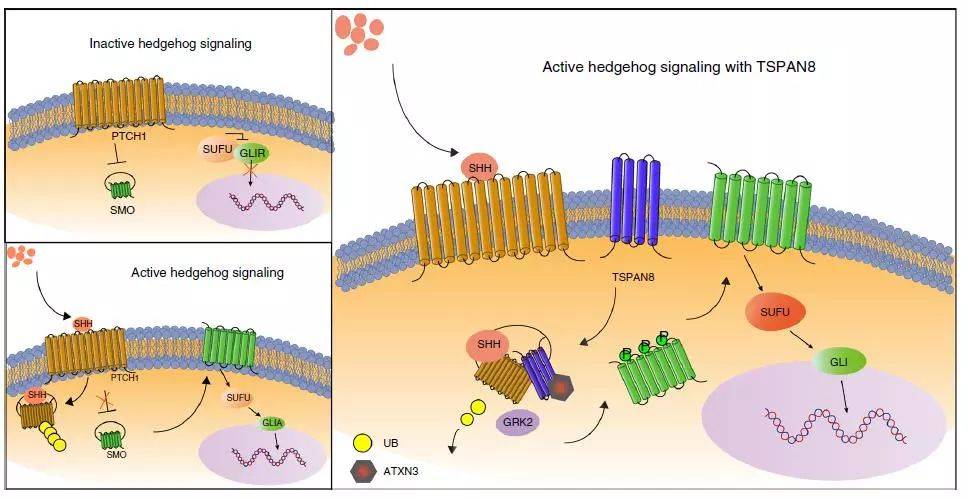
本文发现的主要要点如下:
1) TSPAN8在CSCs中表达上调,与乳腺癌患者治疗抵抗和不良预后相关。
研究者对乳腺癌原代细胞采用三维立体培养富集CSCs和贴壁培养分化细胞并行微阵列分析,显示TSPAN8在CSCs中显著上调。免疫荧光分析揭示TSPAN8和ALDHA1在微球体中一致性过表达。TSPAN8+ 细胞Nanog和Oct4表达增强,干性表型百分比显著增高。TSPAN8过表达显著增强Sox2、Oct4、Nanog和ALDHA1的mRNA和蛋白表达。这些结果均表明TSPAN8表达与肿瘤干细胞表型有关。临床组织标本检测表明TSPAN8在三阴性乳腺癌TNBC中表达显著升高,且与患者总生存时间呈负相关,TSPAN8过表达患者对于新辅助化疗敏感性差,与治疗抵抗相关。
2)TSPAN8通过激活Sonic Hh信号传导参与肿瘤细胞干性维持
研究者在一系列肿瘤细胞株中过表达TSPAN8,发现干性增强,表现为微球体大小和数量增多、集落形成能力增强以及CD44+/CD24-细胞比例增加,并促进细胞对化疗药物阿霉素(ADR)和紫杉醇(PTX)的抵抗性。为评估TSPAN8通过哪一种关键信号途径发挥这一调控作用,研究者在肿瘤细胞中过表达TSPAN8,发现显著增加了PTCH1,GLI,HHIP和SHH(Hh信号通路)mRNA与蛋白表达、SMO磷酸化和GLI1转录活性增高。Hedgehog途径抑制剂Vismodegib和RU-SKI43处理可逆转这一现象。
3)TSPAN8通过募集ATXN3来稳定PTCH1与SHH复合物,进而诱导SMO磷酸化、纤毛易位,调控Sonic Hedgehog信号激活。
免疫共沉淀与GST-pulldown显示TSPAN8直接与PTCH1结合并促进SHH和PTCH1共定位。为明确TSPAN8上调SHH和PTCH1的机制,采用放线菌素D与蛋白质合成抑制剂环己酰亚胺(CHX)处理显示TSPAN8过表达通过延长两种蛋白质的半衰期来稳定PTCH1和SHH表达。这些结果提示TSPAN8可能通过抑制蛋白酶体依赖性降解来增强PTCH1和SHH复合物稳定性。通过免疫沉淀质谱分析,研究者鉴定了ATXN3去泛素化酶能与TSPAN8与PTCH1相互作用;TSPAN8促进ATXN3与PTCH1结合来稳定PTCH1与SHH复合物表达,同时招募GRK2蛋白激酶与SMO的结合和磷酸化,促进SMO纤毛定位。
4)TSPAN8过表达肿瘤形成能力增强。临床上TSPAN8、SHH、PTCH1和ATXN3表达呈正相关性,高ATXN3表达与肿瘤患者不良预后相关。
将患者肿瘤标本中分离的原代肿瘤细胞注射到NOD / SCID小鼠原位接种以进行有限稀释测定,TS+ 细胞比TS- 细胞组小鼠存活时间缩短。与TS细胞(1:873,532)相比,TS +细胞中干细胞比例显著增加(1:10,639)。TSPAN8过表达细胞肿瘤形成能力增强受到ATXN3 shRNA的抑制。
总的来说,本项研究揭示了新的TSPAN8激活Sonic Hedgehog信号通路分子机制,揭示了TSPAN8通过调控肿瘤细胞干性从而促进肿瘤复发转移与耐药的作用机制。
据悉,浙江大学医学院转化医学研究院吕志民教授为本文共同通讯作者。朱容萱和Olivier Gires为共同第一作者。
原文链接:
https://www.nature.com/articles/s41467-019-10739-3
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652471889&idx=3&sn=ac69daa09a94ebc9bbb02fa874c69711&chksm=84e211e5b39598f3cb3ebf84bcc9185ccea798d215e51275b209cacf8bb1d373b228506195c2&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



