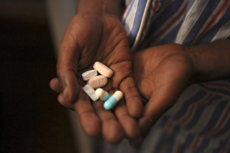
来源:生物谷
大肠杆菌能够合成抗药性蛋白,即便在旨在抑制细胞生长的抗生素存在下,也是如此。这是法国研究人员在一项新的研究中报道的研究结果。他们还发现了这种细菌是如何实现这一壮举的:一种保存完好的膜泵将抗生素从细胞中转运出去---只要足够长的时间就可以让细胞有时间接受来自相邻细胞的编码抗药性蛋白的DNA。相关研究结果发表在2019年5月24日的Science期刊上,论文标题为“Role of AcrAB-TolC multidrug efflux pump in drug-resistance acquisition by plasmid transfer”。 美国东新墨西哥大学微生物学家Manuel Varela(未参与这项新的研究)表示,“这是一个重要的发现。它将有助于解释细菌在遇到抗生素的毒性水平时如何设法传播抗菌素耐药性。”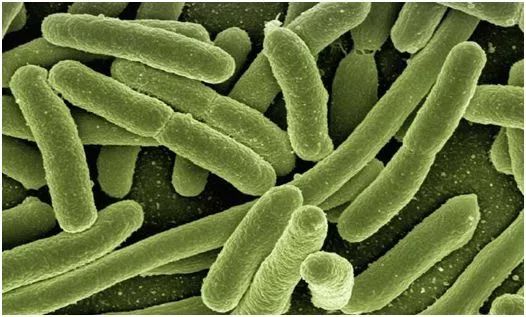
图片来自CC0 Public Domain。
这一发现让论文通讯作者、法国里昂大学细菌遗传学家Christian Lesterlin感到吃惊。他和他的同事们最初开始开发一种实时显微镜系统的项目,以便详细观察质粒转移---细菌细胞彼此分享DNA的过程。通过使用精心设计的荧光蛋白,一旦它们在新的宿主体内表达,他们就能够追踪质粒将编码它们的DNA从供体细胞转移到受体细菌以及所表达的荧光蛋白。他们以大肠杆菌习惯性地分享抗生素耐药基因为例,观察到通过将编码TetA蛋白---一种让细胞对四环素产生耐药性的膜泵---的DNA从细胞中运出,从而将它传递出去。不久之后,他们观察到质粒DNA进入非耐药性细胞中,一段时间后,红色荧光点出现在受者细胞的膜上,这表明TetA蛋白发生表达,而且这些非耐药性细胞对四环素产生抗性。这种抗生素通常用于家畜,但有时也用于治疗肺炎、呼吸道感染和其他疾病,通常会抑制缺乏TetA的细菌的生长,但是通过采用这种机制,许多细菌菌株正在变得具有耐药性。在最初的实验中四环素并不存在,所以为了了解这个过程是如何受到这种药物本身的影响,这些研究人员将细菌细胞暴露在高浓度的四环素中,并再次将它们置于显微镜下。正如所料,这些研究人员观察到质粒DNA进入新的非耐药性细胞中。这是预料之中的,这是因为四环素不会阻碍这一过程。相反,它旨在阻止蛋白合成。令人吃惊的是,他们发现一些新的之前缺乏TetA蛋白的受者细胞中出现红色荧光,这些细胞以前没有TetA蛋白质:显然,尽管暴露于四环素中,它们仍然能够合成包括TetA在内的蛋白。Lesterlin回忆说:“我们花了很多很长时间才证实了这个结果,这非常违反直觉,我们很难确信它确实发生了。”这些研究人员对这些细胞能够做到这一点进行了有根据的猜测:众所周知,许多细菌膜都含有一种称为AcrAB-TolC的多药外排泵,这种泵能够将很多抗生素从细胞中运出,他们认为,在四环素能够阻止蛋白合成和细胞生长之前,这种泵将它从细胞中运出。为了验证这一想法,他们设计了几种突变体,每种突变体在编码组成这种泵的不同蛋白的多个基因中的一个上发生突变。他们发现这些突变体虽然从相邻细胞接受了携带TetA遗传密码的质粒,却不能合成TetA蛋白。在缺乏功能性外排泵的情形下,这些突变体不能将四环素从细胞中运出。随着抗生素水平在细胞内激增,它们不再能够合成蛋白,也就不能生长。这些研究人员表示,当功能正常时,AcrAB-TolC泵将抗生素浓度保持在足够低的水平,为细菌细胞合成质粒DNA中编码的抗性蛋白赢取了时间。在这种情况下,它允许TetA蛋白产生,随后将更多的四环素从细胞运出。最终,细菌可以在抗生素的存在下具有耐药性。正如Lesterlin所说,“对细菌来说,这是比人类健康更好的消息。”美国科罗拉多大学博尔德分校化学工程师和微生物学家Anushree Chatterjee(未参与这项新的研究)指出,“多药外排泵AcrAB-TolC在这个领域早已广为人所知。”不过,她说,事实上,它有助于细菌在接触抗生素的同时获得抗药性,这一消息是新闻。看到细菌能做这么多事情总是令人关注的。”她说,这些发现具有广泛的影响,这是因为AcrAB-TolC在细菌中是非常保存的,而且这种其机制并不仅限于四环素。 Lesterlin和他的同事们证明这种泵还允许细菌在其他的抑制基因表达的抗生素---比如,抑制翻译的氯霉素和抑制转录的利福平---存在的情况下合成抗药性蛋白。 Lesterlin补充说,这种机制与所谓的不会杀死仅能抑制细菌生长的抑菌抗生素(bacteriostatic antibiotics)有关。他猜测这也将适用于在细菌产生耐药性之前直接将它们破坏的溶菌抗生素(bacteriolytic antibiotics)。Chatterjee和Varela都对这项新研究进行了深入研究,其研究结果非常可靠,Varela对Lesterlin团队开发的技术印象特别深刻,这种技术可以在观察TetA蛋白合成的同时观察质粒DNA在细胞之间的转移。 Varela补充道,“这些作者还阐明了可作为开发新型抗菌试剂的新靶点的关键细菌机制。”比如,人们可能通过靶向AcrAB-TolC泵来制造抗生素---一些实验室正在研究这种方法。或者,人们可能能够靶向调节它产生的基因---这个角度吸引了Chatterjee。传统的抗生素设计方法在很大程度上依赖于靶向特定蛋白的小分子,而且对其中的许多小分子而言,细菌已经见过很多年了,最终选择了更多的耐药机制。Chatterjee说,“我们需要研究非传统的途径。允许细胞应对这些应激情况的调节机制是什么?我认为靶向这些过程似乎,有助于开发从一开始就有望阻止耐药性产生的更智能疗法。”
原始出处:Sophie Nolivos et al. Role of AcrAB-TolC multidrug efflux pump in drug-resistance acquisition by plasmid transfer. Science, 2019, doi:10.1126/science.aav6390.
Vanessa R. Povolo et al. Disseminating antibiotic resistance during treatment. Science, 2019, doi:10.1126/science.aax6620.
来源:BIOONNEWS 生物谷
原文链接:http://mp.weixin.qq.com/s?__biz=MzI2NjY1NjA5Mw==&mid=2247501983&idx=3&sn=692f0d687984e1bf5026230a21c2a23b&chksm=ea8848adddffc1bbfc91c41e0b9df8f1befc04db56c1c33f0ae9bd893b70ce1e43c31d1b83ba&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn