来源:医药魔方
用“双特异性抗体领域的开拓者”来形容吴辰冰并不过分。十年前,国际性专业杂志《制药科技》(PharmaceuticalTechnology)公布的《2009年度创新荣誉奖》中,由吴辰冰发明的“双变域免疫球蛋白(DVD-Ig)大分子制药技术”入围,获奖词是「全球制药领域近期5项重大科技成就之一」。吴辰冰是第一位入围该榜单的华裔科学家。

岸迈生物创始人兼首席执行官吴辰冰博士
这是制药行业对他于2007年首次在《自然•生物技术》(Nature Biotechnology)公布DVD-Ig技术的认可。论文发表后迅速获得关注,有权威专家点评「这项技术可用于开发同时抑制多种致病因子的新一代高效生物医药产品,为新药研究领域开启了一扇大门,为生物制药技术搭建了全新平台。」
相比于单克隆抗体开发,同样起步于上世纪80年代的双特异性抗体技术,由于研发壁垒更高,其获批上市的药物远远少于单抗。截止目前,FDA仅批准了2个双特异性抗体,进入Ⅲ期临床试验的项目亦是凤毛麟角(见:双特异性抗体热潮)。
吴辰冰进入“双特异性抗体领域”的契机起步于艾伯维(原雅培公司生物制药部)。众所周知,艾伯维开发出了全球最畅销的单克隆抗体药物修美乐(阿达木单抗)。21世纪初就已经在艾伯维担任研发科学家的吴辰冰有机会投入炙手可热的单抗研究领域。
当年在艾伯维内部有个公认较高挑战的项目,即“如何将针对多种不同靶标的抗体的氨基酸序列组合到一起”。众多科学家前赴后继,最后都折戟在该技术上。吴辰冰通过了长达5年的研究,终于在2007年发表首篇“双特异性抗体”的技术论文,引起了众多制药巨头对这个领域的关注。
吴辰冰对“双特异性抗体”的研究走在国际前端。距离吴辰冰论文发表两年之后,全球批准第一个双特异性抗体药物 Removab(catumaxomab)。罗氏的双特异性抗体平台CrossMAb亦是到了2010年才首次公开,比吴辰冰的研究晚了3年。
4月23日,美国专利商标局(USPTO)授权岸迈生物在美国申请的专利号10,266,608标题为“串联Fabs免疫球蛋白及其用途”的专利。这是该公司最早在全球范围内申请的核心平台技术专利,获得授权的权利要求组成中,广泛涵盖和保护了通过其独有平台技术获得的双特异性抗体。
1
举家回国的初心
2008年,国家“千人计划”向海外科学家伸出了橄榄枝,许多在海外从事药品研发的科学家怀着忐忑如候鸟般回到了祖国的怀抱。但吴辰冰不是只身回来,而是全家在2010年一起回到国内长期定居。
吴辰冰在接受医药魔方记者采访时表示,当时回国的决心和信念都很坚定,主要是想把开发双特异性抗体的理念带到中国,并在中国开发出真正的创新双特异性抗体药物。从当时海归科学家的专业背景来看,以从事工艺、生产等偏下游CMC居多。吴辰冰是当时少数从事抗体药物早期研发的海归科学家。
吴辰冰回国后第一份工作是在睿智化学担任生物制药部门负责人,帮助睿智化学从零开始搭建了生物技术团队。谈及这份经历,吴辰冰回忆道,“早期我进入睿智化学的时候,国内做抗体研发的海归并不多,而是做生产工艺的较多,研发的人很少。这给了我们一个快速发展并与多个国内药企进行创新抗体项目合作的机会。
3年后,吴辰冰被中信国健聘请,出任CSO兼研究院院长。在中信国健,他不仅主导研究了多个单克隆抗体的项目,还见证了中国首个抗体类药物益赛普(注射用重组人II型肿瘤坏死因子受体-抗体融合蛋白)不断获得市场认可的发展过程。
从产品立项到临床研究到扩大生产甚至是上市后管理,吴辰冰对药品“研产销”的链条几乎全摸索了一遍。当三生制药收购中信国健之后,吴辰冰面临两个决策。要么留下来或接受猎头们递来的职业经理人邀请,要么从头开始创业。
如果从追求稳定、安逸的角度来考虑,多数人会考虑选择前者,毕竟后者面临的荆棘和不确定性更多。但想到自己回国的初衷,吴辰冰做出了少数人的选择,在他看来困难的道路往往离实现理想相对更近。
2
重回双抗赛道
2016年2月,上海岸迈生物(EpimAb)在张江注册成立。Epi是希腊词头,释义“连接,在……之上”;mAb是单克隆抗体(monoclonal antibody)的缩写,并常作为抗体药物通用名的尾缀。吴辰冰告诉记者,EpimAb的寓意很简单,就是“连接于单抗,但又超出单抗”,这亦是岸迈核心技术的准确诠释。
彼时制药界研发潮流风起云涌此起彼伏,PD-1/PD-L1、细胞疗法、基因疗法……你追我赶,好不热闹。如此燥热的研发环境下,吴辰冰仍然孜孜不倦地坚守在双特异性抗体领域。
幸运的是,在老朋友老同事以及投资者的支持下,岸迈生物小心翼翼地避开了双特异性抗体领域的一个又一个“坑”。这些“坑”亦是导致双特异性抗体的发展明显滞后于治疗性单克隆抗体的主要原因,比如以下几点:
早期双特异性抗体表达困难,稳定性差,生产工艺复杂;
早期研发成本明显高于单克隆抗体。以emicizumab为例,Chugai的科学家们是在筛选了4万个不同双特异性抗体分子后才确定了成药分子,这当中的付出与坚持恐怕不是一般企业能做得到的;
双特异性抗体涉到靶点生物学、结构生物学、抗体工程、筛选策略,一般只有具备相当实力的公司才敢涉足也才有可能取得成功。
从公司初建的第一位员工到2017年的20多人,岸迈眼下已经有接近50名员工。对比跨国药企动辄数十人甚至几百人的事业部,岸迈的团队规模似乎不足一提。但是如此精湛的团队,其在短短三年间所取得的成效,却是令同行惊叹的。
从该公司陈列墙上摆满的奖杯,不难发现其研发能力得到了政府部门认可;得到了创新界认可,曾多次获得创新医疗大奖;也得到了资本界的认可,并成功完成多次融资,保证了创新研发和临床项目的顺利进行。
3
“三驾马车”发力
之所以能取得如此多成果,用吴辰冰的话说,岸迈正乘着“三驾马车”快速前进。
--形成具有国际知识产权的双抗平台
首先是基于他过往十几年对双特异性抗体技术的关注和积累,吴辰冰携团队开发了全新的双特异性抗体的技术平台FIT-Ig。这是一款IgG-like双特异性抗体平台,能够通过简单的分子生物学手段将两个抗体串联在一起形成双抗。
吴辰冰坦言,与CrossMab(罗氏)、DVD-Ig(艾伯维)、DuoBody (Genmab)、FcAb(F-star)等双特异性抗体平台相比,FIT-Ig具备“2+2”结构域数量,没有空间位阻,也不要突变、肽链和纯化后修饰,更没有改变Fab结构。换句话说,通过FIT-Ig开发的双抗,不仅解决了错配问题,还提高了成药性。
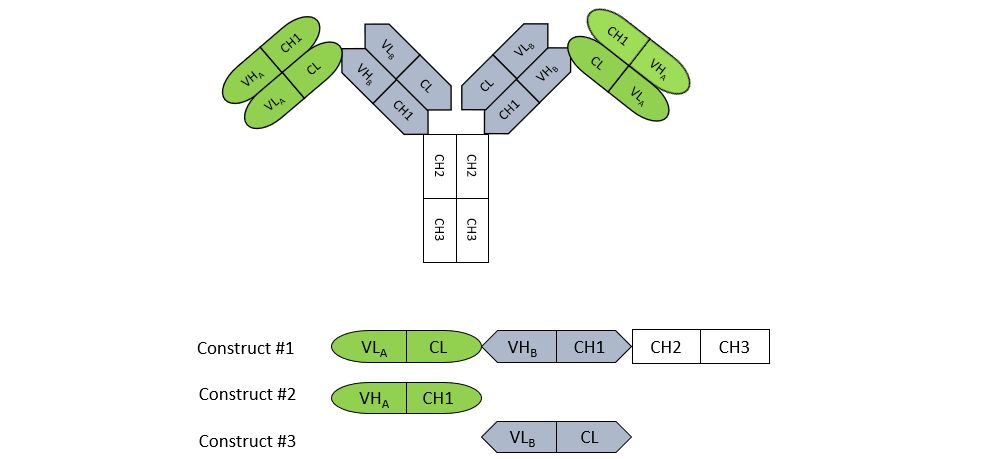
FIT-Ig平台结构原型图(岸迈生物供图)
当记者提出“为何不直接将两种靶向药物联用或者在肿瘤免疫基础上建立combo?”的疑惑时,吴辰冰说,通过该技术构建的双抗,除了具备两个原始抗体的功能,同时兼具区别于现有药物联用不具备的协同效应,拥有双重活性和产业化优势。最重要的是,倘若产业化落地,还有望大幅降低患者的治疗费用。
据吴辰冰介绍,目前真正有自己的专利保护技术的企业为数不多,如基因泰克、安进、艾伯维等,其他多数通过收购或专利授权获得。“这个行业技术壁垒很高,专利保护也很严密,如果没有自己的技术,或者没有获得技术的使用权,就没办法开发双抗。”他向记者透露,岸迈的FIT-Ig具有独家知识产权,并进行了PCT专利申请。就在这个月,该技术获得了美国专利商标局(USPTO)的授权。
--多元模式拓展平台技术的合作
手握FIT-Ig专利技术的岸迈也吸引了国内外多个主流生物医药企业的关注。成立伊始,信达生物对FIT-Ig技术进行了周密评估,最终决定以1.2亿美元的技术授权费用,获得岸迈专有双特异性抗体技术的使用权。
2016年10月,岸迈与英国生物制药公司Kymab达成了一项技术协议。岸迈的FIT-Ig双特异性抗体技术与Kymab的Kymouse全人源抗体技术进行互相授权及合作,进行针对肿瘤免疫领域的原创性双特异性抗体的开发。
2018年4月,浙江特瑞思药业以预付加里程碑付款形式,以2100万美元的总额获得岸迈双抗项目FIT012/TRS008的中国市场开发权益。岸迈不仅保留了该项目除中国以外的全球商业权益,也可使用特瑞思提供的产品数据在中国以外地区的产品开发或授权,同时倘若产品在中国成功上市,岸迈还将获得一定比例的销售提成。
简而言之,岸迈通过技术授权、合作开发、共享收益等多种形式与多家家企业达成了技术与产品的合作。
--建立明显差异的双抗管线
吴辰冰告诉记者,以肿瘤适应症为例。当前的开发方向主要分为以CD3为核心的新一代T细胞导向治疗,针对肿瘤双靶点(如c-MET和EGFR)信号通路阻断的新一代靶向治疗以及针对PD-1/PD-L1等免疫检查点的肿瘤免疫疗法这三大类。
而岸迈的产品立项主要基于三点原则:管线具有明显差异性,针对协同机制的特异靶点,能够满足重大临床需求的适应症。
循着这三点原则检索,岸迈从默沙东K药获批肺癌一线治疗的适应症中找到了些许立项灵感。K药用于肺癌一线治疗的要求是患者PD-L1的表达量要高于50%且没有EGFR突变。而在中国,非小细胞肺癌患者中有50~60%的病人发生EGFR突变。产生EGFR突变的患者,在使用酪氨酸激酶抑制剂治疗一段时间后,会产生耐药性。吴辰冰判断,由于耐药产生通路的多元化,多通路共同抑制可能是使肿瘤治疗成为慢病化管理的发展趋势。
因此岸迈第一个产品EMB01是针对EGFR和C-MET靶点的非小细胞肺癌适应症的双特异性抗体,已经实现中美双报并获批临床。这个项目也受到了国际著名肺癌临床专家/中国肺癌靶向治疗的领军人物的关注,吴一龙教授听完吴辰冰的项目介绍后,便欣然同意担任该项目的全球PI,展开国际多中心临床试验研究。
岸迈的另一个核心产品是基于肿瘤免疫机制的EMB02产品,也是具有双靶点的创新协同机制。同时,在新一代T细胞导向治疗机制方面,吴辰冰告诉记者,“岸迈生物在前期打下来扎实的基础,针对这个领域常见的一些问题,比如安全性、如何突破实体瘤等等,都进行了相应的产品策略的布局,后续会逐步推向临床开发。”
吴辰冰表示,岸迈生物计划在2019年年底完成EMB01项目Ⅰ期临床试验,并希望获得FDA的突破性疗法认证。顺利的话,等再过两年取得不错的Ⅱ期临床数据时,岸迈生物将申请EMB01有条件批准上市。
后记
吴辰冰给人的感觉与传统企业家不同。谈及商业模式,他的反应比较理性,只是简单地描述岸迈与国外的生物科技公司发展轨迹相似。而每当提到科学问题时,他的情绪立刻变得很激动,面部表情也丰富起来,甚至是手舞足蹈地展示起他的技术,犹如孩子一般兴奋。他坦言,比起管人,他更喜欢管理项目。他对岸迈当下的企业文化定位主要是两点——公司以创新为导向,项目以科学为基石。
几年前,记者曾常在各种行业会议上见到吴辰冰的身影。他犹如布道者一般,耐心地向与会者解释双特异性抗体技术的优势。然而当时的参会者眼光多聚集在肿瘤免疫、细胞治疗领域。或许因为相信,所以坚持,吴辰冰对双抗领域的执着获得了医学界大咖的认可。
我们无法预测他们最终能否成功,但当国内双特异性抗体研究热到来之际,岸迈已悄然布局多时,并进入了该领域第一梯队的实力是不容小觑的。在此祝福这位科学家出身的创业者早日圆梦。
来源:ppsyxjz 药学进展
原文链接:http://mp.weixin.qq.com/s?__biz=MzA5MDY3ODExNQ==&mid=2651305489&idx=3&sn=ad81c7d260669e24f5f9665281d31ce3&chksm=8bf4e01dbc83690b54042d7b78b93c1ab9d086f7110b515879af67fde08cae675a0a592774ee&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



