来源:BioArt
在动物界中,像表皮,口腔上皮和小肠上皮这样的屏障组织(barrier tissue)是用来帮助生物体抵抗外界伤害,防止有害病原体入侵的第一道防线。同时,这些组织也会长期接触到外界对生物体无害的抗原,比如共生菌,食物蛋白等,所以它们也需要建立对这些无害抗原的免疫耐受(immune tolerance)以防止过度免疫反应导致的自身免疫疾病。构成这些组织的主要细胞类型除了结构性的角质细胞和上皮细胞外,还有很多免疫细胞。这些免疫细胞包括先天免疫细胞:驻留巨噬细胞(Tissue-Resident Macrophage)、树突细胞(Dendritic Cell)和后天免疫细胞:T细胞与 B细胞等 【1】。这些免疫细胞的种类和功能是非常多样的,他们需要相互协同作用,从而达到在生理状况和病理状况下都能维持屏障组织的稳态的目的。
从发育角度来看,以表皮为例,组成表皮组织的绝大多数细胞——角质细胞 (keratinocyte)是来源于外胚层的。而人们传统上认为表皮组织内的免疫细胞,包括驻留巨噬细胞(也称作朗氏细胞,Langerhans Cell),是来源于血液(中胚层)的。然而,由于小鼠胚胎体内发育无法在空间上进行精确标记加上传统的Cre-LoxP标记方法效率较低,其相关研究中对于表皮组织内驻留巨噬细胞 (朗氏细胞)的来源是有争议且不全面的【2】。
近日,香港科技大学温子龙课题组利用斑马鱼模型的优势弥补了小鼠模型研究中的不足,首次在斑马鱼的表皮中发现了一类新型的来源于外胚层的免疫细胞,并将其命名为介递细胞(metaphocyte)。这类新型的细胞在基因表达谱和细胞形态上都和传统的来源于中胚层的朗氏细胞很相似,但它的功能是通过穿越表皮细胞间隙的触手来获取外界环境中的可溶性抗原 (soluble antigen)。携带这些可溶性抗原的介递细胞会凋亡(apoptosis),而朗氏细胞可以通过吞噬(phagocytosis)介递细胞的凋亡小体来获取这些可溶性抗原。这项研究以An Ectoderm-Derived Myeloid-like Cell Population Functions as Antigen Transporters for Langerhans Cells in Zebrafish Epidermis为题在线发表在Developmental Cell杂志上。

研究人员首先通过时间和空间上可控的定点标记方法,在成年斑马鱼表皮上发现了两种不一样的免疫细胞:传统的血液(中胚层)来源的朗氏细胞,和一种新型的非血液来源的类髓系细胞(myeloid-like cell)。运用转录组测序技术等方法,研究人员发现这种新型非血液来源的细胞和传统的朗氏细胞在基因表达水平和细胞形态等方面是高度相似的。接下来,通过细胞移植和谱系追踪的方法,研究人员证明了这类细胞和角质细胞一样,是从外胚层发育来的。所以在斑马鱼的表皮中存在两种来源不同的免疫细胞:传统中胚层来源的朗氏细胞,以及新型外胚层来源的介递细胞(图1)。那么这两种细胞的功能有什么不同呢?
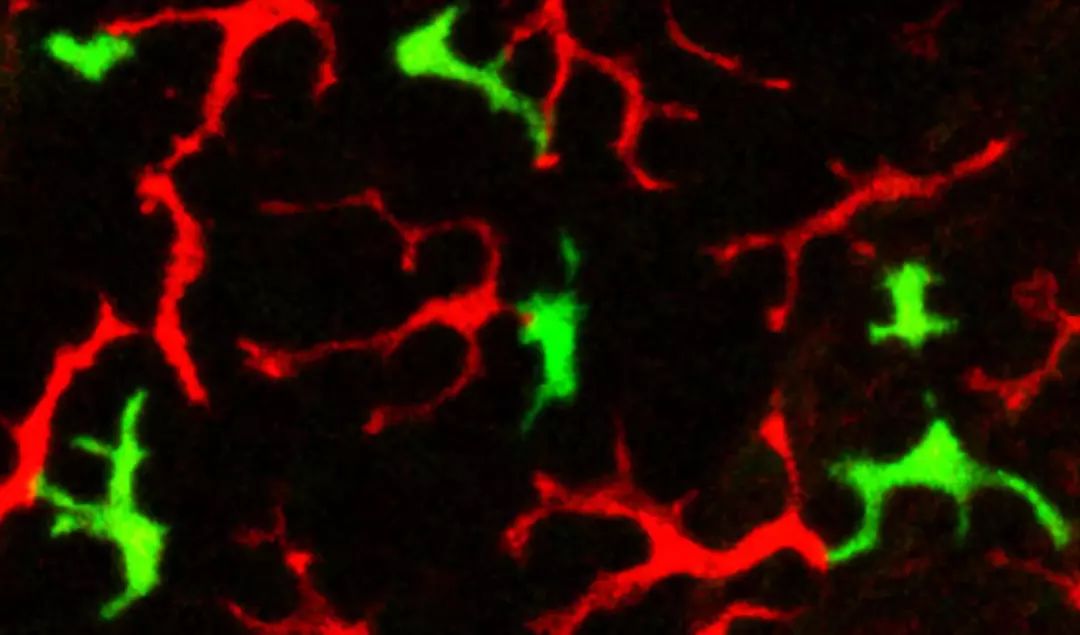
图1. 红色为朗氏细胞,绿色为介递细胞
接下来,研究人员针对这两种细胞进行了功能性的研究。令人意外的是,尽管介递细胞和朗氏细胞高度相似,但他们的功能却是完全不同的。转录组测序结果显示,和朗氏细胞相比,介递细胞的吞噬作用(phagocytosis)相关受体表达量相对较低,所以介递细胞不能像朗氏细胞那样清理因组织损伤而死掉的角质细胞以及入侵的细菌等。但有意思的是,与朗氏细胞相比,介递细胞高表达紧密连接(tight junction)相关的基因,可以形成穿越皮肤最表层角质细胞的触手 (transepithelial protrusion-TEP) ,从而直接获取外界环境中的可溶性抗原。然而传统的朗氏细胞并没有这样的能力。研究人员还发现,这些携带可溶性抗原的介递细胞会凋亡,而朗氏细胞可以通过吞噬介递细胞的凋亡小体来获取这些可溶性抗原。总结来说,外胚层来源的介递细胞的功能是将外界环境中的抗原通过凋亡-吞噬的方式传递给血液来源的朗氏细胞(图2),所以研究人员将这种新型的细胞命名为介递细胞(介导抗原传递的细胞)。
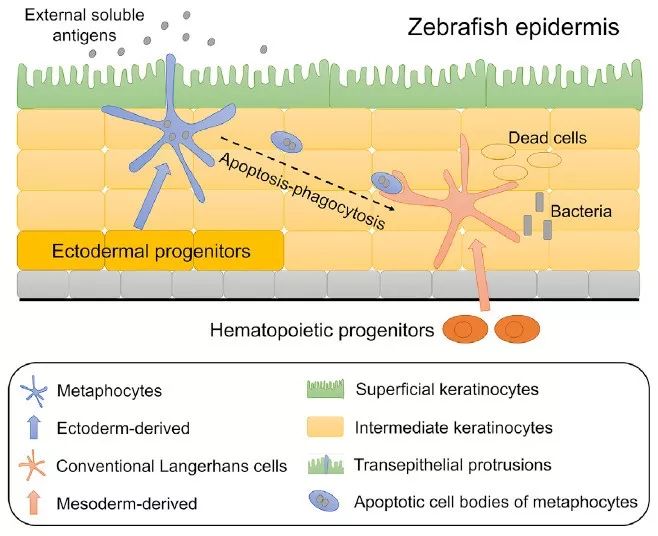
图2. 介递细胞和朗氏细胞的功能
传统观点认为免疫细胞都是来源于血液(中胚层)的,这项研究挑战了这一传统观点,首次发现了在斑马鱼表皮中存在一种外胚层来源的介递细胞,揭示了在屏障组织内免疫细胞来源与功能的多样性和特异性,同时打开了对于非血液来源的免疫细胞研究的大门,为与屏障组织相关的免疫疾病研究奠定了基础。
BioArt,一心关注生命科学,只为分享更多有种、有趣、有料的信息。关注请长按上方二维码。投稿、合作、转载授权事宜请联系微信ID:bioartbusiness 或邮箱:sinobioart@bioart.com.cn。原创内容,未经授权,禁止转载到其它平台。
来源:BioGossip BioArt
原文链接:http://mp.weixin.qq.com/s?__biz=MzA3MzQyNjY1MQ==&mid=2652469285&idx=3&sn=fa02ee4f204dbe5c26ea57a5d612c257&chksm=84e2eb91b3956287b1511a319422e80e1211e32542e450bf584daa1302c25409e7946e881bdb&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn