来源:iNature
ROS是活性化学物质,对许多生物过程至关重要,如细胞增殖,分化和迁移。由于致癌刺激,线粒体功能障碍和癌症的代谢活动增加,大多数癌细胞与正常细胞相比,ROS不断产生~10倍的ROS水平,因此基于内源性ROS的各种刺激响应性药物递送系统被开发以实现随需应变靶向病变部位的药物输送。然而,短寿命(<0.1 ms),有限的扩散和作用范围(10~20 nm)以及内源性ROS的细胞内水平相对不足常常会影响治疗效率。在线粒体中产生约90%的细胞内ROS,其是超氧化物自由基的主要来源,其是大多数ROS物种的前体,而一些其他ROS物种也是线粒体中呼吸链的不可避免的副产物。此外,过量的ROS会损害脂质,蛋白质和DNA,这与线粒体功能的变化有关。大量证据表明线粒体在细胞能量代谢和凋亡细胞死亡中发挥重要作用。
2019年4月12日,华南师范大学邢达、胡祥龙团队发表题为“Mitochondria-specific drug release and reactive oxygen species burst induced by polyprodrug nanoreactorscan enhance chemotherapy”的文章。在该研究中,多聚物药物纳米反应器诱导的线粒体特异性药物有望在线粒体中原位产生高剂量的ROS,这可以破坏线粒体并激活程序性细胞死亡,从而增强癌症治疗的治疗效果。

研究人员开发了具有癌症细胞和线粒体双靶向特性的ROS响应性多前药纳米反应器,证明了线粒体药物释放和mtROS爆发的自我循环,用于增强癌症化学动力学治疗。选择喜树碱(CPT)作为模型线粒体药物,除了一般抑制DNA拓扑异构酶I用于癌症治疗外,它还可以作为细胞呼吸抑制剂来刺激内源性mtROS产生和线粒体超极化。首先,制备具有硫代缩酮键CPTSM的ROS响应性CPT前药单体,然后制备靶向癌症的多前药两亲物,cRGD-PDMA-b-PCPTSM和线粒体靶向药物TPP-PDMA-b-PCPTSM,包括亲水性聚(二甲基丙烯酰胺)(PDMA)和PCPTSM的疏水聚合前药嵌段,分别用三苯基鏻(TPP)或环状Arg-Gly-Asp(cRGD)肽进一步修饰。
双靶向多药物纳米颗粒(DT-PN)由其水性共组装制成。在主动靶向线粒体后,癌细胞中内源性上调的mtROS可诱导线粒体中的初始游离CPT释放。原位释放的CPT进一步触发mtROS的循环增加,实现随后的高剂量CPT释放和最终mtROS爆发的扩增,这有利于长期高氧化应激以有效消除癌细胞。 ROS水平的定量评估在多个水平进行,包括原位线粒体超氧化物,细胞内总ROS和肿瘤内小鼠肿瘤内ROS。
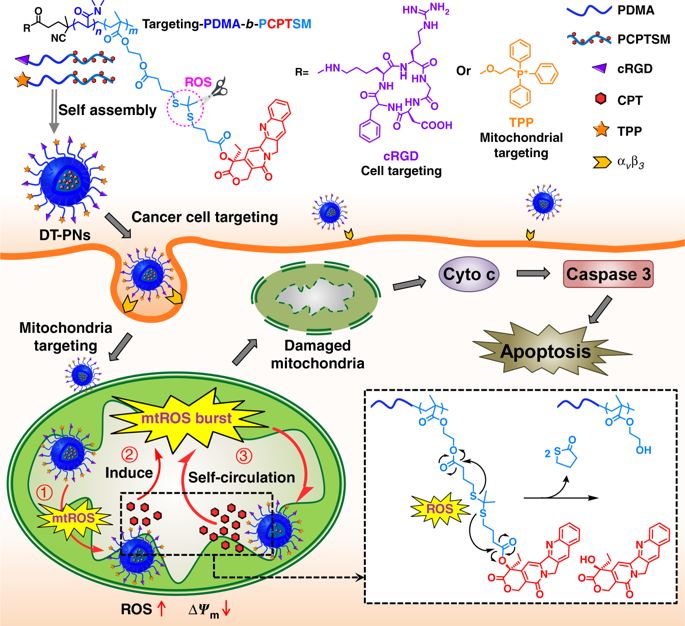
线粒体特异性多前药用于自我循环药物释放与ROS爆发
与正常细胞相比,癌细胞表现出略微升高的活性氧(ROS)水平,并且在线粒体中产生约90%的细胞内ROS。原位线粒体ROS扩增是增强癌症治疗的有前途的策略。在该研究中,研究人员报告癌细胞和线粒体双靶向纳米反应器(DT-PN)与高含量的CPT单元,其在内源性线粒体ROS(mtROS)存在下释放初始游离CPT。原位释放的CPT充当细胞呼吸抑制剂,诱导mtROS上调,从而实现CPT释放和mtROS爆发的后续自我循环。这种mtROS扩增赋予长期高氧化应激以诱导癌细胞凋亡。目前用于增强化学动力学疗法的内源激活mtROS扩增的策略克服了ROS的短寿命和作用范围,避免了外源性光在光动力疗法中的渗透限制,并且对于治疗诊断具有前景。
来源:Plant_ihuman iNature
原文链接:http://mp.weixin.qq.com/s?__biz=MzU3MTE3MjUyOA==&mid=2247500409&idx=7&sn=de17d2006a01a6c71638089541cfba6b&chksm=fce6b1a6cb9138b061ce038da16e0c4fc7077ff501c66bde4b903e92cebab39bf52c78d57a12&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn


