来源:X-MOL(x-mol.com)
注:文末有研究团队简介 及本文作者科研思路分析
近日,中国科学院长春应用化学研究所的彭章泉团队通过原位表面增强拉曼光谱(SERS)和微分电化学质谱(DEMS)技术,研究了微量O2存在条件下Li-CO2电池放电产物Li2CO3的形成机制,这一研究有助于理解此领域一直饱受争议的基础科学问题。
虽然Li-CO2电池作为新型储能器件近年来备受关注,但是在工作过程中至少存在两个悬而未决的基础科学问题:(1)常温、无催化剂条件下CO2十分稳定,能否在电解液稳定窗口内被电化学还原;(2)如果可以,反应机理是什么,影响因素(电极材料/催化剂、电解液等)又是什么。对于第一个科学问题,目前存在三个观点:(1)CO2在电解液稳定窗口内不能还原,但是引入微量O2可以大幅度提升Li-CO2的放电容量;(2)CO2在合适电催化剂条件下可以还原;(3)CO2在碳材料表面(比如商业化的Super P和KB碳等)也可还原。
针对第一个科学问题,彭章泉团队通过原位光/质谱技术解析了无催化剂条件下,电极表面Li2CO3的形成机制。研究结果表明,在DMSO(高DN溶剂)中,包含一个主要的溶液相“电化学”机理(以-OC(=O)OC(=O)OO-为反应中间体)和一个次要的溶液相表面机制(以-OC(=O)OOC(=O)O-为反应中间体);而在CH3CN(低DN溶剂)中,主要发生表面相“化学”反应机制,即氧还原反应在电极表面首先生成Li2O2,接着Li2O2与来自溶液中的CO2发生化学反应生成Li2CO3,具体反应路径如图1所示。其中,微量O2扮演“准催化剂”的角色固定CO2,特别是在高DN溶剂中,溶液相“电化学”机制能够极大改善Li-CO2电池放电的容量。值得注意的是,Li-CO2电池仅检测到Li2CO3一种最终放电产物,极大可能是微量O2在电池中起关键作用,而CO2本身并没有还原。
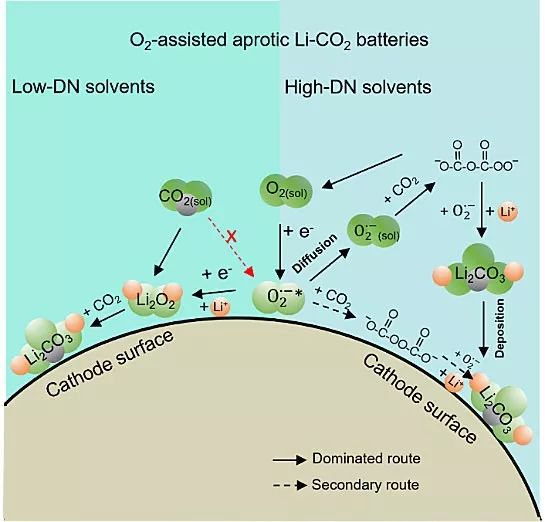
图1. 氧气存在条件下Li-CO2电池的放电原理示意图
该研究工作加深了人们对Li-CO2电池放电过程的认识,对反应路径调节、电解液设计等具有重要的理论指导意义。这一成果近期发表在The Journal of Physical Chemical Letter 上,文章的第一作者是中科院长春应用化学研究所的博士研究生赵志伟。
该论文作者为:Zhiwei Zhao, Yuwei Su and Zhangquan Peng
原文(扫描或长按二维码,识别后直达原文页面):

Probing Lithium Carbonate Formation in Trace-O2-Assisted Aprotic Li-CO2 Batteries Using in Situ Surface-Enhanced Raman Spectroscopy
J. Phys. Chem. Lett., 2019, 10, 322, DOI: 10.1021/acs.jpclett.8b03272
彭章泉研究员简介

彭章泉,1997年7月本科毕业于武汉大学,2000年7月和2003年12月在中科院长春应用化学研究所分别获硕士和博士学位;2004年4月至2006年1月在德国杜塞尔多夫大学物理化学研究所从事博士后研究(超快光谱电化学),2006年1月至2007年11月在丹麦奥尔胡斯大学化学系从事博士后研究(自由基电化学),2007年11月至2012年4月在英国圣安德鲁大学从事博士后研究(固态电化学);2012年4月至今任中科院长春应化研究所研究员。
研究方向:(1) 现场光谱/质谱电化学,(2) 锂-离子/锂-氧气电池。
成果和荣誉:已在Science、Nat. Mater.、Nat. Chem.、Nat. Commun.、Angew. Chem. Int. Ed.、J. Am. Chem. Soc. 等刊物发表SCI论文50余篇,论文被SCI期刊引用超过5000次,获国家杰出青年科学基金(2018)、英国牛顿学者(2018)、德国洪堡学者(2004)。
https://www.x-mol.com/university/faculty/15770
第一作者简介

赵志伟,1993年生,2016年至今在中科院长春应用化学研究所电分析化学国家重点实验室(彭章泉研究员课题组)攻读博士学位,研究方向:现场光/质谱电化学研究金属空气电池电极|电解液界面。
科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:目前在Li-CO2电池领域,已报道的文章侧重点基本都在材料合成方面,对电池工作的基本原理知之甚少。反应机制的不清晰不仅对正极材料/催化剂和电解液的理性设计等带来了诸多困难,也引发相当大的争议。最具争议性的话题是:无催化剂时,Li-CO2电池是否可以放电;如果可以,放电机制/影响因素是什么。这个充满争议性的话题结合我们课题组在研究能源电化学界面的丰富经验,使得我们对Li-CO2电池中Li2CO3形成的机制展开研究。目前,这项研究解决了无催化剂条件下Li-CO2电池的放电机制,未来的研究重点更多会放在催化剂在Li-CO2电池中的角色。
Q:研究中过程遇到哪些挑战?
A:该研究中最大的挑战在于原位检测反应中间体。众所周知,电化学反应产生的中间体存在时间往往很短暂,这就需要不断优化电化学实验条件,尽可能捕捉中间体的谱学信号。在这个过程中,我们团队在原位拉曼分析方面的研究经验积累起到了至关重要的作用。此外,Li-CO2电池需要更多原位表征技术去研究界面反应的机制,希望相关领域的研究者可以开展合作,促进Li-CO2电池技术向前发展。
来源:X-molNews X一MOL资讯
原文链接:http://mp.weixin.qq.com/s?__biz=MzAwOTExNzg4Nw==&mid=2657608233&idx=8&sn=ac1cc637e4aeb5dead93005c398effa3&chksm=80f7cbf9b78042ef5aba8ebb29082c71d02ccbcec0242210d025dacfeb05c9ce3a362626182e&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



