来源:高分子科学前沿
细菌会黏附在表面,形成一层生物膜,阻碍抗菌剂和宿主免疫细胞的渗透。同时,随着抗生素的使用,许多病原体进化出耐药性,给公共健康带来了更大的威胁。而新药发展的速度跟不上病原体产生耐药性的速度,因此,很有必要在原有抗生素的基础上开发新策略对抗病原体。
虽然生物膜在宿主体内的传播会造成感染性细菌的传播,但不妨碍它成为替代/替补抗生素治疗的新策略,因为一旦分散在血液循环中,悬浮的细菌比在生物膜上生长的细菌更容易受到宿主免疫细胞的影响,对抗生素的敏感性也提升好几倍。
生物膜上胞外聚合物基质(extracellular polymeric substances;EPS)中的胞外DNA,聚多糖、糖蛋白等像胶水一样,保持生物膜的完整性。虽然细菌酶和生物表面活性剂能够使生物膜分散,但是它们活性较低,且一种酶只能作用于一种EPS,不能有效剥离生物膜。
中国医学科学院的刘鉴峰、南开大学的史林启、格罗宁根大学的Henny C. van der Mei和Henk J. Busscher合作设计并制备了一种全新的胶束,不仅能实现向生物膜的靶向,还能有效破坏生物膜的完整性,实现优异的抗菌性能。这个双功能胶束由聚乙二醇-b-聚己内酯(PEG-b-PCL)和聚己内酯-b-聚四氨酯(PCL-b-PQAE)共组装得到,并修饰两性离子(含羟基的pH敏感羧基甜菜碱衍生物),记为ZW-MSPMs,不仅能很好靶向生物膜,而且两性离子基团可与胞外DNA和蛋白等相互作用,干扰它们共同发挥生物膜黏合作用。
ZW-MSPMs的合成及体内、体外靶向性能
在生理环境下,胶束的负电性使其有较好的循环稳定性,到达生物膜附近后(pH 5.0),胶束实现电荷反转,正电性利于其与带负电的生物膜相互作用,实现靶向功能。在体外实验中,pH 5.0时,胶束向浮游金黄色葡萄球菌靶向达到78%,在正常生理环境下的靶向仅有11%,因此能有效减少副作用。为了方便观察,作者将ZW-MSPMs和对照组SSPMs(单一胶束组分且不含两性离子)都负载尼罗红,通过腹部成像窗口对小鼠进行活体成像。注射20 min后,ZW-MSPMs在生物膜处的荧光强度开始增强,说明ZW-MSPMs的有效富集。而对照组SSPMs在生物膜处的荧光微不可察,侧面证明pH响应ZW-MSPMs在靶向生物膜方面的优越性。
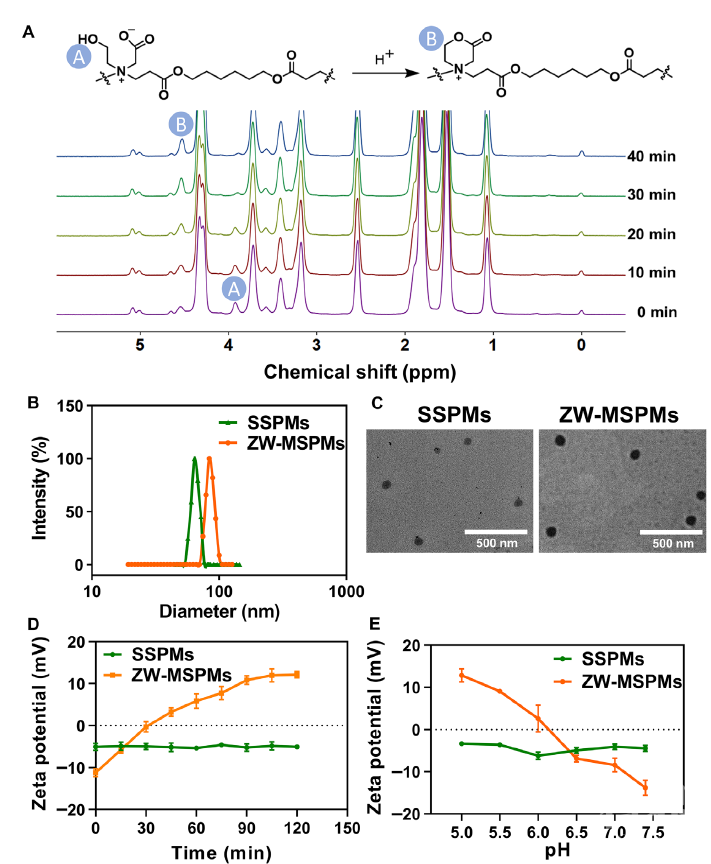 图1 ZW-MSPMs和对照组SSPMs的表征
图1 ZW-MSPMs和对照组SSPMs的表征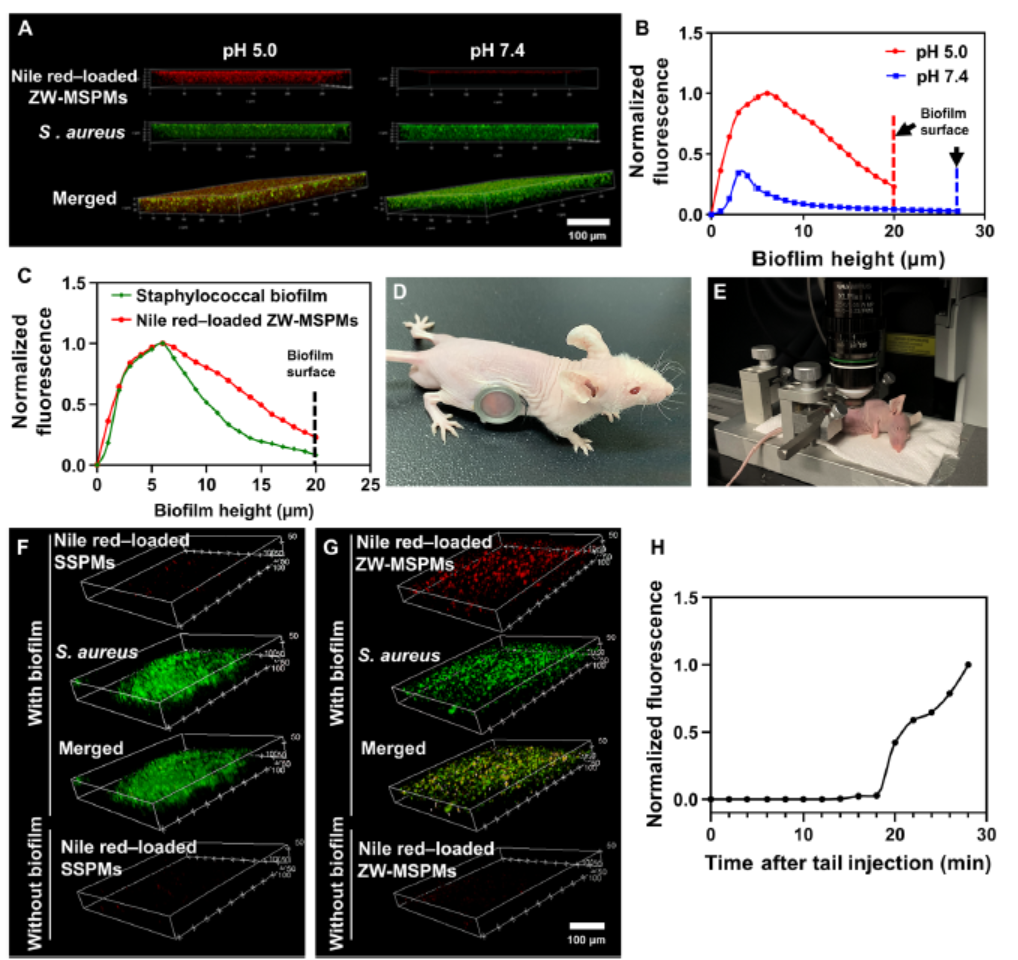 图2 ZW-MSPMs在体外和体内向金黄色葡萄球菌生物膜靶向的性能ZW-MSPMs破坏金黄色葡萄球菌生物膜的能力以及体内抗菌性能实验发现,经过ZW-MSPMs处理后,生物膜的重量明显减少,厚度从20.0 ± 1.6 µm下降到10.0 ± 1.4 µm,而对照组几乎没有任何变化。为了进一步确定生物膜中与ZW-MSPMs相互作用的主要成分,作者研究了鲱精DNA(模拟EPS基质的胞外DNA)和淀粉样纤维(内源性金黄色葡萄球菌生物膜)与ZW-MSPMs的相互作用。结果表明ZW-MSPMs与金黄色葡萄球菌之间的相互作用强于EPS基质成分与金黄色葡萄球菌之间的相互作用。因此,ZW-MSPMs会阻碍或破坏基质成分与生物膜内细菌的相互作用,从而影响生物膜的完整性。生物膜完整性的缺失会加速药物向生物膜内部的渗透,从而增强抗菌性能。于是,作者尾静脉注射抗生素环丙沙星,并通过腹部成像窗口对治疗效果进行观察。经PBS和SSPMs协同环丙沙星治疗小鼠生物膜的绿色荧光几乎没有发生任何改变,说明生物膜完整性较高,而经过ZW-MSPMs和环丙沙星治疗后,生物膜在3-5天后完全消失。5天后,白细胞计数恢复正常,粒细胞计数几乎恢复正常,而PBS或SSPM预处理小鼠血液中免疫细胞计数仍呈高度升高。并且,ZW-MSPMs也不会对其他器官造成损伤,有良好的生物安全性。
图2 ZW-MSPMs在体外和体内向金黄色葡萄球菌生物膜靶向的性能ZW-MSPMs破坏金黄色葡萄球菌生物膜的能力以及体内抗菌性能实验发现,经过ZW-MSPMs处理后,生物膜的重量明显减少,厚度从20.0 ± 1.6 µm下降到10.0 ± 1.4 µm,而对照组几乎没有任何变化。为了进一步确定生物膜中与ZW-MSPMs相互作用的主要成分,作者研究了鲱精DNA(模拟EPS基质的胞外DNA)和淀粉样纤维(内源性金黄色葡萄球菌生物膜)与ZW-MSPMs的相互作用。结果表明ZW-MSPMs与金黄色葡萄球菌之间的相互作用强于EPS基质成分与金黄色葡萄球菌之间的相互作用。因此,ZW-MSPMs会阻碍或破坏基质成分与生物膜内细菌的相互作用,从而影响生物膜的完整性。生物膜完整性的缺失会加速药物向生物膜内部的渗透,从而增强抗菌性能。于是,作者尾静脉注射抗生素环丙沙星,并通过腹部成像窗口对治疗效果进行观察。经PBS和SSPMs协同环丙沙星治疗小鼠生物膜的绿色荧光几乎没有发生任何改变,说明生物膜完整性较高,而经过ZW-MSPMs和环丙沙星治疗后,生物膜在3-5天后完全消失。5天后,白细胞计数恢复正常,粒细胞计数几乎恢复正常,而PBS或SSPM预处理小鼠血液中免疫细胞计数仍呈高度升高。并且,ZW-MSPMs也不会对其他器官造成损伤,有良好的生物安全性。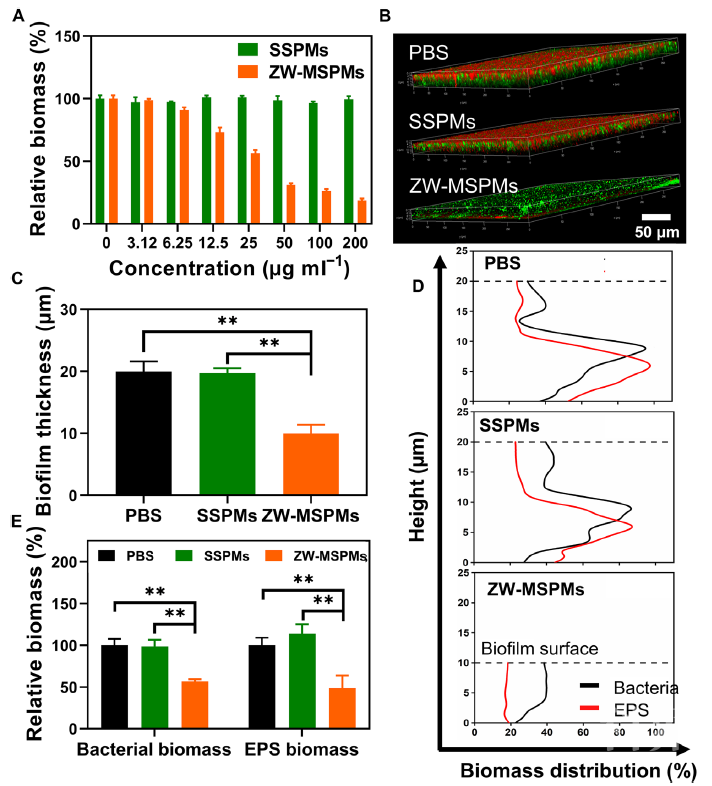 图3 S. aureus ATCC12600GFP生物膜生长48 h后经过PBS、SSPMs、ZW-MSPMs处理后的完整性
图3 S. aureus ATCC12600GFP生物膜生长48 h后经过PBS、SSPMs、ZW-MSPMs处理后的完整性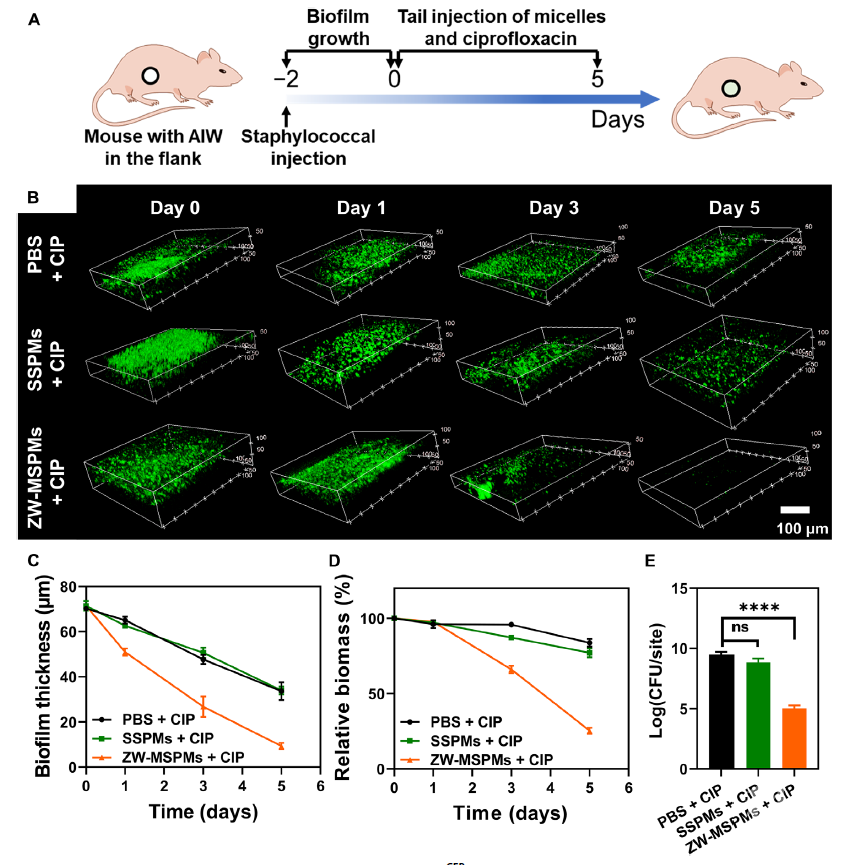 图4 ZW-MSPMs和SSPMs的体内抗菌效果小结作者制备了一种新型的靶向ZW-MSPMs作为生物膜分散剂。两性离子基团和pH响应性不仅能让ZW-MSPMs有效靶向生物膜,还能与EPS基质中的主要成分(胞外DNA和蛋白)产生强烈的相互作用,进而瓦解生物膜的完整性。打破生物膜的屏障后,抗菌剂向生物膜内部的渗透增强,进一步提高抗菌性能。作者通过技术与方法上的创新,通过已有的药物实现抗菌性能的增强。首先,这种方法可能用于易治疗的感染,然后慢慢发展用于更严重、难以治疗的耐抗生素感染。在临床试验中,这种循序渐进的方法可能比一种从发病开始就100%依赖于新疗法的方法更容易被接受。
图4 ZW-MSPMs和SSPMs的体内抗菌效果小结作者制备了一种新型的靶向ZW-MSPMs作为生物膜分散剂。两性离子基团和pH响应性不仅能让ZW-MSPMs有效靶向生物膜,还能与EPS基质中的主要成分(胞外DNA和蛋白)产生强烈的相互作用,进而瓦解生物膜的完整性。打破生物膜的屏障后,抗菌剂向生物膜内部的渗透增强,进一步提高抗菌性能。作者通过技术与方法上的创新,通过已有的药物实现抗菌性能的增强。首先,这种方法可能用于易治疗的感染,然后慢慢发展用于更严重、难以治疗的耐抗生素感染。在临床试验中,这种循序渐进的方法可能比一种从发病开始就100%依赖于新疗法的方法更容易被接受。来源:Polymer-science 高分子科学前沿
原文链接:https://mp.weixin.qq.com/s?__biz=MzA5NjM5NzA5OA==&mid=2651745105&idx=5&sn=866a8778011f083f60d6f66007ac8f9f&chksm=8b4a7914bc3df0027e9c072e0444c7f2e4b8343828c838c58e1255d83cd22ce055802d79b753#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn





