来源:中国科学院重大科技基础设施共享服务平台
7月30日,国家蛋白质科学研究(上海)设施质谱系统用户中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)王红艳研究组与上海大学魏滨团队合作,在国际学术期刊Proc Natl Acad Sci USA上在线发表题为“LRCH1 deficiency enhances LAT signalosome formation and CD8+ T cell responses against tumors and pathogens”的研究成果。
CD8+细胞毒性T细胞(cytotoxic T cell, CTL),在清除胞内菌、病毒等外界病原和肿瘤细胞过程中发挥着重要作用。T细胞受体(TCR)信号是促进静息期CD8+ T细胞活化成CD8+ CTL,并迁移到达病灶部位的关键因素。其中,CAR-T细胞浸润进入实体瘤及其在肿瘤内维持杀伤和增殖等因素成为限制CAR-T治疗实体瘤的瓶颈因素。近年多个实验室尝试通过敲除TCR信号中的抑制性分子,期望增强CAR-T细胞在实体瘤中的治疗效果。当TCR识别MHC呈递的抗原后,关键激酶如LCK、ZAP-70等活化,增强跨膜信号蛋白LAT (linker for activation of T cells)胞内段的多个酪氨酸位点磷酸化,招募GRB2、PLC-γ1、SLP-76等多种信号分子,形成LAT信号复合体(LAT signalosome)。LAT信号复合体随后启动下游多条信号通路,增强CD8+ T细胞的迁移、增殖和杀伤等功能。LAT缺失的CD8+CTLs不能上调FasL的表达,降低IFN-γ的产生,减弱杀伤能力。前人报道SHP-2、SHIP-1和c-Cbl等能够影响LAT信号复合体的形成,从而负调控CD8+ T细胞的功能。但是能直接结合LAT并且负调控TCR的信号分子,目前被报道的甚少。
王红艳研究组2017年发表在J Exp Med的文章揭示信号分子LRCH1(leucine-rich repeat and calponin homology domain-containing protein 1)负调控趋化因子诱导T细胞的迁移功能。在本研究中,利用蛋白质质谱等技术,发现LRCH1直接结合LAT(图1),抑制CD8+ T细胞的抗感染抗肿瘤的功能。这与LRCH1降低TCR信号诱导的LAT磷酸化水平,阻断GRB2与LAT的结合,破坏LAT信号复合体的形成;并且LRCH1促进LAT的内吞的分子机制相关。LRCH1缺失CD8+ T细胞的增殖速度更快,产生更多的IFN-γ、Perforin和Granzyme B等效应分子,对靶细胞的杀伤能力增强。RNA-seq结果提示LRCH1缺失后,许多与CD8+ T细胞的迁移、存活和代谢相关的基因上调表达,包括共刺激分子4-1BB(Tnfrsf9,常用来作为CAR-T细胞的胞内信号传导区域)的转录水平也显著升高。在动物体内的研究发现:Lrch1-/-小鼠能够更有效地清除李斯特菌(Listeria monocytogenes)和流感病毒(H1N1和H7N9)。研究人员进一步在Rag1-/-小鼠的尾静脉注射B16-MO5肿瘤细胞(表达OVA257-264抗原),然后过继性给予能特异性识别OVA257-264抗原的野生型OT1-Tg CTLs或Lrch1-/- OT1-Tg CTLs(图2)。LRCH1缺失的CTLs更显著地阻断小鼠肺部肿瘤结节数量,这与Lrch1-/- CTLs治疗组小鼠肺部有更多的CTLs浸润和增殖,并产生更高水平的IFN-γ和Granzyme B相关。最后,研究人员利用CRISPR-Cas9技术在包装了GPC3(glypican-3,该抗原在肝细胞癌中高表达)的人源CAR-T细胞中敲除LRCH1,结果显示LRCH1缺失的人源CAR-T细胞产生IFN-γ、迁移和增殖能力稍有增强。新型信号分子LRCH1能否作为促进CAR-T细胞功能的潜在靶点分子,有待在活体肿瘤模型中进一步的研究。
国家蛋白质科学研究(上海)设施质谱系统利用蛋白质质谱技术为该研究工作提供了蛋白质互作网络分析的有力支持。
图1 LRCH1与LAT直接结合。(A)293T中过表达相应质粒,免疫共沉淀检测Myc-LRCH1与Flag-LAT间的结合。(B)E. coli中纯化GST、GST-LAT和His-LRCH1,体外间接蛋白间的结合。
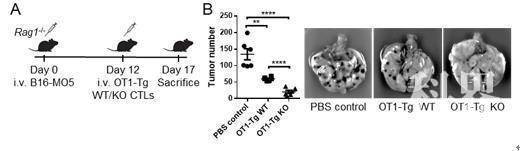
图2 Lrch1-/- CTLs能更有效地清除肿瘤。(A)肿瘤治疗模型图。(B)肺部肿瘤结节个数及代表图。
来源:中国科学院重大科技基础设施共享服务平台
原文链接:http://lssf.cas.cn/lssf/dbzkxyjshss/xwdt/202008/t20200811_4557855.html
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn