来源: RSC英国皇家化学会
1. 研究背景
细胞力学性能不仅能为细胞生物学研究提供新思路,而且还可为基于细胞力学性能变化的疾病诊断提供指导。传统的细胞弹性测量技术,如基于原子力显微镜的细胞压痕实验和微吸管细胞挤压法等,或者依赖昂贵的设备,或者需要复杂的手动操作,难以实现自动化和高通量。近年来,微流体技术在细胞力学性能研究领域取得了重要进展。剪切流、拉伸流等用于使活细胞在流体剪切力作用下直接变形或者在狭窄微流道中被挤压变形,根据细胞变形指数(细胞长轴与短轴之比)、通过时间等参数来定性比较细胞的弹性。该技术不但是高度自动化的,并且具有非常高的通量,可以达到约 2000 个细胞/秒。但是相对于细胞力学性能的定性研究,定量检测可以提供更加准确的数据,促进基于细胞力学性能的疾病快速诊断技术的发展。
要对细胞力学性能进行定量研究,必须对细胞受力进行精确测量和控制。现有微流体技术一般采用数值模拟或者测量细胞周围液体流速等方法间接获取细胞变形过程中的压力数据。本文报道了一种集成细胞变形时压力精密测量功能的微流体系统,该系统使单细胞在微小流道中快速大幅变形,并实时检测变形过程中的压差变化,进而精确计算细胞弹性。该装置在细胞力学性能的精确评估中具有巨大的应用潜力。
2. 成果简介
近日,哈尔滨工业大学(深圳)陈华英课题组在英国皇家化学会(RSC)期刊 Lab on a chip 上发表题为“Cell elasticity measurement using a microfluidic device with real-time pressure feedback” (DOI: 10.1039/D0LC00092B)的研究论文,报道了一款用于单细胞力学性能精密测量的微流控芯片。该芯片集成了微颗粒分离和压力精密检测功能,实现了利用细胞变形量和对应的压差精密测量单个细胞的弹性模量(图 1)。结合图像处理和压差分析程序,该装置有望实现细胞力学性能的自动化检测。该论文第一作者是哈工大(深圳)应届硕士毕业生陈震林。陈华英副教授为通讯作者。
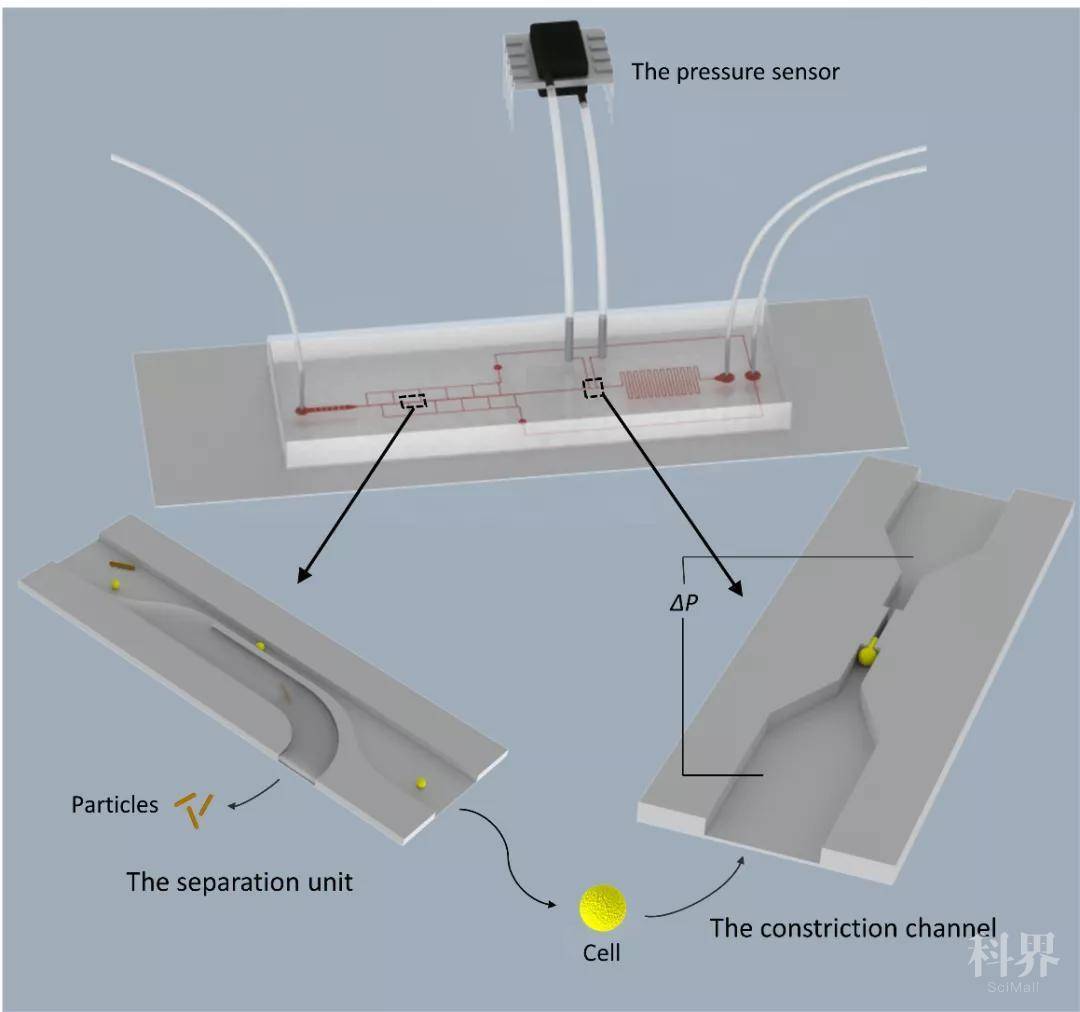
图 1. 利用集成微颗粒分离和压力精密测量功能的微流控芯片进行单细胞力学性能研究的示意图。细胞悬浮液中的微颗粒被分离到侧通道中,主流道中的单个细胞被推送到宽度和高度分别是 6 微米和 16 微米的挤压通道,细胞变形时所在通道压力的实时变化被两侧的精密压力传感器记录。通过细胞变形和压力数据可以精确计算细胞的弹性。
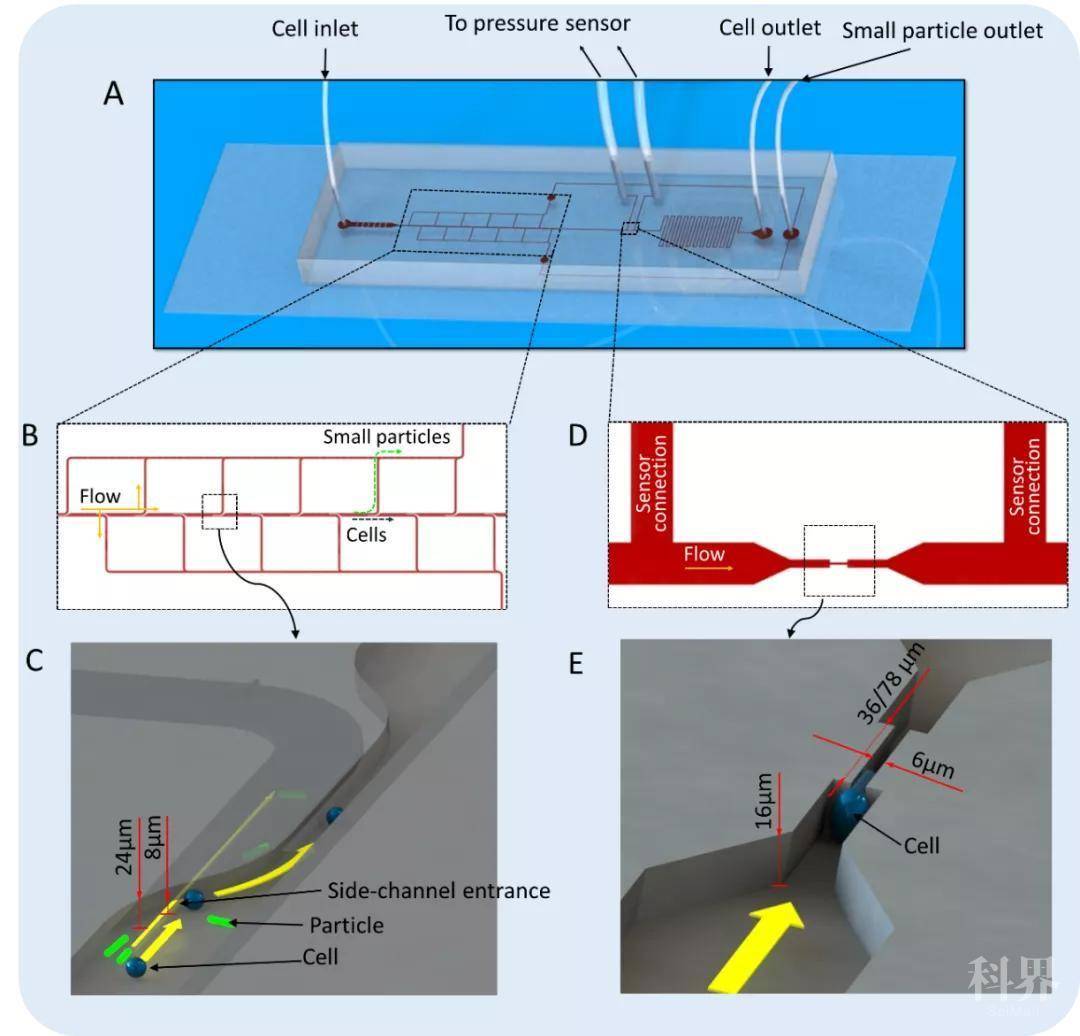
芯片主要由微颗粒过滤单元,压差精密检测系统和细胞挤压通道三部分组成(如图 3)。细胞悬浮液中常常混杂着一些颗粒状或棒状杂质,它们经常会堵塞仅有 6 微米宽的细胞挤压通道。该通道一旦被堵塞,很难通过改变液体流速将颗粒杂质排除,往往只能更换新的芯片从而大大降低实验效率。因而,该芯片集成了如图 2B-C 所示的“多级隧道分流”系统。它的侧流道高度小于主流道高度,尺寸较小的微颗粒会进入较矮的侧流道,而直径较大的细胞会沿主通道流向下游进行单细胞挤压。如图 2D 所示,压力差检测系统主要由 Arduino 信号采集系统和连接细胞挤压通道两端的精密压差传感器组成。单个细胞在流体推动下收缩变形并通过挤压通道(如图 2E 所示)。利用幂律流变模型结合细胞的变形程度和对应的压差数值可以计算单个细胞的弹性模量和粘度。该研究在细胞力学性能研究领域具有重要意义。
该论文的主要内容包括:
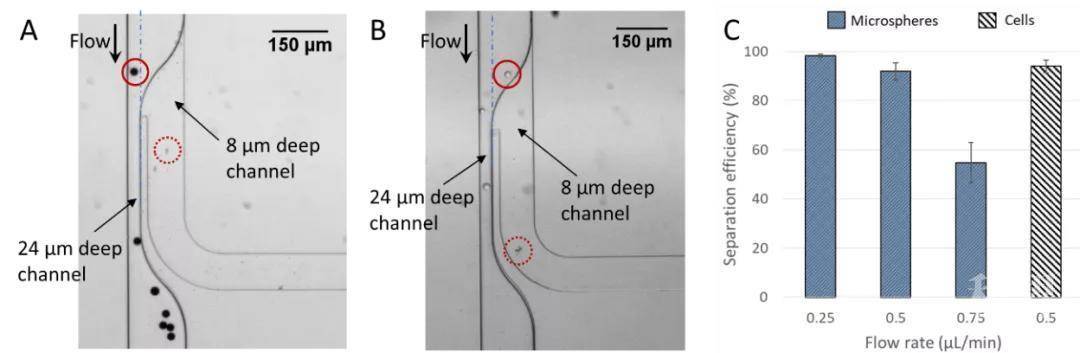
1. 分离机理和效率研究。利用数值模拟分析了颗粒分离的流体力学机理,并采用实验研究了不同流量下该系统对不同尺寸聚苯乙烯微球的过滤效率以及 K562 细胞悬浮液中杂质的过滤效率。
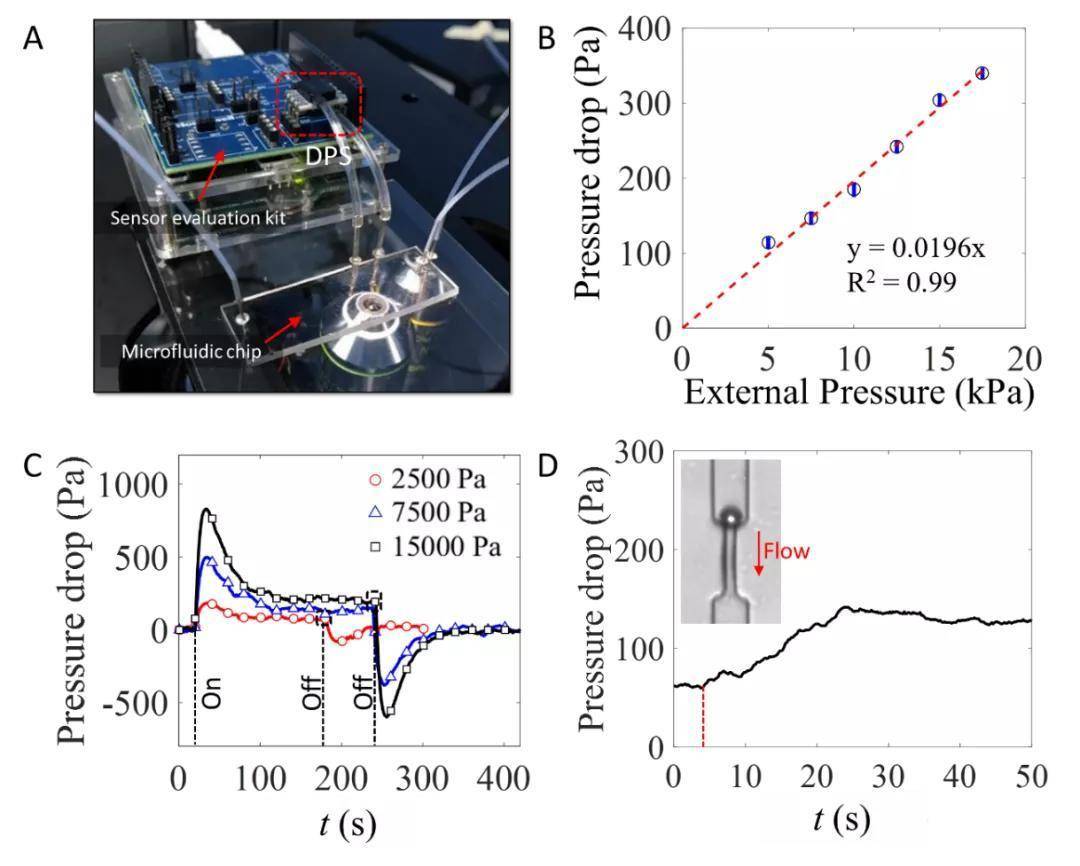
2. 压差精密测量研究。精密压差传感器出入口连接芯片细胞挤压通道两端,电信号由 Arduino 实时采集(如图 4A)。文章对传感器的压力响应进行了详细分析(如图 4B-D)。
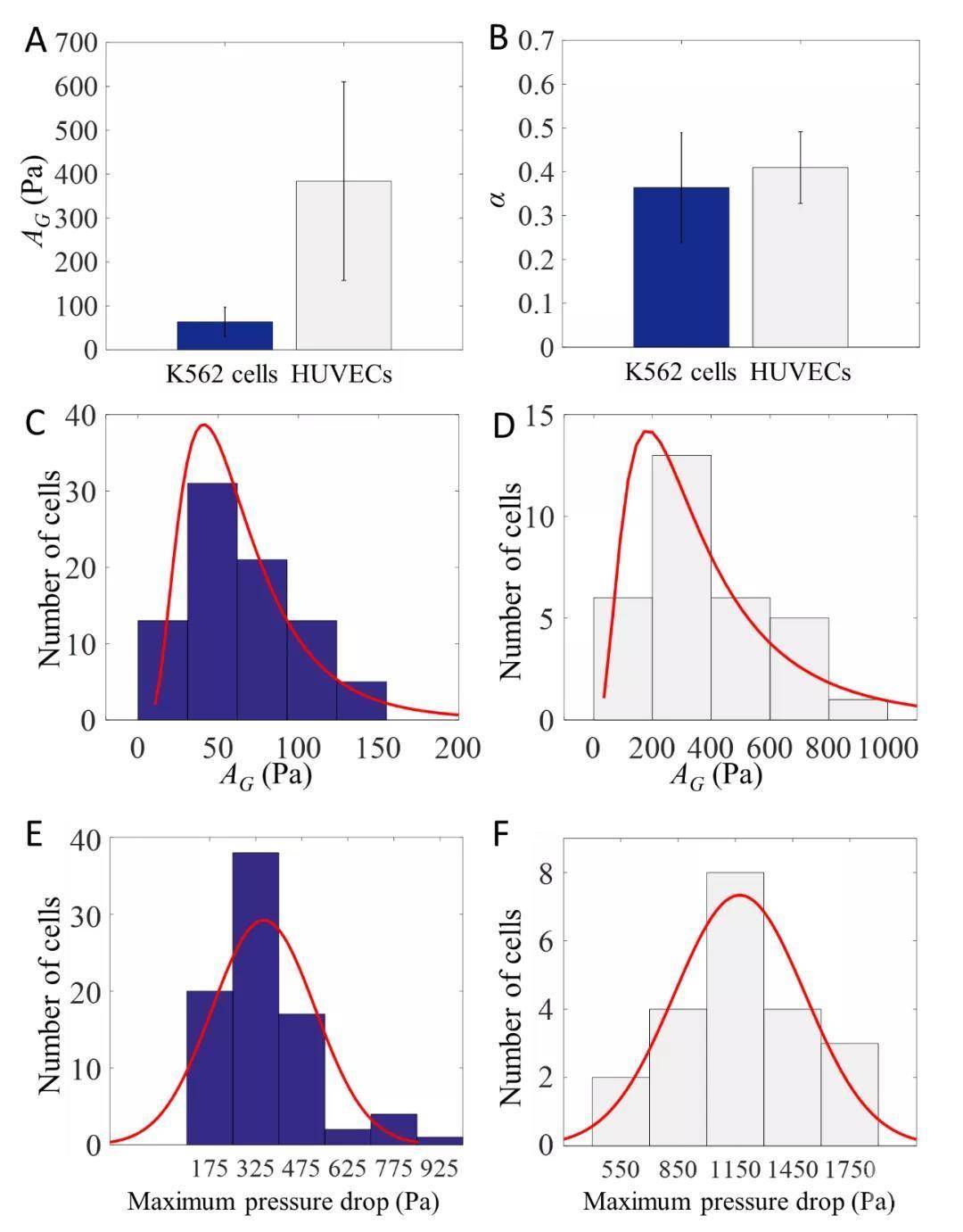
3. 单细胞力学性能检测。利用该装置检测了 K562 和人脐静脉内皮两种细胞。结合幂律流变模型,获得两种细胞的刚度参数 AG 和幂律指数 α 结果如图 5 所示。其中,刚度参数 AG 为等量杨氏模量,α 为表征细胞流动性的幂律指数(0 为完全弹性表现,1 为完全粘性表现)。该论文的结果与前人的研究非常吻合。此外,本研究证明了每个细胞变形通过同一收缩通道时所需要的压力差别可达四倍以上,因此测量导致每个细胞变形的压力对精密研究细胞弹性模量具有重要意义。
* 该工作得到国家自然科学基金 (31701187) 和深圳市科学技术创新委员会(JCYJ20170811160246740,JCYJ20180306172109024 和 JCYJ20170413105329648)的支持。