来源:高分子科学前沿
近年来,光热疗法(PTT)作为肿瘤治疗中的新兴手段被广泛研究。然而,由于肿瘤的耐热性以及由此引起的肿瘤复发,使得PTT的研究面临着巨大挑战。因此,克服肿瘤耐热性是使实现放大PTT效果的一种潜在策略。
朱利民教授课题组多年从事生物医学纳米材料的设计和应用相关领域的研究工作。其中,在光热治疗相关的协同治疗方面,近些年来开发了多种新型的多功能肿瘤诊疗平台,取得了一系列高水平的研究成果。研究工作发表在Advanced Science、Theranostics、ACS Applied Materials & Interfaces、Chemical Engineering Journal、Advanced Healthcare Materials等国际著名期刊上。
近期,该团队利用二维纳米片独特的优势,设计了一种基于硼纳米片的智能纳米平台来实现基于低温PTT和化疗的协同治疗。首先,通过结合热氧化蚀刻与液相剥离技术制备硼纳米片(B NSs),同时使用氨基化PEG与cRGD肽对B NSs进行表面修饰,使其可以实现主动靶向、延长体内循环时间及增强其在肿瘤部位的有效富集。同时,将其作为药物载体负载化疗药物DOX与热休克蛋白抑制剂17AAG,实现药物在癌细胞内的特异性释放。研究结果表明,硼纳米片超高的比表面积使其能够高效的负载小分子(对于DOX与17AAG,负载量分别为603 mg/g 与417 mg/g B-PEG-cRGD)。当载药复合物进入肿瘤细胞内部后,在内部环境及外部近红外激光的刺激下,负载的17AAG释放出来抑制热休克蛋白的表达,克服肿瘤细胞的热耐受性并在低温下有效地诱导细胞凋亡。体外细胞实验与体内动物模型证实了该双响应载药复合物可以实现良好的低温PTT/化疗协同作用。本工作拓展了二维硼纳米片在生物医学中的应用,并为新型低温PTT治疗策略的发展提供了一种新的思路。
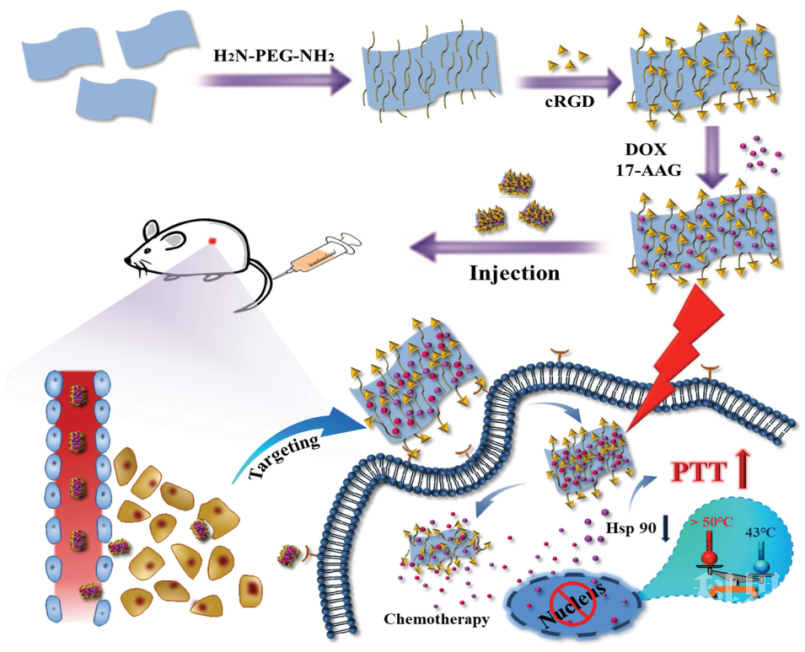
图1 具有相互协同作用的低温PTT/化疗的载药纳米颗粒用于高效癌症治疗示意图。
相关成果以“Functionalized boron nanosheets as an intelligent nanoplatform for synergistic low-temperature photothermal therapy and chemotherapy”为题发表在知名期刊《Nanoscale》上,东华大学化学化工与生物工程学院付梓硕士为该论文的第一作者,通讯作者为东华大学朱利民教授以及课题组毕业博士生吴建荣(现就职上海交通大学附属上海市第六人民医院)。上述工作得到上海市科委项目(16410723700)和教育部生物医学纺织材料“ 111项目”(B07024)的支持。
来源:Polymer-science 高分子科学前沿
原文链接:https://mp.weixin.qq.com/s?__biz=MzA5NjM5NzA5OA==&mid=2651740731&idx=3&sn=1c3811b272a1c8f0f9ae725c9d9eea48&chksm=8b4a487ebc3dc168e19b24ff1c8315e6912719f78706d69af901d57abf96a23f0fa5f729a4b5#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



