来源:brainnews
光遗传学开辟了一个新的让人激动的研究领域,使研究者可以在高时空分辨率下随心所欲地控制某些特异类型的细胞。小编这期汇总了全球研究人员利用Maestro multiwell-MEA(多孔微电极阵列)系统配合光遗传刺激(Lumos)系统进行相关研究的四个案例,帮助大家了解光遗传学与MEA之间可以擦出什么样的火花。
自主神经系统:
hiPSC衍生交感和副交感神经元协调控制心率
来源:日本产业技术综合研究所细胞与分子生物技术研究部,2020, Scientific Reports
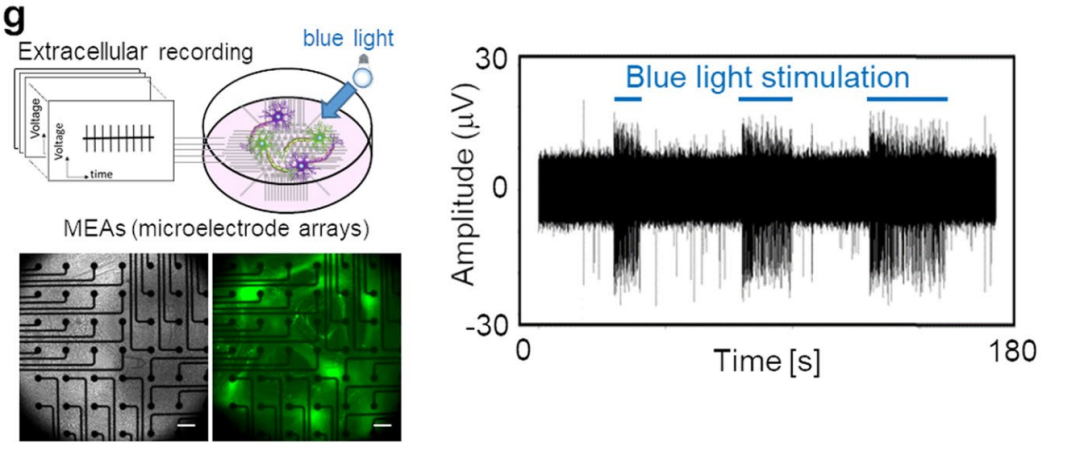
自主神经系统(ANS)通过去甲肾上腺素能交感神经的兴奋作用和胆碱能副交感神经信号的抑制作用来调节组织的动态平衡和重塑。尽管有许多关于从人多能干细胞(hPSCs)诱导交感样神经元的报道,但还没有一种诱导方法能有效地从hPSCs分化出胆碱能副交样感神经元。本文研究者将传统的神经细胞诱导方法从2步修改为4步诱导出自主神经系统神经元,诱导至36天时,在含有微型隧道的培养板上,可观察到神经元轴突的分化。在诱导52天后,给予表达ChR2的神经元蓝光刺激,跟随光刺激的时程,在Maestro MEA系统上会检测到相应时程的神经元放电,证明新方法诱导的神经元已经分化成为具有功能的ANS神经元。
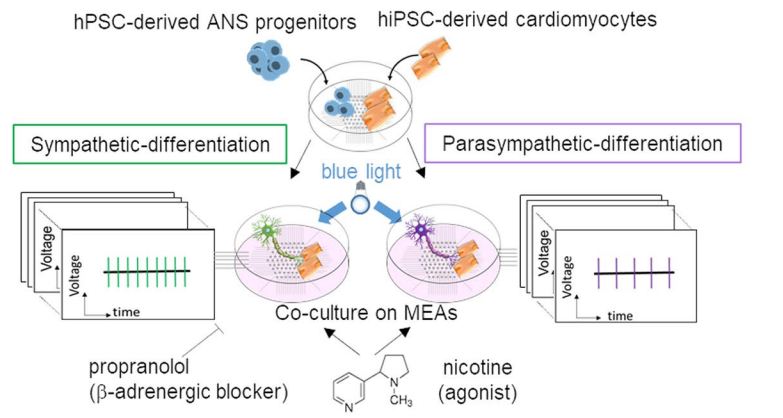
进一步的研究发现,高细胞密度和低神经营养因子可诱导ANS祖细胞分化成为交感样神经元,相反条件下可以诱导出副交感样神经元。为了检验这两种ANS神经元是否能对心肌细胞进行精确调控,研究者先将hiPSC来源的心肌细胞种植在Cytoview MEA 6孔板中,再将诱导至13天的交感样和副交感样神经元分别与心肌细胞进行共同培养。用蓝光或尼古丁刺激表达ChR2的交感样神经细胞时,心肌搏动频率显著增加;而使用尼古丁刺激副交感样神经细胞时,搏动频率明显降低。单独培养的心肌细胞使用尼古丁刺激时,只有微弱的变化。至此,研究者建立了一种从hPSCs中高度选择性地诱导交感样和副交感样神经元的方法,促进了人ANS神经的建模和研究。
脊髓损伤:
利用光遗传学构建斑马鱼脊髓损伤模型
来源:美国斯坦福大学,2017, SfN poster
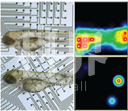
复杂的脊椎动物神经元的丢失往往伴随着永久性的功能障碍,所以细胞消融成为潜在的建立脊髓损伤模型的有效方法。现有的人工手刺法,具有极大的限制性——会引入外来损伤,并且重复性差、死亡率高。而光遗传技术则可以更精确地控制特定细胞消融,模拟脊髓损伤。研究者将光敏感蛋白表达在斑马鱼的外周神经细胞内,使用蓝光刺激诱导细胞消融后,在Maestro MEA系统中检测神经元放电状态。与传统人工方法比较,两种方法中网络簇放电频率都有不同程度的降低,而平均放电频率都有不同程度的升高。这表明了利用光遗传技术可以成功地建立脊髓损伤模型。该研究为神经元环路的连通性与脊髓损伤病理学的探索提供了一种新的强有力的检测方法。
来源:brainnews brainnews
原文链接:https://mp.weixin.qq.com/s?__biz=MzI2ODEyOTE3OQ==&mid=2649574667&idx=2&sn=2a84b33e1969dd4fe1fee13e14617e7e&chksm=f2edabffc59a22e9724b989b6cd031f4af8de993d488c1e625082fd4e4407decb4af9f7e5529#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn