结晶样视网膜变性(Bietti crystalline dystrophy, BCD)是一类会对视力健康造成严重危害的单基因遗传病,以患者眼底的大量黄白色闪亮结晶沉积为代表性特征。它的另一个显著特征是,相对于其他人群,BCD在东亚人群中具有显著增高的发病率。据估计,中国人群中BCD的发病率约为1/24000,占全部视网膜色素变性患者的1/6至1/10。大多数BCD患者于20-40岁发病,出现夜盲和视力下降等症状,在50-60岁发展为法定盲人。
虽然是一类危害严重的致盲性遗传眼病,但与一些西方媒体高度关注的“明星遗传病”相比,针对BCD的基础和临床研究都较为匮乏。迄今BCD仍然缺乏有效的动物模型,导致一方面无法进一步了解BCD病程的影响因素;另一方面也无法验证潜在的治疗药物。在意大利医生G.B. Bietti首次临床观察到并为这种疾病命名的八十年之后,BCD依然无药可治。
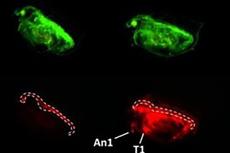
CYP4V2是人体内的ω-氢基化酶基因,在多种代谢通路中发挥作用。遗传自父方和母方的CYP4V2基因同时发生突变,导致了BCD的发病。相对于正常水平而言,BCD患者体内的脂类水平有着显著异常。通过敲除小鼠中包含整个Cyp4v3(CYP4V2的小鼠同源基因)的完整基因座,中国科学院动物研究所研究团队成功构建了Cyp4v3完全缺失的小鼠模型。进一步研究发现,高脂肪饲料喂养的Cyp4v3缺失小鼠模型,展现出眼底结晶和视力功能下降的双重BCD疾病表型。作为六大营养物质之一,脂肪在日常饮食中无法避免。以上的研究结果表明,过高的脂类水平不仅是BCD疾病的异常表征,还是能加速BCD疾病进程的危险因素。这提示了控制日常脂肪摄入,可能是改善BCD疾病护理、延缓疾病进程的重要手段。
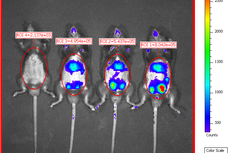
基因治疗(Gene Therapy)是将外源基因导入细胞,纠正或补偿因基因缺陷或基因表达异常引起的疾病的新型治疗手段,在对遗传性疾病的治疗上具有重大潜力。动物所研究团队通过与北京协和医院合作,将腺相关病毒 (Adenovirus associated virus, AAV)包装的人CYP4V2基因注射到高脂肪饲喂的Cyp4v3敲除小鼠模型眼底,进一步验证基因治疗对BCD的适用性。研究发现,经过基因治疗的小鼠眼底厚度显著增加,视觉功能(眼底的电生理反应水平)也得到改善。这些结果首次在活体动物模型中展现了基因治疗对于BCD治疗的有效性。
相关成果于6月1日在国际学术期刊Gene Therapy 发表。该研究工作由中科院动物所、中科院干细胞与再生医学创新研究院和北京协和医院合作完成。动物所研究员李伟和北京协和医院教授睢瑞芳为论文的通讯作者;曲彬、吴世靖、焦贯怡、邹绚、李治琨、郭璐为共同第一作者。该研究受到科技部、基金委及中科院战略科技先导专项等的资助。
论文链接

图:高脂饮食加速BCD疾病进程,基因治疗改善模型鼠视觉功能
内容来源:中国科学院来源:中国科学院
原文链接:http://www.cas.cn/syky/202006/t20200603_4748790.shtml
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn