不是我军不给力
无奈癌症太狡猾
人类这一百年来新的医学技术可谓层出不穷,征服了那么多一度收割无数人命的疾病,却为何至今还不能动得了癌症分毫呢?
其实原因很简单,癌症并不是一种疾病。许多人可能都听说过,癌症源于一些基因突变,但是更确切地说,癌症是细胞层面上的进化。总有那么一些基因突变,会让细胞突破身体的监管,开始肆意分裂,留下大量的后代,而这些后代又会在原来的基础上积累更多基因突变。人类有千千万万的基因,细胞就能有远多于千千万万的突变,这不计其数的突变彼此再排列组合就会有恒河沙数的变化。无论是人体自身的抗癌机制,还是现代医学技术的干预,对癌细胞来说都不过是某种“物竞天择”而已,杀死的都是弱者,而杀不死的必定会更强大。任何有限的手段在这种无穷无尽的变化面前,都会遭到癌症那穷举法般的暴力破解。
不过反过来说,纵然癌症有无数可能的基因突变,但是具体到某一个病例身上,在癌症早期基因突变的种类相对还是比较有限的,如果可以针对每个患者具体的基因突变情况,对症下药制定专门的治疗方案,那么理论上还是有可能在癌症早期将癌细胞一波团灭的,这个思路就是时下比较热门的“个性化医疗”。
虽然“个性化医疗”的愿景很美好,但就目前而言依旧是困难重重
想法是不错,但是实际操作的时候就是另一回事了,基因突变是非常随机的,从这个角度来说,世界上没有任何两例完全相同的癌症,医生永远也不知道下一个癌症病人身上会有怎样的基因突变,这种基因突变又是否可以套用以前的治疗手段。一方面张三的成功经验没准会要了李四的命,而另一方面如果等到发现一种基因突变以后才去从头开发治疗方案,病人可等不起这漫长的研发周期。
跳出“猫鼠游戏”
这种“被动防御”式的研究,只会让科学家在和癌症的猫鼠游戏中永远跑在后面,因此,来自耶鲁大学系统生物研究所的陈斯迪教授与来自瑞士巴塞尔大学的兰德尔·普拉特(Randall J Platt)教授决定“主动出击”,跑赢癌症,防患于未然。这项研究发表在了最新一期的《自然·神经科学》(Nature Neuroscience)上。
之所以发表在神经学期刊上,是因为他们选择了胶质母细胞瘤,也差不多相当于我们一般所说的脑癌作为他们的研究对象。陈教授在接受果壳网采访时说:“胶质母细胞瘤是目前最恶性的肿瘤之一,它发生在脑部,导致很难治疗,目前体内筛选技术在脑组织很难进行,所以我们决定攻克这个难题。”
在此之前,科学家通过临床研究资料已经知道,很多脑癌病人的肿瘤中都有一些特定的基因突变,但是究竟怎样的基因突变组合是引发脑癌的必要条件,那些看似“不必要”的基因突变又对脑癌有着怎样的意义,却依旧难以解答。
兵法有云,知己知彼百战不殆。想要打败敌人,就要先了解敌人,学会用敌人的思路去分析问题。而陈教授便是如此,他们所做的相当于是在小鼠体内重现了癌症的进化。他们人为给小鼠的大脑引入大量随机的基因突变,然后让这些带着不同基因突变的脑细胞在小鼠脑中自由竞争,等小鼠长出肿瘤以后,分析一下肿瘤细胞的基因,就能知道怎样的基因突变会导致怎样的肿瘤了。
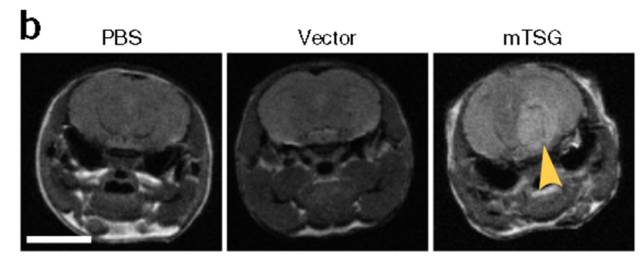
陈斯迪教授的团队在小鼠脑中诱导产生的胶质母细胞瘤
能揽瓷器活
必有金刚钻
当然,等细胞自发基因突变肯定是太缓慢了,他们需要加速这个“进化过程”,为此,他们用到了一种大致可以叫做“CRSPR建立随机突变库筛选”的技术。
通俗来说,首先有一种很强的基因编辑技术叫做CRISPR/Cas9,这个系统由两部分构成,一个是可以引入基因突变的Cas9蛋白,一个是可以精确定位特定基因位置的SgRNA,Cas9蛋白与SgRNA相结合就能非常精确地在特定的基因上制造基因突变。如果Cas9蛋白和一个SgRNA相结合,那么就只能在一个基因上制造突变,而如果把Cas9蛋白和一大堆不同的SgRNA相结合,那么Cas9就有可能在很多基因上都制造出基因突变。不过如果SgRNA非常多的话,Cas9蛋白不太可能和每个SgRNA都结合一遍,所以产生的基因突变就有了很大的随机性。
不过纵使CRISPR/Cas9有千般好,它本质上也就是一些生物大分子,将这些物质安全高效地运送到小鼠的脑细胞内可没那么容易。不过这问题难不倒科学家们,他们采用了一种非常经典的工具,那就是病毒。所谓病毒基本上就是一堆被蛋白质打包起来的遗传物质,再通俗点就是一份“基因快递包裹”。我们知道有的恐怖分子会邮寄所谓的“炸弹包裹”,好多人傻乎乎的也忘了自己最近有没有剁手,一看地址收件人都对,包裹一拆就悲剧了。病毒也是一样,它的蛋白质外壳就像是快递包裹,上头写着给细胞识别的收件人信息,大部分细胞也不会比人聪明到哪去,结果就把病毒的致病基因吸收了进去。
虽说欺骗这些老实巴交的细胞好像不太厚道,但是病毒这特性倒是帮了科学家大忙,通过一些技术手段,科学家可以把病毒当中会导致细胞生病的“坏基因”给换成别的基因,这样病毒也就“浪子回头”,成了真正意义上的快递小哥。在这项研究中,陈教授的团队使用了一种特别适合给神经细胞“送快递”的病毒,腺相关病毒(AAV)。他们将能够表达他们这套CRISPR/Cas9系统的基因包装到AAV中,就能让小鼠的脑细胞出现他们所需的突变了。
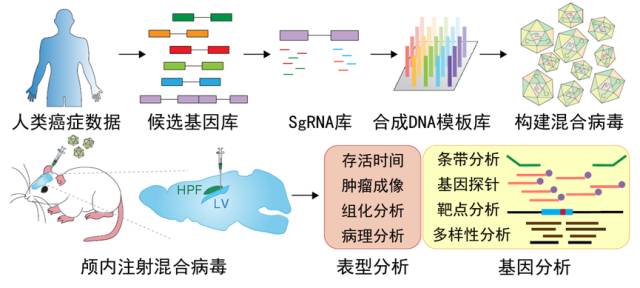
该项研究的技术路线示意图
如果你觉得上面那些专业解释太复杂,那你只要知道他们的这个方法可以让小鼠大脑产生随机基因突变,从而制造出各种各样的脑癌就行了。
陈教授曾在张锋麾下做过一段时间访问博士后,对于CRSPR相关的技术自然是了然于胸(本次研究也得到了张锋的帮助)。利用这种方法,他就可以脱离现实的病人,直接在小鼠身上制造出尚未被充分报道的癌症病例。
除此之外,陈教授还想知道基因突变的种类与组合是否还会影响癌症治疗的效果,为此他使用了类似的方法,同时在癌细胞的“进化”中引入了现代医学干预,比如说他给一些小鼠使用了一种叫做替莫唑胺(temozolomide)的化疗药物,在这种状况下还能“脱颖而出”的癌细胞就必定包含可以对抗这种治疗方案的基因突变。
理论上讲,类似的方案也可以用于评估其它治疗方案的适用范围,从而帮助医生找到最合理的应对手段。陈教授说:“这个新方法能够直接应用于药物-基因共同筛选或者双向筛选,有利于直接发现在体内的变异特异性药物应答,我们现有的工作已经发现几个基因在胶质母细胞瘤影响化疗效果。”
随着CRISPR/Cas9等新技术的进步与成熟,类似的方法也将有更加广阔的应用空间。除了脑癌以外,陈斯迪教授坦言,他们也已经在其它癌症,乃至是癌症以外的疾病上尝试类似的思路,未来或许还会有更多的突破。
陈教授说:“几年前,CRISPR技术带来了目前21世纪最伟大的基础生命科学的突破,同时,癌症研究因为免疫疗法的兴起,已经带来了另一项临床医学的革命。许多十几年前的绝症,比如黑色素瘤、肺癌和好几种类型的白血病,在某些特定人群里已经有很好的疗效。这两项技术的结合将会给生命科学和医学的研究带来一场全新的革命,帮助人类向攻克癌症迈出新的一步。”
尽管就目前而言,科学家还不至于马上跑赢癌症,但是随着新技术的进步,至少他们已经开始跑了。找到致病根源,也许就是万里长征的第一步。
(来源:果壳科学人)




