来源:生物通
干细胞一向以潜力无限而闻名,如今,它的优良品质中还可以再加上一条:视死如归。一项发表在《Current Biology》杂志上的最新研究表明,干细胞能够延迟自己的死亡,以应对身体受到的伤害。
干细胞一向以潜力无限而闻名,如今,它的优良品质中还可以再加上一条:视死如归。一项发表在《Current Biology》杂志上的最新研究表明,干细胞能够延迟自己的死亡,以应对身体受到的伤害。
这项研究是在涡虫中开展的,这种模式生物常常作为研究再生的模型,因为它们具有利用干细胞修复损伤的能力。文章的第一作者、康奈尔大学兽医学院的Divya Shiroor表示:“即使面临挑战并受到胁迫,涡虫干细胞仍然通过延迟死亡来应对损伤。”
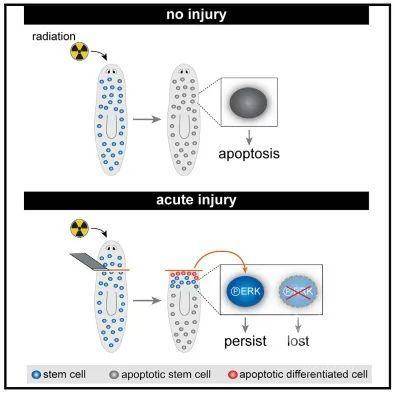
研究人员将涡虫暴露在辐射下,然后让其中的一半受伤。他们发现,如果涡虫未受伤,则正如预期地那样,干细胞在辐射后死亡。但是,若涡虫受伤,则干细胞会存活下来,聚集在伤口部位的附近,延迟自身死亡以引起反应。
Shiroor表示:“如果动物暴露于辐射下,不久又受伤,那么这种辐射诱导的干细胞死亡会大大延迟。”这项成果可能对癌症的研究和治疗具有重要意义,特别是有助于患者选择化疗和手术,因为最新研究发现,手术损伤会促进休眠肿瘤细胞的转移。
研究人员希望进一步了解损伤如何促使涡虫干细胞承受辐射。Shiroor说:“我们希望鉴定出相关基因,如果与哺乳动物共享,那么这些基因也许有助于改造现有的疗法。”
涡虫在某些方面与人类相似,因此它们通常被用于基础研究。与人类一样,涡虫具有干细胞、相似的器官和相似的基因,但由于干细胞数量庞大且缺乏发达的免疫系统,它们在处理损伤时更加内行,而人类免疫系统的存在让情况变得更复杂。
研究人员指出,辐射会导致干细胞迅速启动凋亡,而损伤让凋亡过程延迟发生,同时防止干细胞进入有丝分裂状态,这大概是为了实现DNA损伤的修复。由于干细胞仅仅存在于伤口周围,他们推断“损伤信号”是高度局部的,可被这些细胞直接感知。
他们发现,损伤之后丝裂原活化蛋白激酶ERK(细胞外调节蛋白激酶)的激活驱动了干细胞的持久存在。ERK的药理抑制可阻止干细胞的持久存在。由于局部的细胞死亡不需要ERK活性,故研究人员认为,该通路在干细胞内起作用。
实验室有很多方法可以了解涡虫如何利用干细胞来成功恢复和再生,但Shiroor所在的实验室将辐射和损伤相结合,确定干细胞的反应是独一无二的。他们计划开展更加深入的研究,以了解干细胞如何知道损伤存在,以及其他细胞可能在此过程中起什么作用。
Shiroor表示:“我们已经确定了辐射和损伤后干细胞持续存在的关键基因,我们计划以此为垫脚石,今后开展更深入的探索。”
参考文献
Injury Delays Stem Cell Apoptosis after Radiation in Planarians, Current Biology (2020). DOI: 10.1016/j.cub.2020.03.054
来源:gh_c1fce5726992 生物通
原文链接:https://mp.weixin.qq.com/s?__biz=MjM5NzMwNjYyMg==&mid=2675533299&idx=4&sn=ede86888459dc71ec987de3d640a4ed1&chksm=bc51cc628b264574212c9e4540f259f977f3744d130f9efa2083ac58bf0f349d4b6f8ef79096#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn


