来源:中华泌尿外科杂志公众订阅号
点击上方“蓝色文字”关注我们
作者:刘鹏飞1 侯广东1 倪建鑫1 严奉奇2 魏迪1 郑昱1 王佳1 马帅军1 杨晓剑1 武国军1
作者单位:
1空军军医大学西京医院泌尿外科
2空军军医大学唐都医院泌尿外科
引用本刊:
刘鹏飞,侯广东,倪建鑫,等. 保留肾单位手术后肾功能预后的影响因素分析[J].中华泌尿外科杂志,2020,41(3):179-184.DOI:10.3760/cma.j.cn112330-20190530-00254.
摘要
目的
探讨肾肿瘤行保留肾单位手术(NSS)后肾功能预后的影响因素。
方法
回顾性分析西京医院2016年12月至2018年12月行NSS治疗的115例肾肿瘤患者的临床资料。男75例,女40例。年龄(49.50±12.94)岁;体质指数(24.59±3.59)kg/m2;肿瘤最大径(3.66±1.32)cm;R.E.N.A.L.评分(6.43±1.60)分。术前患肾肾小球滤过率(GFR)(48.22±11.48)ml/(min·1.73m2),健肾GFR(49.73±11.96)ml/(min·1.73m2),总GFR(97.95±21.32)ml/(min·1.73m2)。术前患肾有功能肾组织体积(FPV)(132.23±9.11)cm3。61例行腹腔镜肾部分切除术,54例行机器人辅助腹腔镜肾部分切除术。记录手术时间、热缺血时间(WIT)、术后病理结果。记录术后6个月的血肌酐、患肾GFR、健肾GFR、总GFR、GFR保存率(术后GFR与术前GFR的比值)、患肾FPV、患肾FPV保存率(术后患肾FPV与术前FPV的比值)。患肾FPV通过手术前后的CT影像使用椭球体近似法测量。手术前后GFR和患肾FPV比较采用配对样本t检验。采用Spearman秩相关分析评估各研究因素与患肾GFR保存率间的相关性。多因素分析采用多元线性回归模型分析患肾功能的独立预测因素。以WIT=25 min为截断点将患者分为≤25 min组和>25 min组,比较两组术前患肾GFR,以及术后6个月的患肾GFR和患肾GFR保存率。
结果
本组115例手术均顺利完成,中位手术时间135(75~245) min,WIT(24.57±5.51)min。患肾术后GFR(35.50±7.81)ml/(min·1.73 m2),与术前比较差异有统计学意义(P<0.001),患肾GFR保存率为(74.65±11.10)%。术后6个月患肾FPV保存率为(84.28±4.37)%,与术前比较明显减少(P<0.001)。患肾FPV保存率与患肾GFR保存率呈极强正相关(r=0.802);WIT与患肾GFR保存率呈中等程度负相关(r=-0.503)。多元线性回归分析结果显示,术前患肾GFR(b=-0.150,P= 0.008)、WIT(b=-0.443,P<0.001)、患肾FPV保存率(b=1.638,P<0.001)是患肾GFR保存率的独立预测因素。WIT>25 min组和≤25 min组的患肾GFR保存率分别为(68.77±10.88)%和(79.34±8.88)%,差异有统计学意义(P<0.001)。
结论
在WIT较短(<30 min)的情况下,正常肾组织数量的保留是影响NSS术后肾功能预后的重要因素,有限的WIT起次要作用。在保证肿瘤完整切除的前提下,应尽可能保留更多的正常肾组织,同时尽量将WIT控制在25 min以内。
*
*
肾癌是泌尿系统最常见的恶性肿瘤之一,约占成人所有肾恶性肿瘤的90%[1],我国肾癌发病率每年以6.5%的速度显著增长[2]。随着人们对身体健康的关注及横断面影像学检查技术的提高,局限性肾肿瘤的检出率逐渐升高[3]。对于局限性肾肿瘤来说,保留肾单位手术(nephron sparing surgery,NSS)具有与根治性肾切除术(radical nephrectomy,RN)相似的肿瘤学预后,且能够更好地保护患者肾功能[4-6]。目前,NSS已成为局限性肾肿瘤的标准治疗方法[7]。NSS术后新的肾小球滤过率(glomerular filtration rate,GFR)基线是长期生存的重要预测因素,尤其是对于术前存在慢性肾脏病(chronic kidney disease,CKD)的患者[8-9]。相比RN,NSS最大的优势是更好地保留肾功能,减少术后慢性肾功不全的发生率,然而,NSS术后患者仍会出现不同程度的肾功能损伤。既往的研究结果显示,术中缺血损伤是影响术后肾功能最重要的、可改变的决定因素,最近的研究[10-13]结果则表明术后残留肾体积(肾组织的数量)可能取代肾缺血损伤,成为影响术后肾功能最重要的因素。目前,关于NSS术后肾功能预后的影响因素仍存在争议。本研究回顾性分析2016年12月至2018年12月在西京医院接受NSS治疗的肾肿瘤患者的病例资料,探讨NSS术后肾功能预后的影响因素。
对象与方法
一、一般资料
本组115例,男75例,女40例。年龄(49.50±12.94)岁。体质指数(24.59±3.59)kg/m2。既往有吸烟史28例,饮酒史8例;伴糖尿病18例,高血压病31例。美国麻醉医师协会(American Society of Anesthesiolog,ASA)评分(2.03±0.16)分。肿瘤位于左侧53例,右侧62例;肿瘤最大径(3.66±1.32)cm;R.E.N.A.L.评分(6.43±1.60)分。所有患者术前均行腹部CT检查和99Tcm-DTPA肾核素扫描。除外孤立肾、合并慢性肾功能不全、多发肾肿瘤患者。术前血肌酐值(87.44±14.98)μmol/L。术前患肾GFR(48.22±11.48)ml/(min·1.73m2),健肾GFR(49.73±11.96)ml/(min·1.73m2),总GFR(97.95±21.32)ml/(min·1.73m2),术前患肾有功能的肾组织体积(functioning parenchymal volume,FPV)(132.23±9.11)cm3。61例行腹腔镜肾部分切除手术(laparoscopic partial nephrectomy,LPN),54例行机器人辅助腹腔镜肾部分切除手术(robotic assisted laparoscopic partial nephrectomy,RALPN)。
二、观察指标
记录手术时间、热缺血时间(warm ischemia time,WIT)、术中出血量、术后住院时间、术中及术后输血例数、术后并发症、术后病理学结果。所有患者术后6个月均行腹部CT、99Tcm-DTPA肾核素扫描及常规复查项目(血常规、尿常规、肝肾功、电解质、胸部X线片),记录术后6个月血肌酐、患肾GFR、健肾GFR、总GFR、GFR保存率(术后GFR与术前GFR的比值)、患肾FPV、患肾FPV保存率(术后患肾FPV与术前FPV的比值)。参考文献[10],利用患者手术前后CT影像测量患肾体积。
三、统计学方法
采用SPSS 21.0统计软件处理数据,符合正态分布的计量资料采用Mean±SD表示,不符合正态分布的计量资料采用中位数(范围)表示;计数资料采用频数或百分比表示。患者手术前后肾功能和患肾FPV比较采用配对样本t检验。采用Spearman秩相关分析评估各研究因素与患肾GFR保存率之间的相关性。多因素分析采用多元线性回归模型分析患肾功能的独立预测因素。以WIT=25 min为截断点将患者分为≤25 min组和>25 min组,比较两组术前患肾GFR,以及术后6个月的患肾GFR和患肾GFR保存率。以P<0.05为差异有统计学意义。
结果
本组115例手术均顺利完成,无中转开放或转行RN病例。中位手术时间135(75~245) min。WIT(24.57±5.51)min,≤25 min组64例,>25 min组51例。中位术中出血量50(10~2 200) ml。中位术后住院时间6(4~13) d。6例术中及术后输血。术后病理检查均无阳性切缘,恶性肿瘤110例,良性肿瘤5例;其中透明细胞癌96例,乳头状肾癌5例,嫌色细胞癌5例,Xp11易位性肾癌4例,血管平滑肌脂肪瘤5例。
术后6个月血肌酐值(88.42±16.37)μmol/L,与术前比较差异无统计学意义(P>0.05)。术后6个月患肾GFR(35.50±7.81)ml/(min·1.73m2),与术前比较显著降低,差异有统计学意义(P<0.001),患肾GFR保存率为(74.65±11.10)%;健肾GFR(53.08±11.92)ml/(min·1.73m2),与术前相比代偿增高(P<0.001),健肾GFR保存率为(108.87±20.45)%;总GFR(88.59±16.31)ml/(min·1.73m2),与术前比较明显降低(P<0.001),总GFR保存率为(91.85±12.66)%。术后6个月患肾FPV(112.07±6.89)cm3,与术前比较明显减小(P<0.001),患肾FPV保存率为(84.28±4.37)%。
肿瘤最大径、R.E.N.A.L.评分、手术方式、术前患肾GFR、WIT、患肾FPV保存率与患肾GFR保存率有相关性(P<0.05,表1)。其中,患肾FPV保存率与患肾GFR保存率呈极强正相关,即患肾FPV保存率越大,患肾GFR保存率越高(r=0.802,图1A);WIT与患肾GFR保存率呈中等程度负相关,即WIT越长,患肾GFR保存率越低(r=-0.503,图1B)。多元线性回归分析结果显示,术前患肾GFR(P=0.008)、WIT(P<0.001)、患肾FPV保存率(P<0.001)是患肾GFR保存率的独立预测因素(表1)。
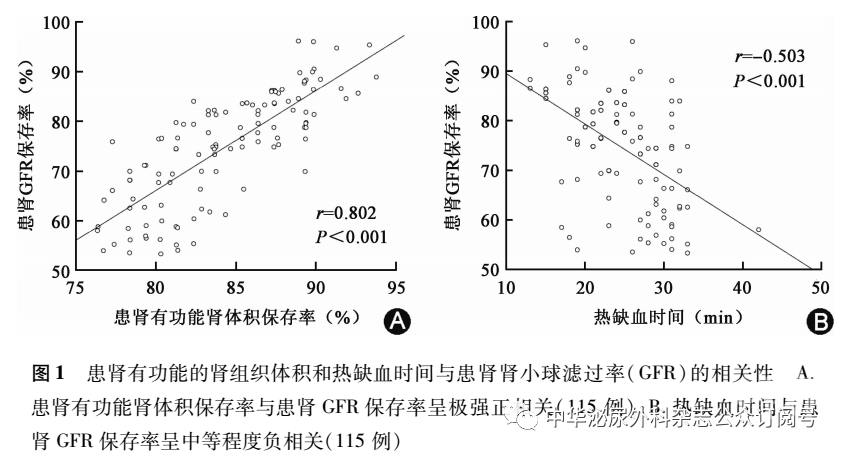
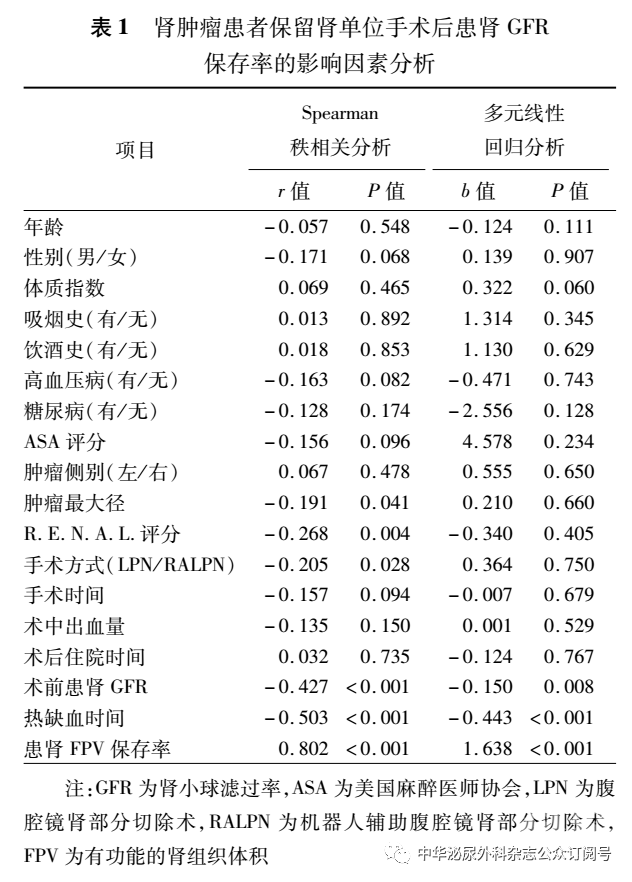
WIT≤25 min组和>25 min组的WIT分别为(20.50±3.29)min和(29.67±2.81)min;术前GFR分别为(47.77±11.57)ml/(min·1.73m2)和(48.79±11.45)ml/(min·1.73m2),差异无统计学意义(t=-0.470,P=0.639);术后6个月患肾GFR分别为(37.33±7.40)ml/(min·1.73m2)和(33.22±7.78)ml/(min·1.73m2),差异有统计学意义(t=2.892,P=0.005);患肾GFR保存率分别为(79.34±8.88)%和(68.77±10.88)%,差异有统计学意义(t=5.607,P<0.001)。
讨论
肾癌对放化疗均不敏感,手术切除是其最重要的治疗方式,既往主要采用RN。越来越多的研究结果表明,与RN相比,NSS具有与其相似的控瘤效果,且肾功能可以得到更好的保留,从而降低肾肿瘤患者术后心血管事件发生率,减少住院和死亡风险,改善生活质量,提高术后总体生存率[13-14]。目前,NSS已取代RN成为T1a期肾癌的首选治疗方式[7]。随着微创技术特别是机器人辅助腹腔镜技术的发展及经验积累,极大地推动着NSS的应用,欧洲泌尿外科学会和美国泌尿外科学会指南均建议将NSS的适应证逐步扩大到T1b期甚至T2期等更复杂的肾肿瘤治疗中[7,15]。NSS术式最重要的目的是在保证完整切除肿瘤的前提下最大限度地保存患者肾功能,但NSS术后患者肾功能仍会出现下降。多数研究结果表明,NSS术后患肾功能约下降20%,总肾功能约下降10%,对侧肾功能出现轻微代偿,增加了4%~6%[11,16]。
传统观点认为缺血再灌注损伤是NSS术后肾功能下降最重要的可改变因素,冷缺血具有保护作用,应避免长时间的热缺血。然而,关于安全的WIT阈值仍未达成共识,一些学者认为WIT>30 min患肾功能会出现不可逆的损伤[12],也有学者认为WIT为40~55 min仍是安全的[17-18]。Thompson等[19]研究发现,WIT每增加1 min,术后发生急性肾衰竭的风险增加5%,新发的CKD Ⅳ期风险增加6%。最近的研究结果表明,WIT>25 min者的术后肾功能会出现不可逆损伤,应尽量将WIT控制在25 min以内[20-21]。以上研究均未将残留肾体积纳入分析中,结果可能具有误导性,因为进一步的研究结果表明缺血时间可能更主要体现了手术的复杂性[16,22]。
Lane等[23]将残留肾体积纳入NSS术后肾功能预后的分析,发现缺血时间不是预测因素,而残留肾体积和术前GFR是术后肾功能的独立预测因素。Thompson等[24]对既往的研究加入肾体积进行重新分析,发现肾组织体积保存率(P<0.001)和术前估算肾小球滤过率(estimated glomerular filtration rate,eGFR)(P<0.001)是术后新发CKD Ⅳ期的独立预测因素,WIT不是预测因素(P=0.137);对WIT进行亚组分析发现,WIT>25 min组与新发CKD Ⅳ期相关(HR=2.27,P=0.049)。Simmons等[10]将肾脏以近似圆柱体的方法测量肾体积,多变量分析结果表明,术前eGFR(P<0.001)和WIT(P=0.02)与围手术期eGFR最低值相关,而只有术前eGFR(P<0.001)和FPV(P=0.04)与远期eGFR相关。与此相似,Ginzburg等[25]发现WIT仅与术后早期肾功能相关(P<0.001),术前eGFR(P=0.006)和FPV(P=0.001)与术后6个月肾功能相关,而WIT与术后6个月肾功能无关(P=0.946),认为术中尽可能多地保存肾组织是术者的首要任务。
大多数研究通过血肌酐值计算总肾功能(eGFR),不能评估患肾和健肾功能的变化情况,忽视了健侧肾脏的代偿作用,低估了患肾功能损伤程度,无法为缺血损伤的影响提供公正和准确的评估,从而降低了研究结果的真实性。本研究通过99Tcm-DTPA肾核素扫描测定患者手术前后的双肾GFR,结果显示手术前后患肾GFR比较差异有统计学意义(P<0.001);与术前相比,术后6个月健肾肾功能代偿增高。本研究结果显示,患肾FPV保存率与患肾GFR保存率呈极强正相关,WIT与患肾GFR保存率呈中等程度负相关;术前患肾GFR、WIT、患肾FPV保存率是患肾GFR保存率的独立预测因素;术后6个月WIT>25 min组的患肾GFR保存率明显低于≤25 min组。这些结果表明保留肾组织的数量是NSS术后肾功能预后关键的可改变因素,有限的WIT起次要作用,行NSS时在保证完整切除肿瘤的前提下,应注重保留更多的肾组织,同时尽量将WIT控制在25 min以内。
越来越多的研究结果表明,正常肾组织数量的保存是影响NSS术后肾功能最重要的因素,缺血起次要作用[11-12,26]。为更多地保存肾组织,越来越多的技术应用于NSS中。术前可以通过CT三维可视化重建等精细的影像学技术更准确清晰地了解肿瘤和肾脏解剖学特征[26-27];手术方式采用肿瘤摘除术(沿着肿瘤组织与周围正常肾组织形成的自然解剖平面将肿瘤钝性摘除)和术中优化肾修复重建过程,从而可以更加精确地切除肿瘤、保护邻近肿瘤的血管和保留更多的正常肾组织,而且肿瘤摘除术的切缘阳性率、肿瘤学预后与标准的NSS相似[28-29]。
本研究存在一定的局限性:纳入研究的患者WIT普遍较短,平均为(24.57±5.51)min;而WIT越长,对肾功能影响越大,因此本研究结论可能并不完全适用于WIT更长的患者。另外,本研究为回顾性研究,且涉及的变量较多,对统计学数据量要求较高,而本研究样本量仅为115例,对研究结论的准确性造成一定的影响,因此,仍需更大样本量的前瞻性随机对照研究进一步探讨。
综上所述,在WIT较短(<30 min)的情况下,正常肾组织数量是影响NSS术后肾功能最重要的可改变因素,有限时间的热缺血损伤起次要作用。在保证肿瘤完整切除的前提下,应尽可能保留更多的正常肾组织,同时尽量将WIT控制在25 min以内。
参考文献(略)

原创声明
《中华泌尿外科杂志》公众订阅号
本文为《中华泌尿外科杂志》原创文章,版权归中华医学会所有。其他媒体、网站、公众号等如需转载本文,请联系本刊编辑部获得授权,并在文题下醒目位置注明“原文刊发于《中华泌尿外科杂志》,年,卷(期):起止页码”。谢谢合作!
长按识别二维码关注我们
中华泌尿外科杂志公众订阅号
来源:gh_665d9f201542 中华泌尿外科杂志公众订阅号
原文链接:http://mp.weixin.qq.com/s?__biz=MzU5NTM4MjI0Mw==&mid=2247484773&idx=1&sn=a4a020b1361a1f02bad3756a947805e7&chksm=fe739fe9c90416ffdf989d851746893ccd96793c069d76a06960e591b1e25f40e8d6845a1199&scene=27#wechat_redirect
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



