来源:CBG资讯

自锂离子电池问世以来,过渡金属氧化物(TMOs)一直被认为是唯一的基于阳离子氧化还原的活性阴极材料。这些特定的TMO阴极材料具有相对较高的锂离子存储容量,因此具有较高的预期能量密度。然而,随着结构的破坏和气态氧的最终释放,TMOs的稳定性开始迅速恶化。因此,最近的研究更多地侧重于锂离子过量的无序化岩盐材料,这也有望为阴离子氧化还原材料提供更大的能量密度和更高的电化学稳定性。 在不到十年的时间里,这一领域的研究取得了迅速的进展,建立了新材料赖以为基础的机制和知识框架。本文提供了一个将各种电池领域统一进行讨论的机会,将在纯阳离子氧化还原(CR)、阳离子和阴离子混合氧化还原(CAR)和纯AR(阴离子还原)之间架起一座桥梁,为这些技术建立一个清晰的讨论场景。
阴阳离子氧化还原的基本原理 锂离子电池中阴离子氧化还原作用的实验证据 在已发表的工作中,也许最具说服力的CAR光谱证据来自于电子准核磁共振光谱(EPR)、X射线吸收光谱(XAS)和共振非弹性x射线散射(RIXS)。由于任何O氧化都可能在O2–的氧化过程中产生自由基,因此EPR是一种理想的识别此类化学物质的技术。使用XAS可以检测活性物质中O的化学环境变化,从而证明CAR的存在。 此外,RIXS可以探测TMO在一定激发能量范围内的发射光谱的能量谱。这有效地将XAS中的发射信息从2D(点对激发能)扩展到3D(点对激发能和发射能),即将XAS吸收光谱上的每个点扩展为对应的全能分辨发射光谱。 总的来说,阴离子氧化还原的证据主要是通过X射线衍射(XRD)、X射线光电子能谱(XPS)、XAS、RIXS、EPR和微分电化学质谱(DEMS)的组合来获得的,这些表征技术令人信服地表明CAR出现在一些TMOs中,并为验证和识别新的CAR材料奠定了基础。
阴离子氧化还原的机理 究竟是什么使特定的TMOs的CAR活性和可逆,在阴离子氧化还原的研究历史上有许多不同的理论。首先,从XAS的研究中,许多研究人员认为CAR和O2–/O–氧化还原电对相关。其次,在Li–O2电池中,就形成Li2O2而言AR可能不是一个完美的O2–/O–氧化还原电对,反而会形成诸如类过氧O2n–二聚体或是单独的O–阴离子之类的氧化O。重要的是要表明AR氧化还原位点的物理位置和相应的TMO晶体结构的变化发生在整个TMO粒子体中。因此,只有采用专门的空间分辨分析技术才能对氧的大量氧化还原进行分析。 额外容量来自作为氧化还原中心的O原子这一理论得到了广泛接受。对于富锂层状材料,阴离子氧化还原的机理被许多团队描述为基于TM–O键的共价程度。当锂离子被除去时,O和TM都可以作为氧化位点为外部电路提供电子。然而,由于O的电负性很强,由TM和O组成的化合物通常会导致TM的O的2p带和d带之间发生明显分离(通常是纯CR材料的氧化还原活性中心)。 当AR发生时,从TMO中移出的电子来自于O(即AR),当2O2–被氧化后,就会形成一个单一的(O2)2–过氧化物。与此同时,O的2p分裂成σ、σ*、π和π*,如图1所示。随着越来越多的锂离子从系统中被剥离,O2最终释放。有趣的是,如果AR和CR的机制只与TM–O键的共价或它们的杂化有关,那么系统的总容量仍然不应该超过TM预测的理论极限。
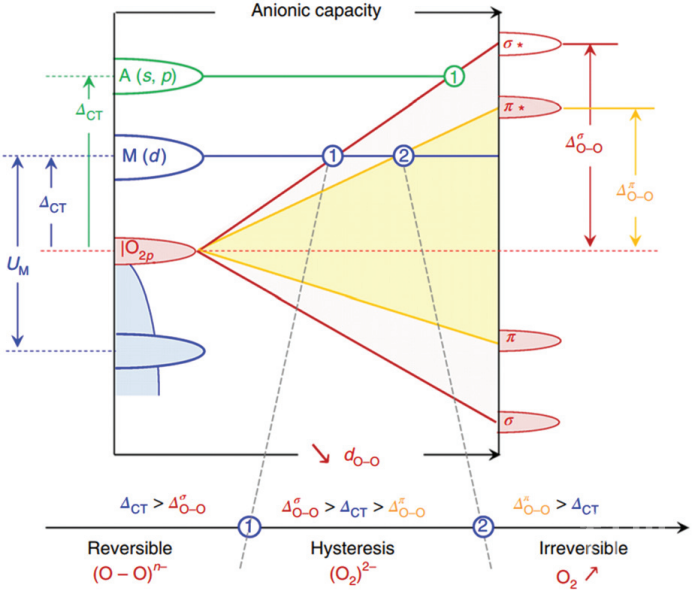
图 1 具有可逆、滞后和不可逆阴离子氧化还原的TMO定性电子结构(来源:Chem. Soc. Rev.)
另一种衡量CAR可逆性和程度的方法是Li和TM的比值以及特定线性Li–O–Li键的存在。这种方法与传统的共价键不同,它允许与传统的共价键无关的附加容量。除了富Li系统和TMO所依赖的状态(莫特–哈伯德或电荷转移)或共价程度之外,Doublet等人最近提出,每个氧的空穴度是一种更普遍、更准确的可逆CAR指标。
阳离子和阴离子氧化还原的光谱 阴离子氧化还原
在阴离子氧化还原的发展时间表中,它的定义有了很大的变化。目前,AR被认为是非键O 2p态的可逆消长,其中O 2p中产生的电子空穴仍然存在于具有O特性的轨道中,即使在整个脱硫过程中的结构和电子重组之后也是如此。然而,随着研究的进展,这一定义可能会继续演变。是否应该将某物归类为AR将继续在研究界进行讨论。不过,最近在Li–O2领域的一些工作仍然不可否认地是AR的某种极端形式,其中存在氧化还原活性TM对Li的完全替代。
Li–O2和Li–S电池
Li–S和Li–O2电池为100% AR,与CAR和CR具有显著不同的特性。从根本上说,S8或O2的锂化被称为转化反应。在转化反应基TMO阳极的情况下,这些硫族化合物的晶体中没有Li离子的插层。虽然纯硫族化合物的TMOs的转化反应机理在循环稳定性和库仑效率方面存在重大问题,但它们在比能量密度和体积能量密度方面都具有巨大的潜力。总的来说,这两种体系大多被认为是从氧化状态为0到–2或–1(在Li2O2的情况下)的完全氧化还原反应。
研究表面,当Li2O足够小,并且有催化剂(通过一些不清楚的机制)时,如图2a所示,有可能实现从O2–到Ox(x~–0.5)的部分氧化。在EPR(图6b)和Raman(图6c)中,有令人信服的证据表明,充入600 mAh/g后,样品中存在LiO2。在~2.5 V左右出现电压平台,这正是图6d所示的低过电位LiO2的电池电压。
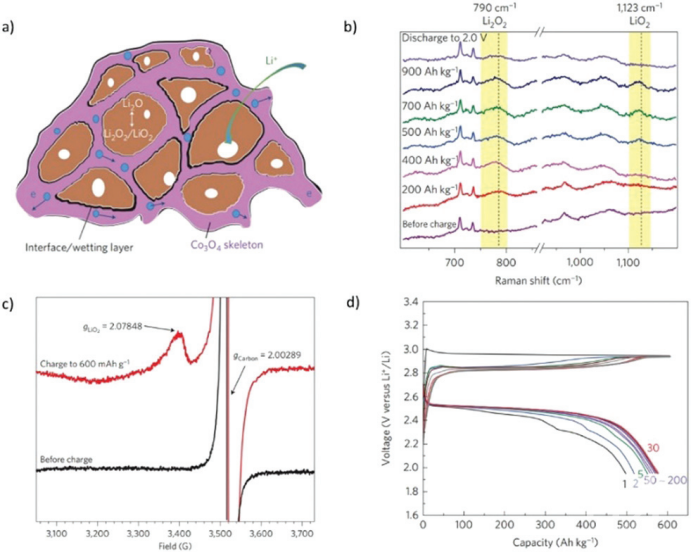
图 2 (a) Co3O4骨架中Li2O的分布。(b)电极在不同SOC下的Raman和(c)电子顺磁共振图谱。(d)不同循环条件下的电压图谱。
(来源:Chem. Soc. Rev.)
可逆的阳离子和阴离子氧化还原 富锂层状阴极材料富锂层状氧化物是一种特殊类型的TMO,具有特别高的容量,被认为是一类由LiMO2(其中M=Mn,Ni,Co)组成并由Li2MnO3稳定的材料。富锂层状氧化物涉及的主要问题是其低的第一圈循环库仑效率,较差的能量密度稳定性和较差的倍率性能。虽然容量保持相对较好,但由于众所周知的电压衰减现象,能量输出在循环过程中迅速减少。目前尚不清楚AR是否是其容量增加和耐久性差的原因。这种类型的阴离子氧化还原材料实际上是有史以来第一次证明可逆的(某种程度上)CAR。
在循环过程中,Mn、Co和Ni的边缘位置与它们的氧化状态有关。由于氧化态与Mn、Co和Ni的边缘能之间存在良好的线性关系,因此可以很容易地推导出氧化过程中TM的变化。然后从总测量容量中减去TM对容量的总电荷贡献,得到O氧化还原的半定量贡献。如图3a所示。总容量从第一个周期到第83个周期略有变化(降解主要以电压的形式发生)。在Co2+/Co3+和Mn3+/Mn4+氧化还原对(补偿了Ni和O的容量降低)的激励下,系统的费米能级增加,因此,能观察到电压下降(图3b)。

图 3 (a)容量中Mn,Co,Ni,O元素的贡献。(b)循环过程中Li1.2Ni0.15Co0.1Mn0.55O2电子结构的变化
(来源:Chem. Soc. Rev.)
在大多数情况下,特别是在这类材料的早期研究中,AR的稳定性很差。在较高的充电电压下,O2的释放是非常常见的,这与循环稳定性差直接相关。除了涂层外,通过掺杂其他金属,可以更容易地在整个LMR颗粒中抑制O2的形成。这些外来元素具有增强TMO电导率和整体稳定性的效应。
可逆阳离子氧化还原稳定的阳离子氧化还原基阴极被广泛认为是实现LIBS的领先技术进步。如图4a所示,NMC811的循环伏安法(CV)在4.1 V时显示出明显的氧化峰,而NMC111和NMC622的成分在4.4 V以上仍保持相对稳定。如图4b所示的电化学质谱清楚地表明,O2的释放与CV中观察到的氧化峰相一致。
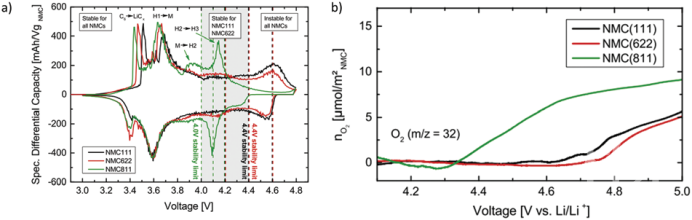
图 4(a) NMC111,622,811的CV曲线。(b) 对应的O2生成图谱。
(来源:Chem. Soc. Rev.)
结论阴离子和阳离子氧化还原将继续在实现高能量密度锂离子电池方面发挥作用。总的来说,CAR的识别和证据围绕着共振非弹性X射线散射的使用。更具体地说,从CR分离的AR应该在~530.9eV和522.8eV的发射能量附近产生信号,两者在不同的工作之间略有不同,但所有这些都不同于在所有激发能量中发射能量为522–527 eV的宽峰。随着先进表征技术的不断发展,作者对CAR的理解和识别也将继续发展。
在电池制造工艺(电解质和阳极的变化)没有重大变化的情况下,包含AR的LIBs提供更高能量密度的能力使这种材料对工业具有高度的吸引力。CAR在商业化之前仍然存在许多障碍。阴离子氧化还原的具体定义传统上是指与TM氧化还原分离的O氧化还原。在这种情况下,O氧化还原增加了系统的容量。这种类型的氧化还原还没有被证明容量和电压在任何足够程度上都是可逆的。相反,β–Li2IrO3被证明是稳定的,产生了稳定的循环且具有较小的电压衰减。此外,对Mn2+/Mn4+双氧化还原(类似于多价Ir氧化还原的β–Li2IrO3)也显示出良好的能量密度,具有较小的电压衰减和良好的容量保持能力。似乎一个基于CAR的系统是不实际的,而高价阳离子氧化还原与轻微增加或提高能力的AR则可能更有希望。
论文信息:Matthew Li, Tongchao Liu, Zhongwei Chen, Khalil Amine, Cheng Zhong and Jun Lu. "Cationic and anionic redox in lithium-ion based batteries." Chemical Society Reviews (2020). DOI: 10.1039/C8CS00426A.
来源:BeanGoNews CBG资讯
原文链接:https://mp.weixin.qq.com/s?__biz=MzI4ODQ0NjUwMg==&mid=2247499953&idx=2&sn=a67f50cec4b534aa186cda3b9e2a84db&chksm=ec3cc1f8db4b48ee548edc4b96eeba6442c6daa2cd2dc7db429ff4af7d58a7c236d454b323e9#rd
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn



