来源:植物生物学
2021年1月3日,Current Opinion in Plant Biology 在线发表美国马里兰大学戚益平(Yiping Qi)团队的题为CRISPR/dCas-mediated transcriptional and epigenetic regulation in plant的综述文章。本文综述了CRISPR/ dCas介导的转录激活和抑制以及表观遗传修饰的最新研究进展。同时还着重展望了CRISPR/dCas系统在植物中的未来发展方向及更广泛的应用前景。

CRISPR/Cas系统介导的精确基因组编辑因其易用性和多功能性而彻底改变了基因组工程。催化失活的Cas变异体(dCas)进一步扩大了CRISPR/Cas系统在遗传学研究和翻译研究中的应用,而不会导致DNA双链断裂。不同的效应域与dCas蛋白的融合使CRISPR/dCas系统成为基因表达调控、表观遗传调控和序列特异性成像的多功能平台。在这篇简短的综述中,作者综述了CRISPR/dCas介导的转录激活和抑制以及表观遗传修饰的最新进展;并指出了CRISPR/dCas系统在植物中的未来发展方向和更广泛的应用前景。
CRISPR/Cas基因编辑技术自问世以来,由于其操作的简易性,已成为植物研究中普遍使用的基因敲除工具。但是,CRISPR/Cas技术在基因敲除过程中产生的DNA双链断裂可能引起染色体的意外缺失或重排。因此,不依赖DNA双链断裂的基因失活工具同样值得关注与推广。另一方面,基于cDNA超表达的基因激活面临转基因沉默以及多基因超表达时工作量倍增等缺点,使得植物基因激活工具同样具有巨大的需求和广阔的运用空间。
Deactivated Cas (dCas)是指通过点突变失去核酸酶活性的Cas蛋白。dCas蛋白(如dCas9) 可与转录抑制结构域(TRD)或转录激活结构域(TAD)融合,dCas蛋白可以与效应蛋白融合,包括转录激活子、抑制子和表观调节子,分别实现有效的基因特异性CRISPR介导的激活(CRISPRa)、干扰(CRISPRi)和表观基因组修饰。
dCas:一个超越基因组编辑的可编程平台
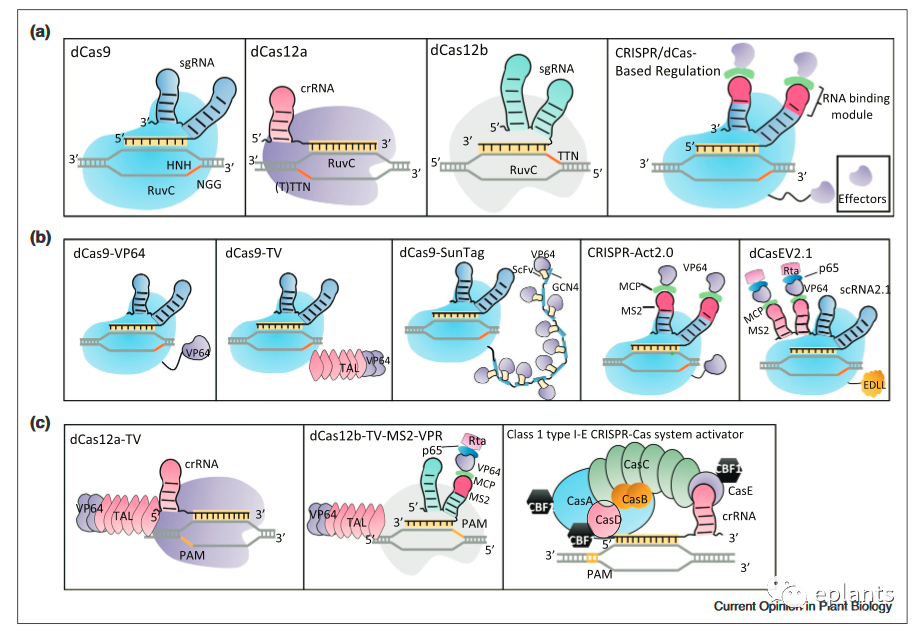
植物中的CRISPR/dCas和CRISPRa系统
A. dCas9/12a/12b介导的CRISPR复合物及其在转录调控中的应用.
sgRNA由反式激活crRNA (tracrRNA)和CRISPR RNA (crRNA)组成。在dCas9中发生HNH和RuvC结构域突变,在dCas12a和dCas12b中发生RuvC结构域突变。效应因子包括激活因子、抑制因子或表观遗传修饰因子。NGG、(T)TTN、TTN分别代表Cas9、Cas12a、Cas12b的PAM核苷酸序列.
B. 基于dcas9的第一代和第二代激活系统的示意图。
在dCas9-VP64中,转录激活因子VP64直接与dCas9融合;在dCa9-TV中,一个由6个TALE TAD motif和2个VP64组成的强效激活因子TV直接融合到dCas9中;在dCas9-SunTag中,小肽GCN4的10个串联重复序列被用来招募多拷贝与转录激活因子VP64融合的单链抗体。单链可变片段;在CRISPR-Act2.0中,sgRNA支架被修饰为包含两个MS2 RNA适配体,招募MS2噬菌体外壳蛋白(MCP)与转录激活因子VP64融合,dCas9与VP64融合;在dCasEV2.1中,两个MS2 RNA适配体融合到sgRNA2.1支架的3 '端,MCP融合到组合转录激活子VP64-p65-Rta (VPR), dCas9融合到转录激活子EDLL。VP64,四份单纯疱疹病毒蛋白16 (VP16);TAL, TAL效应因子转录激活域;核因子kappa B激活域p65;大鼠,eb病毒R反激活因子;EDLL是AP2/ERF转录因子中的一个有效的植物转录激活域。
C dCas12a/b和一类I-E型基于CRISPR- cas的激活系统的示意图。
在dCas12a-TV中,将一个强效激活TV熔合到dCas12a上;在dCas12b-TV-MS2-VPR中,sgRNA支架被修饰为包含一个MS2 RNA适配体,以招募MCP与转录激活因子VPR的融合,dCas9被融合到激活因子TV中;在一类I-E型CRISPR-Cas激活因子中,来自嗜热链球菌DGCC7710的一类I-E型CRISPR-Cas系统由CasA、CasB、CasC、CasD、CasE和crRNA组成,一个植物转录激活域CBF1融合到CasA、CasD和CasE的c端。
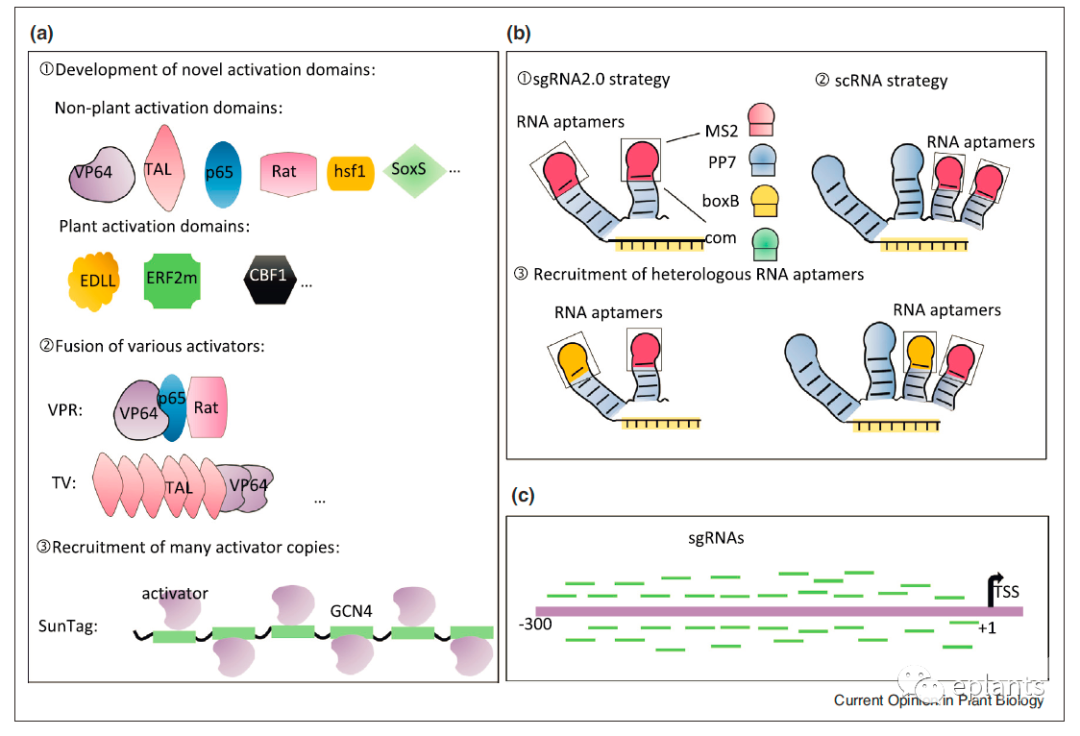
增强CRISPRa效力的策略
(a)开发强大的转录激活因子:
通过招募有效的激活域可以显著提高CRISPRa的激活效价。VP64、TAL、p65、Rat、hsf1和SoxS是非植物性激活域,EDLL、ERF2m和CBF1是植物性激活域。串联不同激活域的dCas蛋白和基于SunTag的多个激活因子副本的融合可以增强CRISPRa的激活效力。VP64,四份单纯疱疹病毒蛋白16 (VP16);TAL, TAL效应因子转录激活域;核因子kappa B的反激活域p65;大鼠,eb病毒R反激活因子;hsf1,人热休克因子1;AP2/ERF转录因子的植物转录激活域EDLL乙烯反应因子修饰的植物转录激活域ERFmCBF1,一个来自拟南芥冷结合因子1的c端酸性植物转录激活域。
(b) CRISPR RNA支架的优化:
具有MS2、PP7、boxB或com RNA适配体的sgRNA支架可以招募其同源RNA结合蛋白融合到激活域来激活基因表达。多个正交的rna结合模块可以被采用到一个sgRNA支架中,这允许招募相同或不同的激活剂。
(c) 优化CRISPRa的靶向位置:
CRISPRa受sgRNA相对于靶基因转录起始位点(TSS)的位置影响。MS2、PP7、boxB、com代表RNA适体。
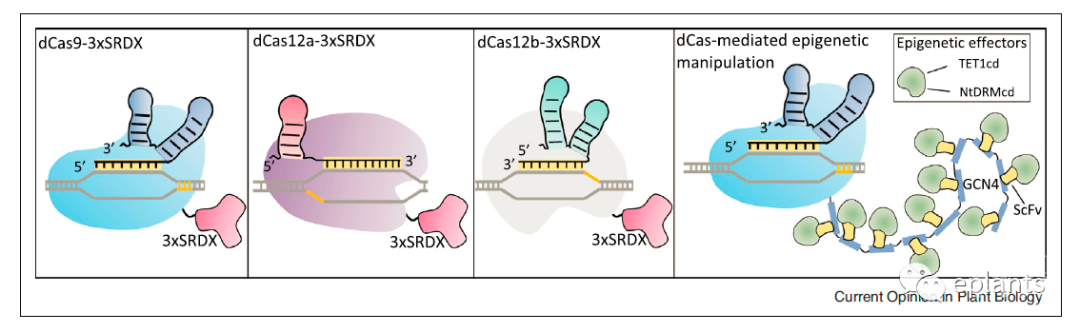
CRISPR/ dCas介导的抑制和表观遗传操作系统
dCas9/12a/12b-3xSRDX抑制因子和dCas-SunTag系统介导的表观遗传修饰因子的图示。3xSRDX阻值可以通过dCas/sgRNA复合体被招募到靶位点。dCas蛋白的转录抑制作用可以通过融合不同抑制域的dCas蛋白来提高。基于SunTag系统,多个融合到scFv的表观遗传修饰体TET1cd或NtDRMcd被dCas/sgRNA复合物招募到特定的位点。
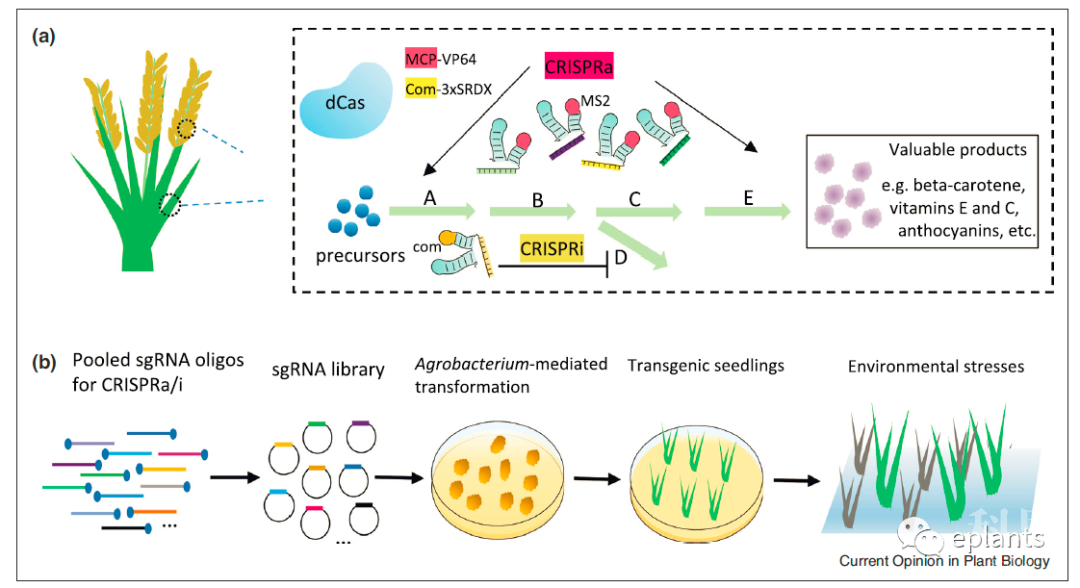
CRISPR-dCas技术在植物中的未来应用
(a)使用CRISPR激活(CRISPRa)和CRISPR干扰(CRISPRi)系统的重组代谢工程流程。CRISPR-dCas平台可以同时干扰通路的多个部分,从而重定向通量并提高分支代谢通路所需产物的输出。用MS2发夹构建的sgRNA招募融合到VP64的MCP激活A、B、C、E的基因表达,用com发夹构建的sgRNA招募com融合到3xSRDX,抑制D的基因表达。
(b)基于CRISPRa/i的高通量筛选控制植物发育和环境胁迫响应的关键基因
sgRNA文库可能针对整个基因组、基因家族或具有相关功能的基因群。sgRNAs可以与与激活或抑制因子融合的选定的dCas蛋白一起转化到植物中。sgRNAs在具有有趣性状的选择群体中的靶位点可以通过深度测序来揭示。
来源:PlantBiotech 植物生物学
原文链接:http://mp.weixin.qq.com/s?__biz=MzI5NTk2MTcyOA==&mid=2247494571&idx=2&sn=0851ad503ac473bce483ac215739ae2e
版权声明:除非特别注明,本站所载内容来源于互联网、微信公众号等公开渠道,不代表本站观点,仅供参考、交流、公益传播之目的。转载的稿件版权归原作者或机构所有,如有侵权,请联系删除。
电话:(010)86409582
邮箱:kejie@scimall.org.cn